
Поливанова А.Г._Высокоэффективная жидкостная хроматография БАВ
.pdfМинистерство образования и науки Российской Федерации
Российский химико-технологический университет имени Д. И. Менделеева
А. Г. Поливанова
Высокоэффективная жидкостная хроматография
биологически активных веществ
Лабораторный практикум
Утверждено Редакционным советом университета в качестве учебного пособия
Москва
2013
УДК 543.544.5.068.7 (076) ББК 24.4я7
П50
Рецензенты:
Кандидат химических наук, старший научный сотрудник Института элементоорганических соединений им. А. Н. Несмеянова РАН
Ю. В. Фёдоров
Доктор химических наук, профессор, заведующий кафедрой аналитической химии РХТУ им. Д. И. Менделеева
В. В. Кузнецов
Поливанова А. Г.
П50 Высокоэффективная жидкостная хроматография биологически активных веществ. Лабораторный практикум.: учеб. пособие / А. Г. Поливанова. – М. : РХТУ им. Д. И. Менделеева, 2013. – 56 с.
ISBN 978-5-7237-1053-5
Настоящее пособие составлено в соответствии с программой практических занятий курса «Современные физико-химические методы анализа органических веществ». Целью данного пособия является обучение студентов практическим навыкам работы на жидкостном хроматографе. Пособие содержит описание практических работ по высокоэффективной жидкостной хроматографии биологически активных веществ, кроме того, в нем представлены разделы, касающиеся теории жидкостной хроматографии, устройства и принципов работы жидкостных хроматографов, рассмотрены основные аспекты пробоподготовки образцов, принципы качественного и количественного анализа и обработки хроматографических данных. Для предварительного виртуального обучения работе на жидкостном хроматографе дано краткое руководство пользования компьютерным тренажёром «Жидкостной хроматограф».
Предназначено для студентов, обучающихся по направлению 240100 «химическая технология» и по специальности 020201 «фундаментальная и прикладная химия».
|
УДК 543.544.5.068.7 (076) |
|
ББК 24.4я7 |
ISBN 978-5-7237-1053-5 |
© Российский химико-технологический |
|
университет им. Д. И. Менделеева, 2013 |
|
© Поливанова А.Г., 2013 |
2
ОГЛАВЛЕНИЕ |
|
Введение............................................................................................................. |
5 |
Глава 1. Основные понятия жидкостной хроматографии................................ |
5 |
1.1. Определения жидкостной хроматографии ........................................... |
5 |
1.2. Основные принципы и термины жидкостной хроматографии............ |
5 |
1.3. Основные хроматографические параметры.......................................... |
7 |
1.4. Общие принципы оптимизации хроматографического анализа........ |
11 |
Глава 2. Молекулярная адсорбционная хроматография................................ |
13 |
2.1. Нормально-фазовая и обращёно-фазовая жидкостная |
|
хроматография.............................................................................................. |
13 |
2.2. Подвижные фазы для обращено-фазовой высокоэффективной |
|
жидкостной хроматографии......................................................................... |
19 |
Глава 3. Жидкостной хроматограф................................................................. |
22 |
3.1. Хроматографическая колонка ............................................................. |
23 |
3.2. Основные типы насосов, используемых в высокоэффективной |
|
жидкостной хроматографии......................................................................... |
25 |
3.3. Дозаторы для высокоэффективной жидкостной хроматографии...... |
26 |
3.4. Детекторы для высокоэффективной жидкостной хроматографии.... |
28 |
3.5. Хроматографы «Милихром А-02» и «Альфахром» ........................... |
33 |
Глава 4. Проведение хроматографического анализа...................................... |
35 |
4.1. Качественный и количественный анализ с помощью |
|
высокоэффективной жидкостной хроматографии...................................... |
35 |
4.2. Пробоподготовка в высокоэффективной жидкостной |
|
хроматографии.............................................................................................. |
37 |
4.3. Проведение анализа на жидкостном хроматографе........................... |
43 |
4.4. Работа в программе тренажёр «Жидкостной хроматограф» ............. |
45 |
4.5. База данных для высокоэффективного жидкостного |
|
хроматографа ................................................................................................ |
46 |
4.6. Обработка хроматограмм .................................................................... |
46 |
5. Задания для лабораторного практикума..................................................... |
50 |
Контрольные вопросы для допуска к лабораторной работе.......................... |
53 |
Литература........................................................................................................ |
54 |
3
Список сокращений
ЖХ – жидкостная хроматография НФ – неподвижная фаза ПФ – подвижная фаза
ВЭЖХ – высокоэффективная жидкостная хроматография ЭКР – экстраколоночное расширение пика ЖАХ – жидкостная адсорбционная хроматография
НФЖХ – нормально-фазовая жидкостная хроматография ОФЖХ – обращёно-фазовая жидкостная хроматография ОФ ВЭЖХ – обращёно-фазовая высокоэффективная жидкостная хроматография ЭС – элюирующая сила
УФ-детектор – ультрафиолетовый детектор ДДМ – детектор на диодной матрице
4
Введение
Жидкостная хроматография (ЖХ) – один из основных методов аналитической химии. Она находит применение во многих областях человеческой деятельности: в науке – для решения аналитических и препаративных задач; в промышленности – для контроля качества продукции (фармацевтическое, пищевое, ликероводочное, нефтеперерабатывающее и другие производства); в медицине – для проведения ранней диагностики некоторых заболеваний, изучения метаболизма лекарств в организме; в государственных структурах (Федеральная служба по контролю за оборотом наркотиков, Федеральная служба безопасности, Криминалистические лаборатории Министерства внутренних дел, Антидопинговый комитет и др.) – для проведения криминалистических и судебно-медицинских экспертиз; в природоохранной службе – для мониторинга экологического состояния окружающей среды и в прочих отраслях.
В связи с этим для любого специалиста в области биологически активных веществ, в какой бы химической организации он ни работал, знание основ метода высокоэффективной жидкостной хроматографии (ВЭЖХ) совершенно необходимо.
Глава 1. Основные понятия жидкостной хроматографии
1.1. Определения жидкостной хроматографии
Жидкостная хроматография (ЖХ) – это наука о межмолекулярных взаимодействиях и переносе молекул или частиц в системе несмешивающихся и движущихся относительно друг друга фаз.
ЖХ – это метод разделения смесей веществ или частиц, основанный на различии в скорости их перемещения в системе несмешивающихся и движущихся относительно друг друга фаз.
ЖХ – это процесс дифференцированного многократного перераспределения веществ или частиц между несмешивающимися и движущимися относительно друг друга фазами, приводящий к обособлению концентрационных зон индивидуальных компонентов исходных смесей этих веществ или частиц.
1.2. Основные принципы и термины жидкостной хроматографии
Принцип жидкостной хроматографии состоит в разделении компонентов смеси, основанном на различии в равновесном распределении их между двумя несмешивающимися фазами (компонентами хроматографической системы), одна из которых неподвижна (сорбент), а другая подвижна (элюент).
5
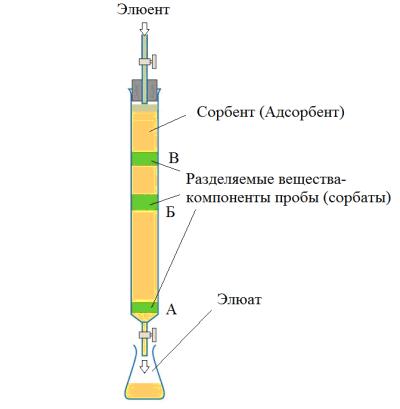
Сорбент – твёрдое вещество, жидкость или их смеси, способные поглощать или удерживать газы, пары или растворённые вещества и используемые в хроматографии в качестве неподвижной фазы.
Адсорбент (неподвижная фаза, НФ) – твёрдый сорбент, концентрирующий на своей поверхности газы, пары или растворённые вещества. Адсорбентом заполнена хроматографическая колонка, в которой, в свою очередь, происходит разделение смеси веществ на отдельные компоненты.
Проба – аликвота анализируемой смеси, вводимая в хроматографическую систему.
Сорбат (адсорбат) – компонент пробы, индивидуальное соединение, внесённое в хроматографическую колонку.
Хроматографическая система состоит из хроматографической колонки (рис. 1), заполненной определённым адсорбентом, через которую при определённой температуре проходит элюент определённого состава.
Элюент (подвижная фаза, ПФ) – растворитель или смесь растворителей, предназначенная для прокачки анализируемой смеси через хроматографическую колонку.
Элюат – раствор, выходящий из хроматографической колонки.
Элюент (или подвижная фаза, ПФ) в жидкостной хроматографии выполняет двоякую функцию:
-обеспечивает перенос десорбированных молекул по колонке;
-регулирует константы равновесия, а следовательно, и удерживание разделяемых веществ в результате взаимодействия с адсорбентом (сорбируясь на его поверхности) и с молекулами этих веществ.
Рис. 1. Хроматографическая колонка
6
ВЖХ природа подвижной фазы имеет существенно большее значение, чем
вгазовой хроматографии. В результате комбинации ограниченного числа сорбентов и неограниченного числа различных по составу подвижных фаз возможно решение чрезвычайно большого числа практических задач.
Метод ЖХ применим для разделения значительно более широкого круга веществ, чем метод газовой хроматографии, поскольку большая часть веществ не обладает летучестью, а многие вещества неустойчивы при высоких температурах. В ЖХ разделение обычно происходит при комнатной или слегка повышенной (40 °С) температуре.
Отличительной особенностью высокоэффективной жидкостной хроматографии (ВЭЖХ) является использование мелкозернистых сорбентов (с размером частиц обычно 3 – 5 мкм, при необходимости до 1.8 мкм) и высокого
давления, |
поскольку, чтобы жидкость могла пройти через трубку длиной |
7 – 25 см, |
плотно упакованную таким сорбентом, необходимо создать |
значительное давление. Элюент при этом подаётся в хроматографическую систему специальными насосами, и рабочее давление в системе может достигать 400 бар.
Метод ВЭЖХ позволяет разделять сложные смеси веществ быстро и полно (среднее время анализа составляет от 3 до 40 минут).
Существуют различные варианты ЖХ в соответствии с характером основных проявляющихся межмолекулярных взаимодействий:
–в ситовой хроматографии разделение компонентов осуществляется за счёт разницы в растворимости молекул при их прохождении (фильтрации) через слой сорбента;
–в адсорбционной хроматографии – за счёт разницы в адсорбируемости молекул, проходящих через слой частиц сорбента, покрытых неподвижной фазой в виде тонкого слоя или поверхностно-привитых радикальных групп;
–в ионообменной и ионной хроматографии – за счёт разницы в способности к обмену ионами с ионообменниками;
Для анализа объектов окружающей среды наиболее широко используют ВЭЖХ в адсорбционном и ионообменном вариантах.
1.3.Основные хроматографические параметры
Хроматограмма – графический результат хроматографического процесса
– кривая, отображающая зависимость сигнала прибора (концентрации вещества) в вытекающей из колонки подвижной фазе от объёма вытекающей фазы или от времени.
Хроматограмма состоит из ряда пиков, каждый из которых при полном разделении соответствует одному компоненту анализируемой пробы. Площадь или высота пика пропорциональна концентрации компонента в элюате.
При передвижении молекул одного вещества в хроматографической системе каждая молекула реально следует по своей собственной траектории
7
вдоль хроматографической колонки. Молекулы с наименьшей траекторией будут двигаться впереди фронта данной фракции, а некоторые молекулы – напротив, будут несколько запаздывать. Основная же часть молекул движется в средней области фракции.
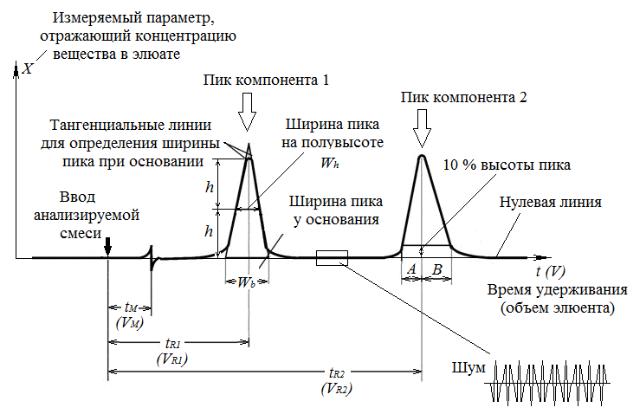
Таким образом, реально молекулы одного вещества будут выходить из колонки в несколько разное время, что определяет форму хроматографического пика вещества как гауссову кривую (рис. 2).
Рис. 2. Хроматограмма
tM – время удерживания несорбируемого соединения; VM – объем удерживания несорбируемого соединения; tR1 и tR2 – абсолютные времена удерживания компонентов 1 и 2 соответственно; VR1 и VR2 - объемы удерживания компонентов 1 и 2 соответственно;
Хроматографический пик – участок хроматограммы, соответствующий площади, ограниченной функцией хроматограммы в момент выхода определяемого вещества из колонки, и базовой (нулевой) линией.
Нулевая (базовая) линия хроматограммы – линия, соответствующая нулевой концентрации анализируемых веществ в элюате.
Шум – помехи, статистические флуктуации нулевой линии хроматограммы (рис. 2). Уровень шума складывается из статистических флуктуаций всех параметров, принимающих участие в образовании сигнала детектора.
Дрейф нулевой линии – постепенное смещение, регистрируемое на хроматограмме.
8
Основание пика – продолжение нулевой линии, соединяющее начало и конец хроматографического пика.
Площадь пика, S – площадь хроматограммы, заключенная между пиком и его основанием. В первом приближении S = h × Wh.
Высота пика, h – расстояние от вершины пика до его основания, измеренное вдоль оси отклика детектора.
Ширина пика на полувысоте, Wh – отсекаемый пиком отрезок линии, проведенной параллельно основанию пика на середине его высоты (рис. 2).
Ширина пика у основания, Wb – отрезок основания пика, отсекаемый двумя касательными, проведенными в точках перегибов восходящей и нисходящей ветвей хроматографического пика (рис. 2).
Геометрический объём колонки, Vc – внутреннее пространство пустой колонки.
Свободный объём, Vo – часть объёма колонки, не занятая сорбентом.
Объём удерживания вещества, VR – объём подвижной фазы,
затрачиваемой на элюирование пробы вещества. Объём удерживания определяют между точкой ввода пробы и точкой, при которой регистрируется максимум сигнала детектора.
Мёртвый объём, VM – объём подвижной фазы между точкой ввода пробы и точкой её обнаружения (кюветой детектора). Мёртвый объём включает в себя свободный объём колонки, объёмы устройства ввода пробы (дозатора), детектора, а также объёмы коммуникаций между ними.
Приведённый объём удерживания вещества, VR' – объём удерживания вещества за вычетом мёртвого объёма: VR' = VR – VM.
Абсолютное время удерживания вещества, tR – время пребывания исследуемого вещества в хроматографе. Практически время удерживания определяют от момента ввода пробы вещества в хроматограф до момента регистрации максимума соответствующего хроматографического пика.
Мёртвое время, tM – время пребывания (удерживания) несорбируемого вещества в хроматографе. На практике мертвое время определяют от момента ввода пробы несорбируемого вещества в хроматограф до момента регистрации максимума сигнала детектора.
Приведённое время удерживания, tR' – абсолютное время удерживания за вычетом мертвого времени: tR' = tR – tM.
Эффективность хроматографической колонки – количество ступеней установления равновесия между подвижной и неподвижной фазами в выбранных условиях для данного сорбата, способность к образованию узкой концентрационной зоны индивидуального компонента разделяемой смеси. Эффективность колонки в численном выражении определяется значениями числа теоретических тарелок (N) и высотой, эквивалентной высоте теоретической тарелки (Н). Чем выше эффективность, тем больше величина N, тем меньше расширение первоначально узкой концентрационной зоны по мере прохождения её через колонку, и тем меньше ширина пика у основания на выходе из колонки. Эффективность целиком и полностью является свойством
9

хроматографической колонки и определяется размером частиц адсорбента, качеством изготовления адсорбента, качеством упаковки колонки адсорбентом и прочими параметрами.
Число теоретических тарелок, N – величина, характеризующая качество колонки и рассчитываемая по параметрам удерживания выбранного вещества
ж tR ц2
по формуле: N =16ґзиWb чш
2
= 5.545ґжз tR цч .
ззWh чч и ш
Высота, эквивалентная высоте теоретической тарелки, H – величина,
характеризующая качество хроматографической колонки и рассчитываемая как
отношение длины колонки (L) к числу теоретических тарелок: H = L .
N
Приведенное число теоретических тарелок, N' – отношение числа реально рассчитанных теоретических тарелок на колонке данной длины к
условной колонке длиной 100 см . N' = 100ґ N , где L - длина колонки в см.
L
Приведенная высота, эквивалентная высоте теоретической тарелки –
H'= H , где d – средний (эффективный) диаметр частиц сорбента (мкм), H' d
также как и Н является характеристикой эффективности колонки. Вполне удовлетворительным принято считать колонки со значением H равным (3 – 3,5) × d. Очень хорошими считаются колонки с Н = 2d.
Фактор удерживания вещества (коэффициент ёмкости), k' – один из основополагающих параметров удерживания в жидкостной хроматографии, безразмерная величина, характеризующая удерживание вещества и равная отношению абсолютного объёма удерживания к свободному объёму колонки
(k'=VN ), а также отношению приведенного времени удерживания к мёртвому
VO
времени k'= tR .
tM
Селективность хроматографической системы (относительное удерживание – αR/cm, фактор разделения – α) – избирательность, способность подвижной и неподвижной фаз к специфическим взаимодействиям с молекулами сорбата, обладающими определёнными структурными признаками, приводящая к разной скорости перемещения концентрационных зон индивидуальных компонентов. Количественно селективность выражается как:
- величина, равная отношению приведенного объёма (времени) удерживания определённого вещества, взятого для сравнения (стандарта) и
хроматографируемого в идентичных условиях α |
|
= |
kR |
= |
tR' |
= |
VR' ; |
|
kcm |
tcm' |
|||||
|
R/cm |
|
|
|
Vcm' |
- величина, которая пропорциональна отношению приведенных времен
удерживания двух веществ α= tR2 -tM ;
tR1 -tM
10
