
Поливанова А.Г._Высокоэффективная жидкостная хроматография БАВ
.pdf
- величина, характеризующая разделительную способность колонки по отношению к веществам 1 и 2 и численно равная отношению факторов удерживания или приведенных времён (объёмов) удерживания
α |
|
= |
k1' |
= |
t1' |
= |
V1' |
. |
|
k2' |
t2' |
|
|||||
|
1/2 |
|
|
V2' |
||||
Селективность колонки зависит от многих факторов, варьируя которые можно подобрать оптимальные условия хроматографии смеси компонентов интересующей экспериментатора. Исходя из химической природы разделяемых компонентов хроматографист должен выбрать подходящий состав растворителя (подвижную фазу) и соответствующий по химической природе сорбент. Определённое влияние на селективность имеют и такие термодинамические факторы, как температура и давление в колонке, изменяющие коэффициенты распределения веществ между подвижной и неподвижной фазами.
Коэффициент асимметрии, АS – отношение двух отрезков, образуемых на горизонтальной линии, проведенной на высоте, составляющей 10 % от основания пика, при её пересечении с вертикалью, опущенной из вершины пика (рис. 2). При этом берётся отношение "тыльного" отрезка к
"фронтальному". As= BA.
Разрешение пиков, RS – расстояние между максимумами выбранных соседних пиков, делённое на полусумму их ширины у основания (выраженных
в одних и тех же единицах измерения), Rs = 2 |
tR2 |
-tR1 |
. Разрешение как |
Wb1 |
|
||
|
+Wb2 |
||
параметр, характеризующий разделение пиков, увеличивается по мере возрастания селективности, отражаемой ростом числителя, и роста эффективности, отражаемой снижением значения знаменателя из-за уменьшения ширины пиков.
Экстраколоночное расширение пика (ЭКР) – размывание хроматографической зоны, происходящее в инжекторе, соединительных капиллярах и в ячейке детектора.
1.4. Общие принципы оптимизации хроматографического анализа
При выборе хроматографической системы (хроматографических условий анализа) для решения какой-либо конкретной задачи необходимо добиться достаточно высоких значений эффективности и селективности для выявления или разделения всех компонентов анализируемой смеси (рис. 3).
Хроматографические условия анализа включают: тип и марку используемого хроматографа, размеры хроматографической колонки и марку используемого в ней адсорбента, состав и расход (скорость подачи) элюента, тип элюирования, объём пробы, тип детектора и условия детектирования, температуру при которой проводится анализ.
Процесс улучшения методики разделения веществ, содержащихся в пробе, называется оптимизацией хроматографического анализа.
11
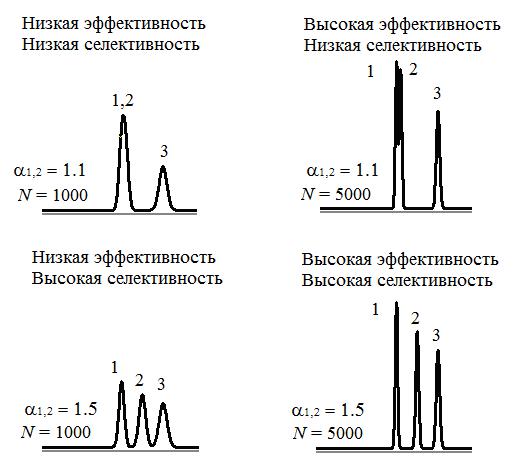
При рутинной работе на одном приборе смена колонки (адсорбента) производится редко. Для улучшения разделения анализируемой смеси в ЖХ, чаще всего, варьируют состав и соотношение компонентов подвижной фазы (элюента), а также режимы элюирования (изократическое или градиентное) (см. раздел 2.2.). Кроме того, подбирают температуру, при которой проводится хроматографический анализ (в зависимости от температурного рабочего диапазона адсорбента), и скорость потока элюента (предел скорости потока определяется предельным рабочим давлением хроматографа). Помимо оптимальных значений эффективности и селективности, важным моментом для оптимизации хроматографического метода анализа является сокращение его времени (объема элюента).
Рис. 3. Эффективность и селективность 1,2,3 – хроматографические пики компонентов разделяемой смеси
Повышение температуры в хроматографической системе даёт сразу три позитивных эффекта. Во первых, из-за ускорения массообмена достаточно сильно возрастает удельная эффективность неподвижной фазы. Во-вторых, опять же из-за ускорения массообмена потери эффективности при увеличении скорости потока сокращаются, т.е. можно ускорять разделение без риска сильно потерять в эффективности. В третьих, вязкость любой жидкости при повышении температуры становиться меньше, что приводит к уменьшению перепада давления в колонке. В результате запас по верхнему предельному
12

давлению в хроматографической системе увеличивается, т.е. можно дополнительно увеличивать скорость потока. Однако увеличивать температуру анализа можно не безгранично, поскольку все сорбенты имеют свой температурный предел.
Глава 2. Молекулярная адсорбционная хроматография
Жидкостная адсорбционная хроматография (ЖАХ) основана на конкурентном взаимодействии молекул вещества и молекул растворителя с активными центрами адсорбента на его поверхности. Поверхность адсорбента, находящегося в равновесии с подвижной фазой всегда покрыта более или менее прочно связанным адсорбционным слоем. Если подвижная фаза содержит два или более компонентов, то состав адсорбционного слоя отличается от состава в объёме подвижной фазы. Адсорбция молекулы сорбата может происходить с вытеснением одной или нескольких молекул адсорбированного слоя или без него.
Рис. 4. Взаимодействия молекул на поверхности адсорбента
Процессы взаимодействия молекул адсорбата с адсорбционными слоями и поверхностью твердого адсорбента весьма сложны, главную роль в них играют ион-дипольные и диполь-дипольные взаимодействия. Селективность разделения в ЖАХ определяется не только межмолекулярным взаимодействием молекул данного адсорбата, но и межмолекулярными взаимодействиями молекул подвижной фазы с адсорбентом и с молекулами адсорбата, находящимися как на поверхности адсорбента, так и в адсорбционном слое и в объёме элюента.
Взависимости от природы элюента и неподвижной фазы (обычно силикагель) различают нормально-фазовую (НФЖХ) и обращённо-фазовую (ОФЖХ) жидкостную хроматографию.
2.1.Нормально-фазовая и обращёно-фазовая жидкостная хроматография
Внормально-фазовой жидкостной хроматографии (НФЖХ) адсорбент – полярный, а элюент – неполярный (например, гексан, хлороформ, либо их
13

смеси с более полярными органическими растворителями – спиртами, сложными эфирами и т.д.). Понятие «полярный» подразумевает наличие у адсорбента поверхностных групп, имеющих постоянный дипольный момент, или существование постоянного некомпенсированного поверхностного заряда. В настоящее время наиболее распространённым полярным адсорбентом является силикагель – гель ортокремневой кислоты. Силикагель имеет формулу mSiO×nH2O. Частички силикагеля представляют собой неорганический полимер с силанольными (≡Si-ОН) и силоксановыми (≡Si-О-Si≡) группами на поверхности (рис. 5). Силанольные группы имеют дипольный момент и могут образовывать водородные связи. У поверхности силикагеля, кроме полярных групп, существует также постоянный некомпенсированный поверхностный заряд.
Рис. 5. Поверхность немодифицированного силикагеля
Силикагель обладает рядом уникальных свойств, совокупность которых позволяет успешно использовать его в ВЭЖХ:
- жёсткая механическая матрица силикагеля позволяет очень плотно заполнять колонки суспензионным способом при давлении до 100 МПа без разрушения силикагеля; та же матрица позволяет использовать высокие давления при работе с силикагельными колонками;
- силикагель достаточно химически инертен, устойчив в диапазоне рН 2.0 – 8.5;
-он обладает развитой, до нескольких квадратных метров на грамм, регулируемой в процессе синтеза удельной поверхностью;
-возможно получение силикагеля с частичками, имеющими как регулярную, так и не регулярную формы.
ГЕКСАН |
ВОДА |
Адсорбция молекул вещества происходит в основном за счёт образования водородных связей с полярными группами на поверхности силикагеля
H
Si O
H
O
Рис. 6. Нормально-фазовая ЖХ
14
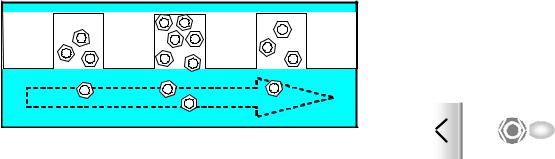
Удерживание веществ в НФЖХ растёт с увеличением их полярности. Разделения компонентов достигают, меняя элюирующую силу подвижной фазы (см. раздел 2.2.), которая зависит от энергии взаимодействия компонентов подвижной фазы с поверхностью неподвижной фазы. В нормально-фазовой хроматографии элюирующая способность подвижной фазы увеличивается с ростом её полярности.
В обращёно-фазовой жидкостной хроматографии (ОФЖХ) адсорбент – неполярный (гидрофобные силикагели с химически «пришитыми» к их поверхности углеводородными радикалами или химически привитые фазы), элюент – полярный (смеси воды и полярных растворителей: ацетонитрила, метанола, тетрагидрофурана и др.).
Удерживание веществ в ОФЖХ растет с увеличением их гидрофобности (неполярности). Наименьшей элюирующей силой обладает вода, а для повышения элюирующей силы в элюенте увеличивают содержание ацетонитрила или других растворителей. Чем больше содержание органического растворителя, тем выше элюирующая способность подвижной фазы.
ГЕКСАН |
ВОДА |
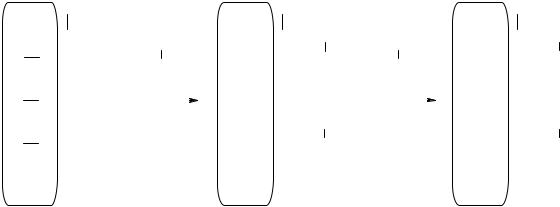
Адсорбция молекул вещества происходит в основном за счёт гидрофобных взаимодействий с неполярными группами на поверхности модифицированного силикагеля
 Si
Si
OH
 Si
Si
Рис. 7. Обращёно-фазовая ЖХ
Преимущества обращёно-фазовой ЖХ
Использование химически модифицированных (привитых) силикагелей в качестве неподвижной фазы значительно расширяет возможности ВЭЖХ и даёт ей целый ряд преимуществ перед другими вариантами жидкостной хроматографии:
–это очень гибкий метод, так как изменяя состав водно-органических смесей, используемых в качестве подвижной фазы, можно на одной колонке обеспечить разделение соединений различной природы (как растворимых в воде, так и в органических растворителях);
–селективность данного метода почти всегда значительно выше, чем у других вариантов хроматографии для всех соединений, кроме сильнополярных;
–при использовании гидрофобизированных силикагелей быстро устанавливается равновесие между подвижной и неподвижной фазами, эти адсорбенты отличаются высокой эффективностью разделения;
–возможность использования в подвижной фазе буферных растворов может улучшить селективность и эффективность разделения ионогенных соединений.
15
В настоящее время более 90 % всех анализов методом ВЭЖХ выполняют на химически привитых фазах, главным образом, с привитыми алкильными группами.
Неподвижные фазы для обращёно-фазовой ЖХ
Обращённые фазы могут отличаться друг от друга характеристиками матрицы – силикагеля и строением привитого радикала. К основным характеристикам силикагеля относятся: размер зерна (обычно от 3 до 10 мкм), форма зерна (сферическая или неправильная), размер пор зерна (от 5 до 50 нм), удельная поверхность (от 10 до 600 м2/г). Гирдофобизированные силикагели чаще всего получают при обработке силикагеля хлорсиланом (рис. 8). Названия таких адсорбентов С8, С16, С18 соответствуют привитым на силикагеле углеводородным цепочкам длиной 8,16, 18 углеродных атомов соответственно.
|
|
|
|
O |
|
|
|
|
|
CH3 |
|
|
|
|
|
O |
|
|
|
|
|
|
CH3 |
|
|
CH3 |
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
CH3 |
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
O |
|
Si |
|
OH Cl |
|
|
|
O |
|
Si |
|
O |
|
|
Si |
|
|
R Cl |
|
|
|
|
O |
|
|
Si |
|
|
O |
|
|
|
Si |
|
|
R |
||||||||||||||||||||||||||||||||||
|
|
|
Si |
|
R |
|
|
|
|
|
|
|
Si |
|
CH |
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
CH3 |
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
O |
|
|
Si |
|
|
OH |
|
|
|
O |
|
|
Si |
|
|
OH |
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
Si |
|
|
|
O |
|
|
|
|
Si(CH3)3 |
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- HCl |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
- HCl |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
O |
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
CH3 |
||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
O |
|
|
|
|
|
|
|
|
OH |
|
|
|
O |
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
Si |
|
|
|
|
|
|
|
Si |
|
|
|
|
Si |
|
|
|
R |
|
|
|
|
|
|
|
|
|
O |
|
|
|
Si |
|
|
|
O |
|
|
|
|
|
Si |
|
|
|
R |
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
CH3 |
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Присоединение функциональной группы R |
Инактивация оставшихся свободных |
|
R = C8H17 , C16H31 , C18H35 |
и др. |
силанольных групп ("endcapping") |
Рис. 8. Синтез привитых мономерных фаз |
||
Наибольшее распространение получила обращенная фаза с привитыми |
||
октадециловыми группами – |
С18. Её |
используют для разделения как |
неполярных (например, ароматических углеводородов), так и полярных (водорастворимых) соединений. Самая распространённая основа элюента для работы на таких неподвижных фазах – вода или водно-солевой буфер; в качестве добавки часто применяют ацетонитрил или метанол, реже тетрагидрофуран или изопропиловый спирт.
В зависимости от способа обработки свойства гидрофобизированных силикагелей могут изменяться, поэтому свойства коммерческих колонок
различных |
фирм несколько отличаются. Содержание углерода составляет |
5 – 20 %. |
Степень покрытия поверхности силикагеля органическим |
модификатором составляет 10 – 60 %, в лучших случаях она достигает 90 %. Наличие остаточных силанольных групп приводит к тому, что адсорбционный и ионообменный механизмы удерживания не всегда сопутствуют обращённофазовому варианту хроматографии. Для уменьшения числа силанольных групп адсорбенты дополнительно обрабатывают триметилхлорсиланом (эндкеппинг –
«endcapping») (рис. 8).
16
В табл. 1 представлены типичные обращённо-фазовые сорбенты.
Таблица 1
Привитые фазы на основе силикагеля
|
|
|
|
|
|
O |
|
|
CH3 |
|||||
|
|
|
|
O |
|
|
|
|
|
|||||
|
|
|
|
|
Si |
|
O |
|
Si |
|
R |
|||
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
O |
|
|
CH3 |
|||||
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Условные |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
обозначения |
R |
|
|
|
|
|
|
|
|
|
|
Назначение |
||
фазы |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
С18, RP18, |
|
|
|
|
Универсальная фаза с высокой ёмкостью. |
|||||||||
|
|
|
|
Возможно разделение гидрофильных |
||||||||||
октадецил I, |
-CH2(CH2)16CH3 |
|
|
|||||||||||
|
веществ методом ион-парной |
|||||||||||||
ODS |
|
|
|
|
||||||||||
|
|
|
|
хроматографии |
||||||||||
|
|
|
|
|
||||||||||
|
|
|
|
|
Универсальная фаза со средней ёмкостью. |
|||||||||
C8, RP8, |
-CH2(CH2)6CH3 |
|
|
Возможно разделение липофильных |
||||||||||
октил |
|
веществ методом обращённо-фазовой |
||||||||||||
|
|
|
|
|||||||||||
|
|
|
|
|
хроматографии |
|||||||||
С4, бутил |
-CH2(CH2)2CH3 |
|
|
Разделение белков и пептидов методом |
||||||||||
|
обращённо-фазовой и гидрофобной |
|||||||||||||
|
|
|
|
|
хроматографии |
|||||||||
С1 |
-CH3 |
|
Фаза с очень низкой ёмкостью |
|||||||||||
Фенил |
-C6H5 |
|
Фаза со средней ёмкостью |
|||||||||||
Нитрил, CN |
-CH2CH2CH2CN |
|
Фаза с низкой ёмкостью |
|||||||||||
Нитро, NO2 |
-CH2CH2CH2NO2 |
|
|
Фаза с низкой ёмкостью; селективна к |
||||||||||
|
ароматическим соединениям |
|||||||||||||
|
|
|
|
|
||||||||||
Недостатками классических обращённо-фазовых сорбентов на основе силикагеля являются узкий рабочий диапазон рН и сорбционная активность остаточных силанольных групп. Этих недостатков в значительной степени лишены, к примеру, сорбенты С18 нового поколения фирмы «Феноминекс», которые обладают стабильностью в диапазоне значений рН 1.5 – 10.
Способ получения таких адсорбентов заключается в введении С18 и С8 радикалов не в виде монохлорида кремния (Cl–Si(CH3)2–R), а в виде дихлорида (Cl2–Si(CH3)–R) или трихлорида кремния (Cl3–Si–R). В данном случае концевые атомы хлора могут гидролизваться и вступать в реакцию полимеризации. В результате получается полимерная С18 или С8 «прививка» (рис. 9).
Полимерный слой адсорбента С18 «закрывает» силикагель и способствует значительному замедлению процесса гидролиза (растворения адсорбента), что значительно продлевает срок эксплуатации колонки, даже при работе с элюентами имеющими сильнокислый рН 1.5 – 3.
Другим ограничением для неподвижных фаз на основе силикагеля является низкий температурный предел для проведения анализа, равный 50 °С. Реально
17
предпочитают проводить анализ на таких адсорбентах при 40 °С.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Cl |
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Cl |
|
|
|
|
|
|
|
|
|
|
|
R |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Cl |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Si |
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
O |
|
|
||||||||||||||||||||||||
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
Si |
|
|
OH |
|
O |
|
Si |
|
O |
|
|
Si |
|
|
|
R |
|
O |
|
Si |
|
|
O |
|
|
Si |
|
|
R |
|
O |
|
Si |
|
O |
|
|
|
Si |
|
|
|
R |
|||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
Cl |
|
|
|
|
+ H2O |
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
O |
|
R |
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
SiCl R |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
SiCl R |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
Si |
|
|
OH |
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
O |
|
|
Si |
|
OH |
|
|
|
|
|
|
O |
|
|
Si |
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
Si |
|
|
OH Si |
|
Cl |
|||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
- HCl |
|
|
|
|
|
|
|
|
|
|
|
- HCl |
|
|
|
|
|
|
|
|
|
|
|
|
- HCl |
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
O |
|
|
|
|
|
|
|
O |
|
|
|
|
|
Cl |
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
OH |
|
|
|
|
|
O |
|
|
|
|
|
|
|
O |
|
||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
O |
|
|
|
|
|
|
|
|
OH |
|
|
O |
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
Si |
|
|
|
|
|
|
|
|
Si |
|
|
|
|
Si |
|
|
|
R |
|
|
O |
|
|
Si |
|
|
|
O |
|
|
Si |
|
|
|
R |
|
|
O |
|
|
Si |
|
|
O |
|
|
|
|
Si |
|
|
|
|
|
R |
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
Cl |
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
O |
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Cl |
|
|
|
|
|
|
|
|
|
|
|
R |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Si |
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Cl |
|
|
||||||
R = C8H17 , C18H35
Рис. 9. Синтез привитых полимерных фаз
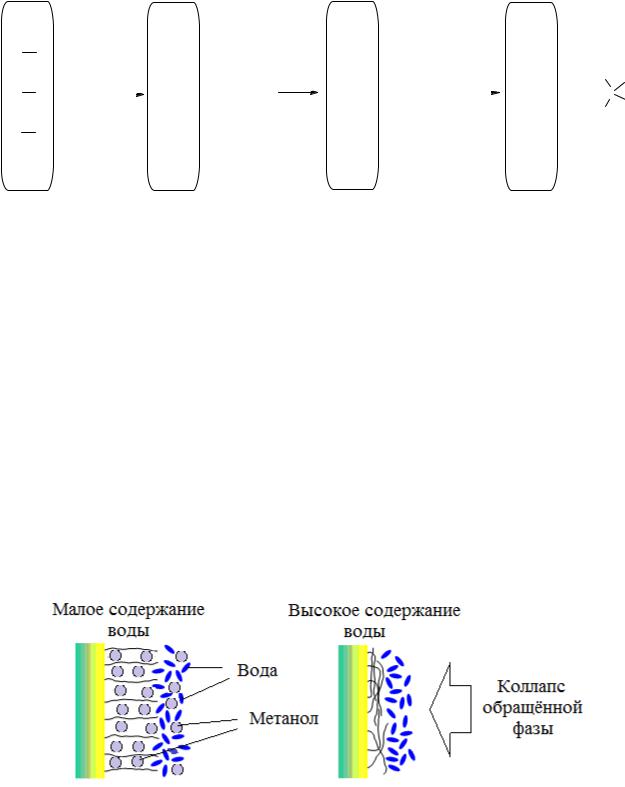
При работе на обращёно-фазовых адсорбентах низкого качества с элюентами, содержащими 90 % и более водной основы, может возникнуть крайне неприятный эффект фазового коллапса (коллапс обращённой фазы).
Этот процесс выражается в том, что в течение небольшого времени (порядка нескольких часов) поначалу «отличная хроматограмма» начинает «плыть» – удерживание всех компонентов резко падает, и соответственно ухудшается эффективность колонки. Все вещества на хроматограмме выходят в виде одного широкого пика с низким временем удерживания. Если промыть колонку органическим элюентом, а затем вновь повторить анализ, то «нормальное» разделение снова будет наблюдаться, но не очень длительное время.
Причина возникновения эффекта фазового коллапса заключается в том, что неполярная поверхность С18 фазы перестаёт смачиваться элюентом, обедненным органическим растворителем, и он просто перестает проникать в поры адсорбента (рис. 10). Соответственно, поры перестают работать, что приводит к резкому уменьшению времени удерживания разделяемых веществ.
Рис. 10. Коллапс обращённой фазы
Для того, чтобы эффекта фазового коллапса не возникало, неполярный адсорбент всё-таки должен содержать какое-то минимальное количество полярных групп, что обеспечивается различными специфическими подходами к синтезу обращёно-фазовых адсорбентов.
18
Механизм разделения в обращёно-фазовой ЖХ
Наиболее удачной и распространенной теорией, объясняющей процессы, происходящие при обращёно-фазовом варианте ЖХ, является сольвофобная теория Хорвата – Меландера. Суть этой теории заключается в следующем. Существует принципиальное различие между процессами сорбции на полярных поверхностях из относительно неполярных растворителей (НФЖХ) и сорбции из воды либо сильнополярных растворителей на неполярных поверхностях (ОФЖХ). В первом случае между молекулами сорбатов и неподвижных фаз образуются ассоциаты за счёт кулоновских взаимодействий или водородных связей. Во втором случае причиной ассоциации на поверхности являются так называемые сольвофобные взаимодействия в подвижной фазе. Для полярных подвижных фаз, в особенности содержащих воду, характерно сильное кулоновское взаимодействие и образование водородных связей между молекулами растворителей. Все молекулы в таких растворителях связаны довольно прочно межмолекулярными силами. Для того чтобы поместить в эту среду молекулу сорбата, необходимо образование «полости» между молекулами растворителя. Энергетические затраты на образование такой «полости» лишь частично покрываются за счёт взаимодействия полярных групп в молекуле сорбата с полярными молекулами растворителя. В аналогичном положении по отношению к растворителю находятся и неполярные молекулы неподвижной фазы. С энергетической точки зрения более выгодно такое положение, когда поверхность раздела между полярной средой (растворителем), неполярными фрагментами неподвижной фазы и молекулами сорбата минимальна. Уменьшение поверхности раздела и достигается при сорбции.
В целом же можно заключить, что в ОФ ЖХ разделение смеси веществ происходит в результате различия в коэффициентах распределения веществ между подвижной и неподвижной фазами по распределительному механизму. Удерживание веществ на поверхности неподвижной фазы в ОФ ЖХ в основном определяется гидрофобными взаимодействиями.
2.2. Подвижные фазы для обращено-фазовой высокоэффективной жидкостной хроматографии
Выбор элюента, как правило, в более значительной степени влияет на разделение, чем выбор неподвижной фазы. Следует отметить, что выбор элюента и оптимизация условий разделения – задача достаточно сложная.
При выборе элюента в первую очередь следуют правилу: «подвижная фаза, прежде всего, должна растворять разделяемые компоненты!».
Для оптимизации состава 2-х и более компонентного элюента существуют различные способы, как для изократического, так и для градиентного элюирования.
Изократическое элюирование – это использование элюента постоянного состава в течение всего хроматографического анализа. Достоинством такого элюирования является техническая простота исполнения и высокая
19
воспроизводимость времён удерживания, площадей и высот пиков хроматограмм.
Градиентное элюирование предполагает увеличение по определённому закону элюирующей силы элюента в процессе одного анализа. Например, для ОФ ЖХ – это увеличение содержания ацетонитрила в элюенте по ходу анализа, если элюент – смесь воды и ацетонитрила. Градиентное элюирование является одним из наиболее эффективных способов повышения качества разделения смесей.
Основными характеристиками подвижной фазы является элюирующая способность (элюирующая сила) и селективность.
Элюирующая сила (ЭС) элюента – это способность элюента вытеснять адсорбат с поверхности адсорбента. Считается, что чем прочнее элюент адсорбируется на адсорбенте, тем выше его элюирующая сила. ЭС подвижной фазы определяется способностью вступать в межмолекулярные взаимодействия с разделяемыми соединениями и группами на поверхности адсорбента. Эти взаимодействия способствуют десорбции разделяемых соединений, более быстрому перемещению хроматографических зон. Многократное увеличение гибкости метода в ВЭЖХ достигается за счёт применения в качестве элюента смесей растворителей. Принцип составления таких смесей прост. Необходимо взять два индивидуальных растворителя, один из которых имеет заведомо недостаточную элюирующую силу, а другой – заведомо избыточную, варьируя соотношение этих растворителей, можно получить нужную элюирующую способность. Под этим обычно имеют в виду, что на данном адсорбенте данный адсорбат будет иметь приемлемое значение фактора удерживания (Rf).
Расположенные в ряд по возрастанию элюирующей силы растворители образуют так называемый элюотропный ряд. Элюотропные ряды являются простейшей формой оценки силы индивидуальных растворителей. Они дают количественную оценку элюирующей способности растворителей в тех или иных вариантах хроматографического разделения. При составлении элюотропного ряда элюирующая способность может быть охарактеризована различными параметрами, такими как:
-диэлектрическая проницаемость растворителя εr, определяющая его способность к разделению зарядов и ориентации собственных диполей; иными словами величина диэлектрической проницаемости определяет диссоциирующую способность жидкости, т.е. способность растворять электролиты путём их разделения на ионы;
-параметр адсорбционной силы растворителя ε0, который представляет собой относительную энергию взаимодействия молекул подвижной фазы с поверхностью адсорбента;
-параметр полярности растворителя Р (параметр Снайдера или полярность по Снайдеру), который рассчитывают как сумму логарифмов коэффициентов распределения стандартных веществ (этанола, диоксана и нитрометана) между паровой фазой и испытуемым растворителем;
20
