
- •Методи дослідження доброякісності лікарських речовин.
- •2.1 Хімічні кількісні методи аналізу лікарських речовин
- •2.1.1 Гравіметричний Аналіз
- •2.1.2 Титрометричні методи аналізу
- •2.1.3 Методи осадження. Аргентометрія
- •Комплекосонометрія
- •Кислотно-основне титрування
- •Методи окислення-відновлення
- •2.2 Фізичні і фізико-хімічні методи дослідження лікарськіх засобів
- •2.2.4 Спектроскопія комбінаційного розсіювання світла
- •2.2.7 Рентгеноструктурний та рентгеноспектральний аналіз
- •2.2.8 Термогравіметричний аналіз
- •2.2.9 Рефрактометрія
- •2.2.10 Поляриметрія
- •Методи визначення чистоти лікарських речовин
- •2.3.1 Визначення каламутності та забарвленості
- •2.3.2 Визначення кислотності, лужності та рН середовища
- •2.3.3 Випробування на граничних вміст домішок
- •3. Хроматографія
- •3.1 Історія
- •3.2 Класифікація хроматографічних методів
- •3.3 Найрозповсюдженіші техніки хроматографії
- •3.3.1 Тонкошарова хроматографія
- •3.3.2 Високоефективна рідинна хроматографія (верх).
- •3.3.3 Адсорбційна хроматографія
- •3.3.4 Афінна хроматографія
- •3.3.5 Ексклюзійна хроматографія
- •Висновки:
2.3.2 Визначення кислотності, лужності та рН середовища
Невідповідність лікарської речовини за цими показниками може бути наслідком присутності домішок більш кислотного або основного характеру, ніж сама речовина.
Подібні домішки можуть утворюватися при добуванні або зберіганні лікарських засобів( домішки мінеральних кислот, продуктів гідролізу, вплив лужності скла, поглинання речовиною вуглекислого газу з повітря).
Контроль кислотності, лужності, рН середовища регламентується відповідним розділом монографій та може здійснюватися різними способами:
за зміною забарвлення кислотно- основних індикаторів (рН індикаторів)
визначенням величини рН за методом, наведеним у загальній фармакопейній статті «Визначення рН». Таке визначення є обовязковим для всіх ін’єкційних розчинів;
кислотно-основним титруванням.
2.3.3 Випробування на граничних вміст домішок
Державна фармакопея не вимагає абсолютної чистоти лікарського засобу і не допускає в ньому певні домішки в сурово визначених межах. У фармакопейному аналізі існують два методи визначення вмісту домішок:
Наприклад:
Дослідження на солі амонію – залежно від властивостей лікарської речовини та допустимої домішки солей амонію її визначення проводиться за одним із чотирьох методів.
Метод А грунтується на здатності солей амонію утворювати солі амонію з розчином калію тетрайодомеркурату лужного( Реактив Несслера) жовто-бурий осад або жовте забарвлення залежно від концентрації.
NH4+ + 2[HgI4]2‾ + 2OH‾ → [NH2Hg2I2]+I‾ + 5I‾ + 2H2O.
Виявлення домішки кальцію
При приготуванні всіх розчинів, застосовуваних у даному випробуванні, має використовуватися вода дистильована Р.
До 0.2 мл еталонного розчину кальцію спиртового (100 ppm Ca) Р додають 1 мл розчину амонію оксалату Р. Через 1 хв. додають суміш 1 мл кислоти оцтової розведеної Р і 15 мл розчину, що містить зазначену в окремій статті кількість випробовуваної речовини, і струшують.
Паралельно за цих самих умов готують еталон, використовуючи суміш 1 мл кислоти оцтової розведеної Р, 10 мл еталонного розчину кальцію водного (10 ppm Ca) Р і 5 мл води дистильованої Р.
Через 15 хв. опалесценція випробовуваного розчину не має перевищувати опалесценцію еталона.
Ca2+ + C2O42– → CaC2O4↓.
Виявлення домішки хлоридів
До 15 мл розчину, зазначеного в окремій статті, додають 1 мл кислоти азотної розведеної Р і виливають суміш за один раз у пробірку, що містить 1 мл розчину срібла нітрату Р2.
Паралельно за цих самих умов готують еталон, використовуючи замість 15 мл випробовуваного розчину 10 мл еталонного розчину хлориду (5 ppm Cl) Р і 5 мл води Р. Пробірки поміщають у захищене від світла місце.
Через 5 хв. пробірки переглядають на чорному фоні горизонтально (перпендикулярно до осі пробірок). Опалесценція випробовуваного розчину не має перевищувати опалесценцію еталона.
Cl‾ + Ag+ → AgCl↓.
Виявлення домішки важких металів (метод А)
До 12 мл водного розчину, зазначеного в окремій статті, додають 2 мл буферного розчину рН 3.5 Р і перемішують. Одержану суміш додають до 1.2 мл реактиву тіоацетаміду Р і негайно перемішують.
Паралельно за тих самих умов готують еталон, використовуючи замість 12 мл випробовуваного розчину суміш 10 мл еталонного розчину свинцю (1 ppm або 2 ppm Pb) Р, як зазначено в окремій статті, і 2 мл випробовуваного розчину.
Готують „сліпу” пробу, використовуючи суміш 10 мл води Р і 2 мл випробовуваного розчину. Порівняно із „сліпою” пробою еталон повинен мати світло-коричневе забарвлення.
Через 2 хв. коричневе забарвлення випробовуваного розчину має бути не інтенсивнішим за забарвлення еталона.
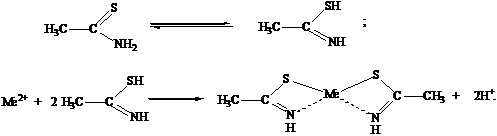
Інший можливий хімізм:
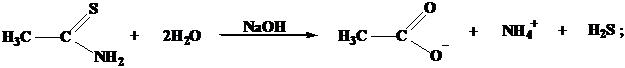
H2S → HS– + H+ → S2– + 2H+;
Pb2+ + S2– → PbS↓.
Виявлення домішки заліза
Кількість випробовуваної речовини, зазначену в окремій статті, розчиняють у воді Р, доводять об’єм розчину водою Р до 10 мл і перемішують або використовують 10 мл розчину, зазначеного в окремій статті. Додають 2 мл розчину 200 г/л кислоти лимонної Р і 0.1 мл кислоти тіогліколевої Р. Перемішують, підлужують розчином аміаку Р, доводять об’єм розчину водою Р до 20 мл.
Паралельно за цих самих умов готують еталон, використовуючи 10 мл еталонного розчину заліза (III) (1 ppm Fe) Р.
Через 5 хв. рожеве забарвлення випробовуваного розчину має бути не інтенсивнішим за забарвлення еталона.
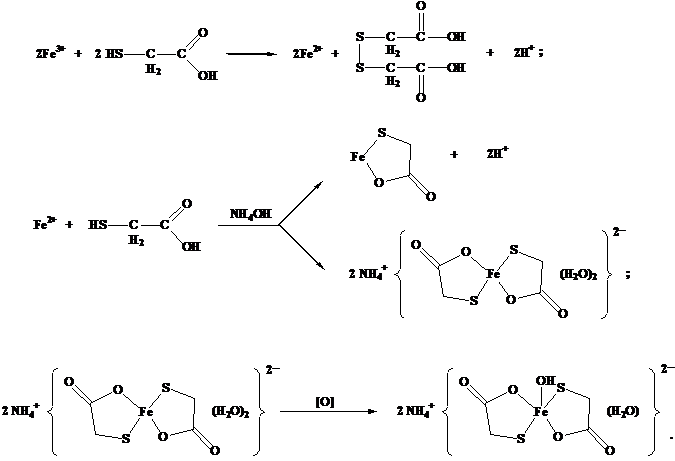
Виявлення домішки сульфатів
При приготуванні усіх розчинів, застосовуваних у даному випробуванні, має використовуватися вода дистильована Р.
До 1.5 мл еталонного розчину сульфату (10 ppm SO4) Р1 додають 1 мл розчину 250 г/л барію хлориду Р. Струшують і залишають на 1 хв., потім додають 15 мл випробовуваного розчину, приготованого, як зазначено в окремій статті, і 0.5 мл кислоти оцтової Р.
Паралельно за цих самих умов готують еталон, використовуючи замість випробовуваного розчину 15 мл еталонного розчину сульфату (10 ppm SO4) Р.
Через 5 хв. опалесценція випробовуваного розчину не має перевищувати опалесценцію еталона.
Ba2+ + SO42‾ → BaSO4↓.
Виявлення домішки цинку
До 10.0 мл розчину випробовуваної речовини, приготованого, як зазначено в окремій статті, додають 2.0 мл розчину кислоти хлористоводневої Р1 і 0.2 мл розчину калію фероціаніду Р.
Паралельно готують еталон з використанням замість випробовуваного розчину 10 мл еталонного розчину цинк-йона (5 ppm Zn), який готують шляхом розведення водою Р у 1000 разів еталонного розчину цинку (5 мг/мл Zn) Р.
Через 10 хв. опалесценція випробовуваного розчину не має перевищувати опалесценцію еталона.
3Zn2+ + 2K+ + 2[Fe(CN)6]4‾ → K2Zn3[Fe(CN)6]2↓.
