
- •Законы Ньютона
- •II закон Ньютона
- •III закон Ньютона
- •4. Закон сохранения импульса Закон сохранения импульса.
- •5.Закон сохранения механической энергии
- •7.Момент инерции. Основной закон динамики вращательного движения
- •9.Уравнение состояния идеального газа. Изопроцессы
- •10.Первое начало термодинамики
- •11.Тепловой двигатель. Цикл Карно
- •12.Второе начало термодинамики
- •13.Энтропия и вероятность
- •14.Закон Кулона. Напряженность
- •15.Потенциал. Электрический диполь
- •Потенциал
- •17.Энергия электрического поля. Закон Джоуля – Ленца
- •18.Диэлектрики. Конденсаторы
- •19.Магнитная индукция. Закон Био-Савара
- •20.Сила Ампера. Сила Лоренца
- •21.Классификация веществ по магнетическим свойствам
- •22.Закон электромагнитной индукции. Правило Ленца
- •23.Интерференция
- •24.Дифракция
- •25.Поляризация света
7.Момент инерции. Основной закон динамики вращательного движения
Моментом инерции материальной точки относительно оси вращения называется произведение массы материальной точки на квадрат ее расстояния до этой оси.
Моментом
инерции тела называется сумма моментов
инерции всех материальных точек тела
![]()
![]()
Основной закон динамики вращения (II закон Ньютона для вращательного движения):
Момент вращающей силы, приложенной к телу, равен произведению момента инерции тела на угловое ускорение.
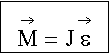
Момент инерции тела характеризует инерционные свойства тела при вращательном движении подобно массе, характеризующей инерционные свойства тела при поступательном движении. Момент инерции тела имеет множество значений, в зависимости от оси вращения.
Если вращающий момент M = const постоянен и момент инерции J = const, то основной закон вращения можно представить в виде
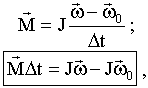
M Δt - импульс момента силы, Jω-момент импульса тела .
8. Основное положение МКТ
Молекулярно-кинетической теорией называют учение о строении и свойствах вещества на основе представления о существовании атомов и молекул как наименьших частиц химических веществ.
В основе молекулярно-кинетической теории лежат три основных положения:
Все вещества – жидкие, твердые и газообразные – образованы из мельчайших частиц – молекул, которые сами состоят из атомов («элементарных молекул»). Молекулы химического вещества могут быть простыми и сложными, т.е. состоять из одного или нескольких атомов. Молекулы и атомы представляют собой электрически нейтральные частицы. При определенных условиях молекулы и атомы могут приобретать дополнительный электрический заряд и превращаться в положительные или отрицательные ионы.
Атомы и молекулы находятся в непрерывном хаотическом движении.
Частицы взаимодействуют друг с другом силами, имеющими электрическую природу. Гравитационное взаимодействие между частицами пренебрежимо мало.
9.Уравнение состояния идеального газа. Изопроцессы
Соотношение
![]()
Уравнение Менделеева-Клайперона
называется уравнением состояния идеального газа.
Уравнение, устанавливающее связь между давлением, объемом и температурой газа было получено в середине XIX века французским физиком Б. Клапейроном, в форме (*) оно было впервые записано Д. И. Менделеевым. Поэтому уравнение состояния газа называется уравнением Клапейрона–Менделеева.
Следует отметить, что задолго до того, как уравнение состояния идеального газа было теоретически получено на основе молекулярно-кинетической модели, закономерности поведения газов в различных условиях были хорошо изучены экспериментально. Поэтому уравнение (*) можно рассматривать как обобщение опытных фактов, которые находят объяснение в молекулярно-кинетической теории.
Газ может участвовать в различных тепловых процессах, при которых могут изменяться все параметры, описывающие его состояние (p, V и T). Если процесс протекает достаточно медленно, то в любой момент система близка к своему равновесному состоянию. Такие процессы называются квазистатическими. В привычном для нас масштабе времени эти процессы могут протекать и не очень медленно. Например, разрежения и сжатия газа в звуковой волне, происходящие сотни раз в секунду, можно рассматривать как квазистатический процесс. Квазистатические процессы могут быть изображены на диаграмме состояний (например, в координатах p, V) в виде некоторой траектории, каждая точка которой представляет равновесное состояние.
Интерес представляют процессы, в которых один из параметров (p, V или T) остается неизменным. Такие процессы называются изопроцессами.
Изотермический процесс (T = const)
pV = const;
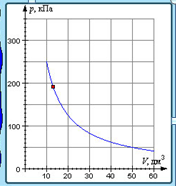
график изотермы. T3 > T2 > T1
Коэффициент пропорциональности в этом соотношении увеличивается с ростом температуры, изотермы, соответствующие более высоким значениям температуры. ). Уравнение изотермического процесса было получено из эксперимента английским физиком Р. Бойлем (1662 г.) и независимо французским физиком Э. Мариоттом (1676 г.). Поэтому это уравнение называют законом Бойля–Мариотта.
Изохорный процесс (V = const)
Изохорный процесс – это процесс нагревания или охлаждения газа при постоянном объеме V и при условии, что количество вещества ν в сосуде остается неизменным.
![]()

График изохоты. V3 > V2 > V1
Экспериментально зависимость давления газа от температуры исследовал французский физик Ж. Шарль (1787 г.). Поэтому уравнение изохорного процесса называется законом Шарля.
Изобарный процесс (p = const)
Изобарным процессом называют квазистатический процесс, протекающий при неизменным давлении p. Уравнение изобарного процесса для некоторого неизменного количества вещества ν имеет вид:
![]()
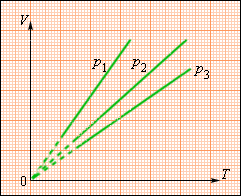
График изобары. p3 > p2 > p1
Зависимость объема газа от температуры при неизменном давлении была экспериментально исследована французским физиком Ж. Гей-Люссаком (1862 г.). Поэтому уравнение изобарного процесса называют законом Гей-Люссака.
