
Идиопатический легочный фиброз
.pdf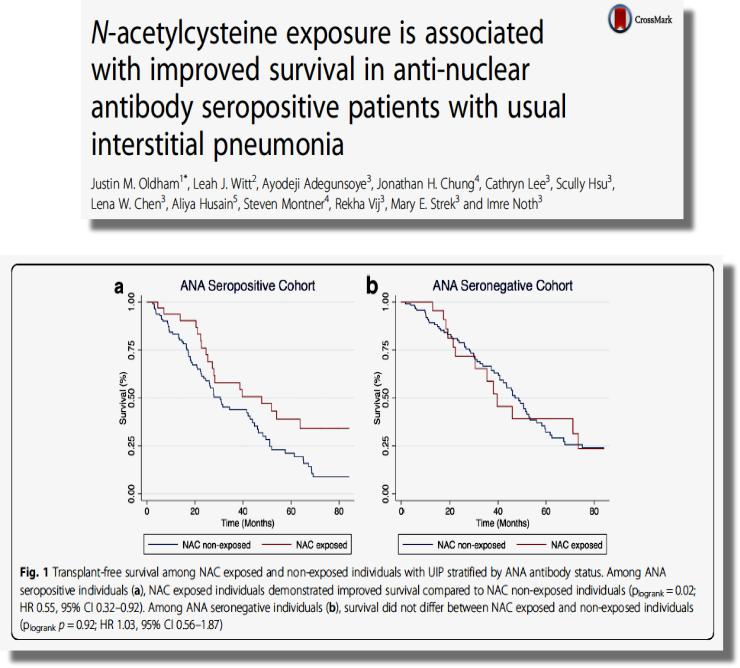
Oldham et al. BMC Pulmonary Medicine (2018) 18: 30
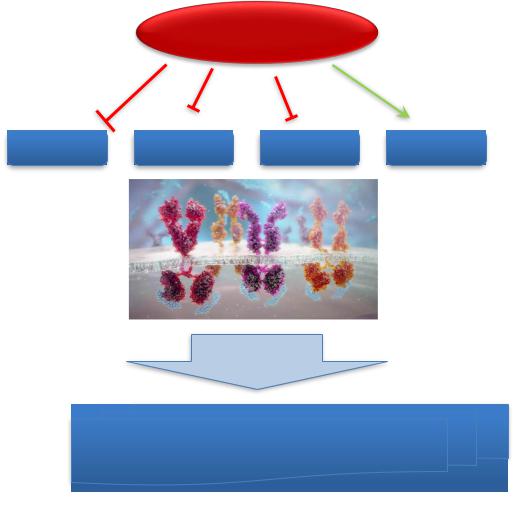
Возможные механизмы действия нинтеданиба
• Внутриклеточный ингибитор тирозин |
|
Нинтеданиб |
|
|
киназ |
|
|
||
|
|
|
|
|
• Мишень – рецепторы FGF, PDGF, VEGF |
|
|
|
|
• Конкурентно связывается с АТФ- |
VEGF |
PDGF |
FGF |
SHP-1 |
|
||||
участками рецепторов и блокирует внутриклеточные сигнальные пути
•Антиангиогенная, противоопухолевая активность
Антифибротические
эффекты
Hilberg F, et al. Cancer Res. 2008;68(12):4774-4782. Tai WT, et al. J Hepatol. 2014;61(1):89-97.
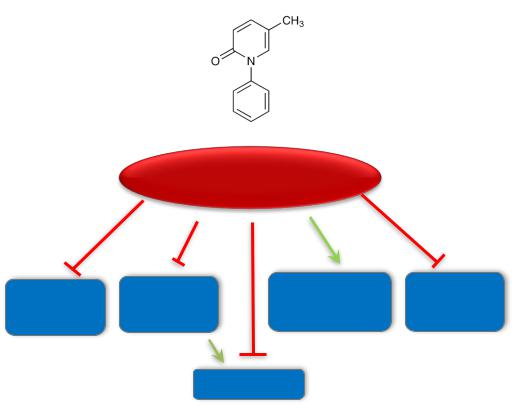
Возможные механизмы действия пирфенидона
•Антифибротические эффекты
•Молекулярная мишень не известна
• Активен в нескольких моделях |
Пирфенидон |
|
|
фиброза у животных (легких, |
|
|
|
печени, почек) |
|
|
|
TNF-α |
TGF-β |
MMPs |
ROIs |
коллагеназы |
|||
коллаген
Hilberg O, et al. Clin Respir J. 2012; 6: 131-143.
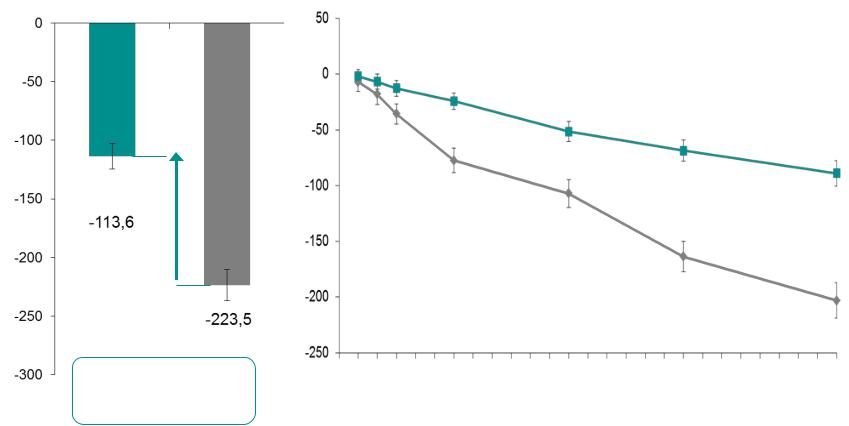
INPULSIS: ежегодная скорость снижения FVC
Ежегодное снижение (SE) FVC с поправкой (мл/год)
109.9 мл/год
(95% ДИ: 75.9, 144.0) p<0.0001
FVC |
|
|
|
|
|
|
Нинтеданиб 150 мг 2 р/с |
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
Плацебо |
|
|
Среднее (SE) изменение от исходного уровня |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0 |
2 |
4 |
6 |
12 |
24 |
36 |
52 |
|
|
|
|
|
|
Week |
|
|
|
No. of patients
 Нинтеданиб 150 мг 2 р/с (n=638)
Нинтеданиб 150 мг 2 р/с (n=638)  Плацебо (n=423)
Плацебо (n=423)
Nintedanib |
626 |
616 |
613 |
604 |
587 |
569 |
519 |
|
|||||||
Placebo |
417 |
408 |
407 |
403 |
395 |
383 |
345 |
|
Richeldi L, et al. NEJM 2014; 370: 2071-82
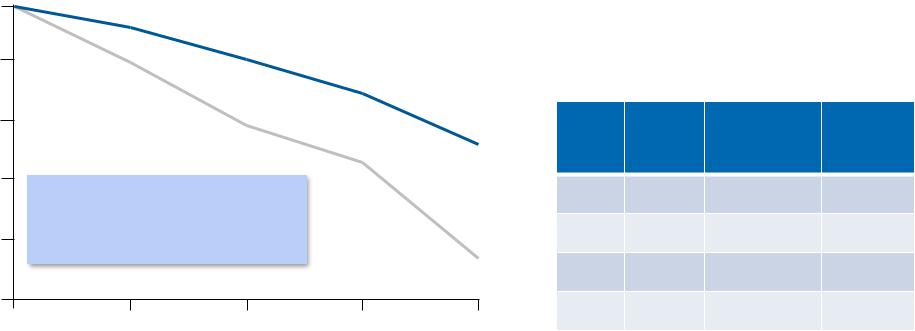
ASCEND:SupportiveсреднееAnalysisабсолютноеof Primary Endpoint:изменение ФЖЕЛ (мл)
Mean Change in FVC Volume (mL)*
|
0 |
|
|
|
|
|
|
|
|
-100 |
|
Пирфенидон (n = 278) |
|
|
|
|
|
) |
|
|
|
|
|
|
|
|
(мл |
|
|
|
|
|
|
|
|
ФЖЕЛ |
-200 |
|
|
|
|
|
Относительная |
Rank |
|
|
|
|
неделя |
мл |
разница |
ANCOVA |
|
Изменение |
|
|
|
|
|
|
% |
P-value |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
-300 |
|
|
|
13 |
59.6 |
62.5 |
< 0.0001 |
|
|
|
|
|
||||
|
|
Абсолютная разница = 193 mL |
Плацебо (n = 277) |
|
|
|
||
|
-400 |
Относительная разница= 45.1% |
|
26 |
111.0 |
54.9 |
< 0.0001 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
39 |
116.7 |
43.9 |
< 0.0001 |
|
-500 |
|
|
|
52 |
192.8 |
45.1 |
< 0.0001 |
|
0 |
13 |
26 |
39 |
||||
|
52 |
|
|
|
||||
|
|
|
Неделя |
|
|
|
|
|
King et al. N Engl J Med 2014; 370: 2083-92
Richeldi L et al. Respir Med 2016; 113: 74-79
Риск смертности от любых причин:
ASCEND & CAPACITY − объединенная популяция к 52 нед
кумулятивный риск |
смерти (%) |
Общий |
|
8 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Плацебо (n = 624) |
|
Количество оцененных |
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
6 |
|
|
|
HR 0.52 (95% CI 0.31–0.87)* |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
пациентов |
|
||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||
|
|
|
P = 0.011† |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
неделя |
|
Пирфенидон |
Плацебо |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0 |
|
490 |
624 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
13 |
|
618 |
619 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Пирфенидон (n = 623) |
26 |
|
609 |
603 |
||||||||||||||||||||||
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
39 |
|
596 |
586 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0 |
13 |
26 |
|
|
|
|
|
|
|
|
|
|
|
39 |
52 |
|
|
|
52 |
|
509 |
490 |
|||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
week |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
Впредварительно запланированном объединенном анализе, риск летального исхода от любых причин в группе пирфенидона снизился на 48% к 52 неделе в сравнении с плацебо (P = 0.01)
*Cox proportional hazards model; † log-rank test.
Nathan SD et al. Lancet Respir Med 2016, http://dx.doi.org/10.1016/S2213-2600(16)30326-5
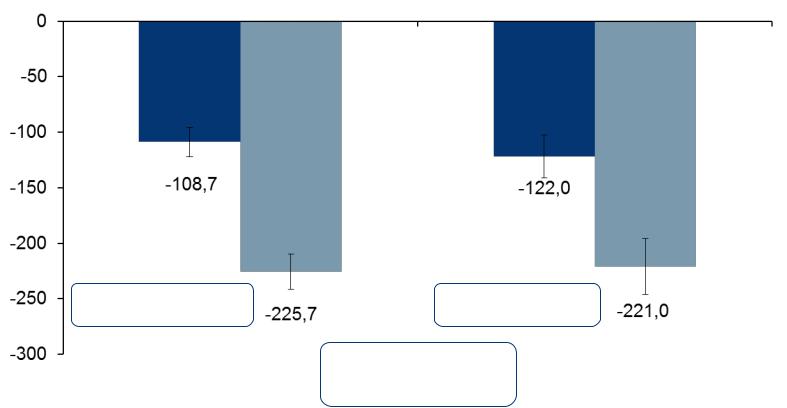
Ежегодная скорость снижения FVC при терапии нинтеданибом в зависимости от типа ИЛФ
rate (SE) of decline in |
(mL/year) |
annual |
FVC |
Adjusted |
|
Honeycombing on HRCT and/or confirmation |
Features of possible UIP pattern* on |
||
of UIP pattern by surgical lung biopsy |
HRCT and no surgical lung biopsy |
||
n=425 |
n=298 |
n=213 |
n=125 |
∆117.0 mL |
∆98.9 mL |
(95% CI: 76.3, 157.8) |
(95% CI: 36.4, 161.5) |
Treatment-by-time-by- subgroup interaction p=0.8139
|
Nintedanib |
|
Placebo |
*And traction bronchiectasis.
Raghu et al. AJRCCM 2017; 195: 78-85
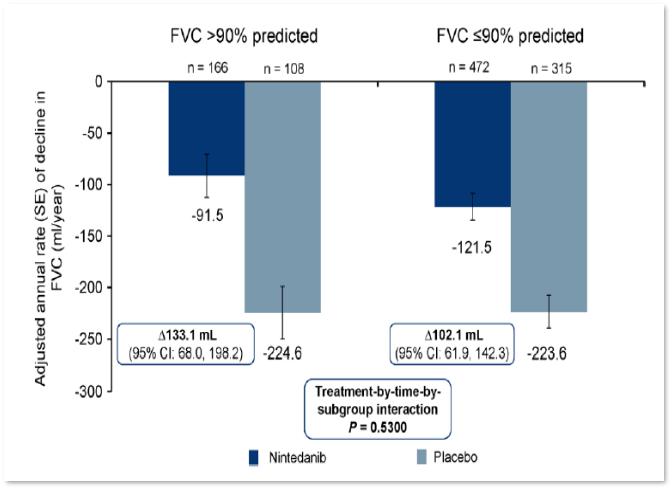
Нинтеданиб обеспечивает сходные преимущества у пациентов с сохранной функцией (ФЖЕЛ >90%) и (ФЖЕЛ ≤90%)
Kolb M et al. Thorax 2017; 72: 340–346
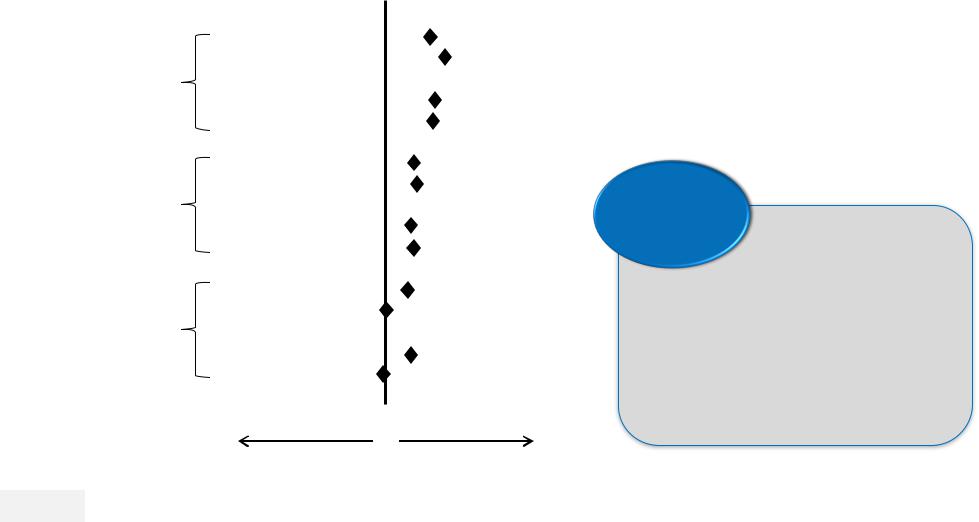
Пирфенидон эффективен у пациентов с ФЖЕЛ ≥80% или стадией по шкале − GAP I
Конечная
точка
ФЖЕЛ
6МШТ
UCSD
SOBQ
n=1247
|
|
Эффект от лечения* |
|
|
|||||||||||||||||||
подгруппа |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
p value |
||
FVC < 80% |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0.3969 |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
FVC ≥ 80% |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
GAP stage II-III |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0.8152 |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
GAP stage I |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
FVC < 80% |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0.9583 |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
FVC ≥ 80% |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
GAP stage II-III |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0.9327 |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
GAP stage I |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
FVC < 80% |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0.1957 |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
FVC ≥ 80% |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
GAP stage II-III |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0.0804 |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
GAP stage I |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
−1.0 |
−0.5 |
0.0 |
0.5 |
|
1.0 |
||||||||||||||||||
|
Преимущества |
|
|
|
|
Преимущество |
|||||||||||||||||
|
плацебо |
|
|
|
|
пирфенидона |
|
|
|||||||||||||||
Заключение
Пирфенидон одинаково эффективен у пациентов с ФЖЕЛ ≥ 80% vs <80% и GAP стадией I vs II/III
Albera C et al. Eur Respir J 2016;48:843
