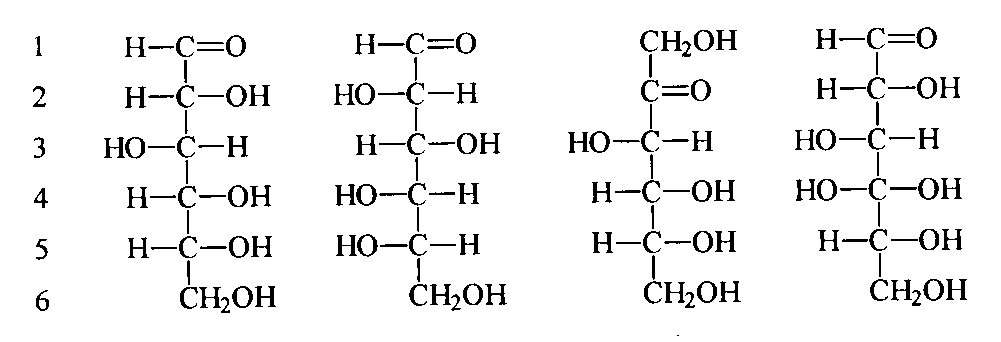- •Характеристика обмена углеводов
- •Болезнь гирке (гликогеноз при дефиците г-6-Фазы)
- •Болезнь мак-ардля (гликогеноз со снижением мышечной силы)
- •Высокие концентрации инсулина в крови обладают анаболическим, а низкие - катаболическим действием на обмен веществ
- •Метаболический синдром
- •Нарушение толерантности к глюкозе
- •Контроль за лечением диабета
- •Дневник больного сахарным диабетом
- •Гипергли-кемия
- •Кетонемия
- •Диабетический кетоацидоз
- •Гиперосмолярная некетоновая гипергликемия
- •Лекарственная гипогликемия
- •Гипогликемия из-за избытка инсулина при сд I типа
- •Функциональная гипогликемия
- •Алкогольная гипогликемия
- •Транзиторная гипогликемия у новорожденного
- •Большой плод от матери больной диабетом
- •Методические аспекты определения углеводов
- •Методические аспекты определения гликированного гемоглобина
- •Библиография

ДОЛГОВ В.В., АМЕТОВ А.С., ЩЕТНИКОВИЧ К.А., ДЕМИДОВА Т.Ю., ДОЛГОВА А.В.
ЛАБОРАТОРНАЯ ДИАГНОСТИКА НАРУШЕНИЙ ОБМЕНА УГЛЕВОДОВ,
САХАРНЫЙ ДИАБЕТ
МОСКВА - 2002
МИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ
ФЕДЕРАЦИИ
РОССИЙСКАЯ МЕДИЦИНСКАЯ АКАДЕМИЯ
ПОСЛЕДИПЛОМНОГО ОБРАЗОВАНИЯ

ДОЛГОВ В.В., АМЕТОВ А.С., ЩЕТНИКОВИЧ К.А., ДЕМИДОВА Т.Ю., ДОЛГОВА А.В.
ЛАБОРАТОРНАЯ ДИАГНОСТИКА НАРУШЕНИЙ ОБМЕНА УГЛЕВОДОВ,
САХАРНЫЙ ДИАБЕТ
Москва 2002
Лабораторная диагностика нарушений обмена углеводов, сахарный диабет
Авторы: В.В. Долгов, А.С.Аметов, К.А. Щетникович, Т.Ю.Демидова, Долгова А.В.
Книга подготовлена сотрудниками кафедры клинической лабораторной диагностики (профессором В.В. Долговым, доцентом К.А. Щетникович) и сотрудниками кафедры эндокринологии РМАПО (профессором А.С.Аметовым, доцентом Т.Ю.Демидовой и аспирантом А.В.Долговой). Книга составлена на основе опыта преподавания разделов клинической лабораторной диагностики и эндокринологии курсантам циклов переподготовки и повышения квалификации.
В пособии представлены данные по клинико-диагностическому значению определения показателей углеводного обмена. Особое внимание обращается на механизмы гликирования белков, значение этого процесса в осложнениях сахарного диабета, применение тестов, связанных с гликированием, для диагностических целей. Подробно с клиническими примерами разбираются болезни накопления гликогена, сахарный диабет, типы гипогликемии.
В пособии приведен обширный справочный материал, изложены принципы лабораторной диагностики заболеваний.
Пособие предназначено для врачей клинической лабораторной диагностики и эндокринологов, широкого круга врачей, использующих результаты лабораторного анализа в своей практике и студентов медицинских институтов
Спонсором издания данного учебного пособия является ПЛИВА - Лахема а.с., Брно, Чешская Республика.
Фирма ПЛИВА-Лахема - традиционный партнер лабораторной службы России, более 35 лет производит и поставляет широкий ассортимент диагностических средств для клинико-диагностических лабораторий. Компания имеет Представительство в Москве, создала совместное чешско-российское предприятие ЗАО “ЛАХЕМА ИТЕРНЭШНЛ”, широкую дилерскую сеть, позволяющую быстро и надежно поставлять реактивы в любой регион России.
ПЛИВА-Лахема а.с. поддерживает образовательные программы в области клинической лабораторной диагностики: организует семинары, участвует в конференциях и выставках, издает за свои средства учебно-методическую литературу как российских, так и чешских специалистов, спонсировала издание книги “Квалификационные тесты” по клинической лабораторной диагностике.
Авторы высказывают фирме искреннюю благодарность за поддержку издания данного учебного пособия.
Характеристика обмена углеводов
Характеристика углеводов
Углеводы - альдегиды и кетоны многоатомных спиртов. В зависимости от числа атомов углерода в молекуле моносахарида различают триозы, тетрозы, пентозы, гексозы и т.д. Моносахариды соединяются посредством гликозидной связи, образуя дисахариды, олигосахариды (до 6 моносахаридных остатков) и полисахариды (гликоген, крахмал). Углеводы образуют соединения с белком (гликопротеиды и протеогликаны), липидами (гликолипиды) и другими веществами (гетеромоносахариды). В организме наиболее распространены пентозы (входят в состав нуклеиновых кислот и коферментов, в частности НАДФ) и гексозы (глюкоза, фруктоза, галактоза).
В форме альдегидов моносахариды называются альдозами, в форме кетонов - кетозами (рис 1). Атомы углерода в молекуле гексоз номеруются от 1 до 6 (как показано около формулы D-глюкозы. Аббревиатура D- или L- отражает позицию гидроксильной группы ( -ОН ) в последнем положении перед группой -СН2ОН. D- и L-формы сахаров являются стереоизомерами; D-изомеры записываются с расположением гидроксильной группы справа, L-изомеры - слева от атома углерода. В организме человека сахара представлены в основном D-изоформами, именно к этой изоформе специфичны ферментные системы и транспортные белки, переносчики углеводов через клеточную мембрану.
D-глюкоза L-глюкоза D-фруктоза D-галактоза (альдоза) (альдоза) (кетоза) (альдоза) |
Рис. 1. Структурная формула гексоз, наиболее распространенных в организме.
|
D- и L-изоформы сахаров имеют асимметричные атомы углерода, связанные с разными группировками, поэтому обладают способностью вращать плоскость поляризованного луча. На этом основано определение D-глюкозы в моче с помощью поляриметра.
Альдегидная группа моносахаров может перестраиваться с образованием енольной формы, этому способствует щелочная среда. При высоких температурах и высоких концентрациях щелочей моносахариды не только способны перегруппировываться, но и ионизироваться. Так, в щелочной среде происходит сдвиг в сторону образования анионной формы енола:
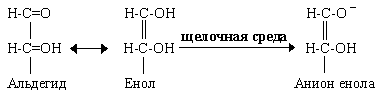
Наличие двойной связи и отрицательного заряда в анионной форме енола позволяет глюкозе быть активным восстановителем, на этом основана группа методов определения глюкозы. Так, глюкоза в щелочной среде восстанавливает ионы металлов, в частности соли Fe, Cu , с изменением окраски растворов, что используется при фотометрическом определении глюкозы. Другие сахара также способны восстанавливать ионы металлов в щелочной среде - они суммарно обозначаются как восстанавливающие сахара. Из-за присутствия группы восстанавливающих метаболитов в сыворотке крови при определении глюкозы методами, основанными на использовании её восстанавливающих свойств, результаты будут примерно на 20 % выше, чем при определении глюкозы специфическими методами. Это относится и к референтным (нормальным) диапазонам. Из-за большой вариации результатов, связанных в том числе и с изменениями уровня восстанавливающих метаболитов, от редуктометрических методов определения глюкозы в КДЛ в настоящее время повсеместно отказываются.
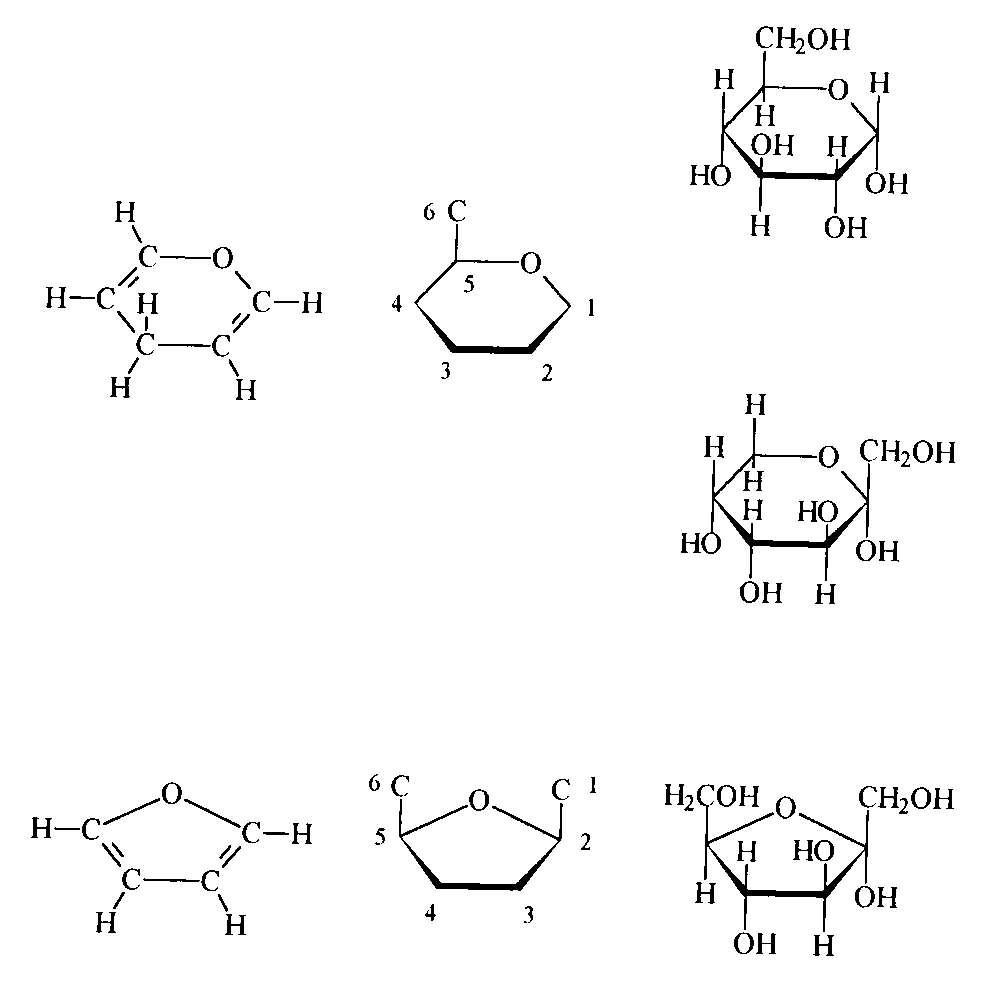
Альдегидная группа моносахаридов взаимодействует с гидроксильной группой, находящейся около 5 углеродного атома, формируя пиранозное кольцо. В виде кольца структура сахаров изображается на плоскости, при этом более жирные линии показывают стороны, направленные в сторону читателя. Расположение гидроксильной группы в 1 позиции определяет конфигурацию: если она расположена под кольцом - то это конфигурация, если над кольцом - конфигурация. Если в состав кольца входит 5 атомов углерода и 1 кислород - это производное пирана и обозначается как пиранозная структура, если кольцо состоит из 4 атомов углерода и 1 кислорода, это производное фурана - соответственно фуранозная структура (рис. 2).
D-Фруктоза D-Фруктофураноза
Фуран
D-Фруктоза D-Фруктопираноза
D-Глюкоза D-Глюкопираноза
Пиранозная
структура
Пиран
Фуранозная
структура
|
Рис. 2. Проекционные формулы Хеуорса для глюкопираноз и фруктофураноз. D-глюкопираноза - это внутримолекулярный полуацеталь , содержащий асимметричный С5 атом. Систематическое название для кольцевой формы D-глюкозы будет D-глюкопираноза |
Для разных моносахаридов константа равновесия между открытой и циклической формой различна. Для глюкозы она составляет примерно 5 х 10-4, поэтому из общего количества в сыворотке только около 0,002 % глюкозы постоянно присутствует в открытой форме. В циклической форме углеводы устойчивы и малоактивны, в открытой форме углеводы обладают высокой реакционной способностью и могут взаимодействовать без участия ферментов с белками (рис. 3), нуклеотидами и липидами; эти реакции получили название гликирования.
Способность к гликированию различна у разных сахаров, это в частности зависит от соотношения открытой и кольцевой форм сахаров. В таблице 1 приведено процентное содержание открытой формы и относительная реакционная способность по гликированию для наиболее распространенных в организме сахаров и их фосфорилированных форм.
Исходя из данных таблицы 1, следует, что гликирующая способность глюкозы меньше, чем у фруктозы в 7,5 раз, чем у галактозы в 4,7 раза, чем у глюкозо-6-фосфата в 50 раз, чем у фруктозо-6-фосфата в 75 раз. Тем не менее, концентрация в сыворотке крови глюкозы значительно выше, чем всех других углеводов, поэтому именно глюкоза вносит основной вклад в процесс гликирования внеклеточных белков. В связи с этим высказываемые предположения о замене пищевой глюкозы на плохо усваиваемую фруктозу могут быть чреваты осложнениями, связанными с усилением процессов гликирования белков. У фруктозы и галактозы больший процент молекул находится в открытой форме, они активнее, чем глюкоза взаимодействуют неферментативно с белками. С этим связано, по-видимому, токсическое действие галактозы у детей с галактоземией.
НОСН
СНО


Открытая форма
глюкозы
0,002
%

НСОН
НСОН
О
НОСН
НОСН

К = 510-4
НСОН
НСОН
СН
НСОН

СН2ОН
СН2ОН


БЕЛОК
- NН2
Быстрый переход
обратимая реакция
Н2С-NH-БЕЛОК
НСО=N-БЕЛОК
Н2С-NH-БЕЛОК
НСОН
НСОН
СО


НОСН
НОСН
НОСН
Восстановлен-ное
основание Шиффа
Основание Шиффа
НСОН
НСОН
НСОН
Кетоамины (фруктозамины)
СН
НСОН
НСОН
СН2ОН
СН2ОН
СН2ОН
Необратимые стадии, при которых
образуются стабильные гликированные
белки
Рис. 3. Неферментативное гликирование белков при взаимодействии с глюкозой. Гликированию подвержены в крови гемоглобин, белки эритроцитарных мембран, коллаген, сывороточные белки, в том числе альбумин, белки липопротеидов, некоторые ферменты (алкогольдегидрогеназа), мембранные белки эндотелиальных клеток и др.
Таблица 1. Процентное содержание открытой формы и относительная реакционная способность в процессах гликирования некоторых сахаров и их производных.
Реакционная способность гликирования сахаров
|
||
Углевод |
% свободной альдозной (кетоновой) форм |
Относительная гликирующая способность |
Глюкоза |
0,002 |
1 |
Фруктоза |
0,25/0,7 |
7,5 |
Галактоза |
0,02 |
4,7 |
Манноза |
0,005 |
5,3 |
Рибоза |
0,05 |
6,7 |
Глюкоза-6-фосфат |
< 0,4 |
50 |
Фруктозо-6-фосфат |
4 - 5 |
75 |
Переваривание и всасывание
Гидролиз гликогена и крахмала пищи начинается в ротовой полости под влиянием амилазы слюны. Моносахариды способны всасываться уже в ротовой полости. В желудке нет ферментов, осуществляющих гидролиз углеводов. В полости тонкой кишки под влиянием амилазы сока поджелудочной железы они гидролизуются до декстринов и мальтозы (полостное переваривание). На поверхности микроворсинок энтероцитов локализованы ферменты сахараза, мальтаза, лактаза, изомальтаза и другие, расщепляющие декстрины и дисахариды до моносахаров (пристеночное пищеварение).
При врожденном или приобретенном недостатке одного или нескольких ферментов гидролиза дисахаридов развивается дисахаридазная недостаточность. Всасываются углеводы в виде моносахаров. Дисахариды блокируют места всасывания моносахаридов, поэтому всасывание моносахаридов нарушается. У детей при лактазной недостаточности развивается гипотрофия. Непереваренная лактоза поступает в толстую кишку, где расщепляется бактериями до органических кислот (молочная, уксусная). Повышение лактозы и органических кислот нарушает осмолярность в просвете кишки, нарастает секреция жидкости, объем химуса, увеличивается моторика кишечника, развивается диарея. Диагностика дисахаридазной недостаточности основана в первую очередь на клинических проявлениях, а также на определении активности ферментов дисахаридаз в биоптатах слизистой оболочки тонкой кишки, определении лактозы, сахарозы в кале, снижении рН кала, проведении нагрузочных тестов. В то же время ионы водорода, образующиеся при расщеплении органических кислот, способны поступать в кровоток. В удаление избытка ионов Н+ включаются легкие, состояние проявляется увеличением концентрации водорода в конденсатах выдыхаемого воздуха.
Скорость всасывания отдельных моносахаров в тонкой кишке различна. Глюкоза и галактоза всасываются быстрее других моносахаридов. Для глюкозы, очевидно, существует пассивная диффузия, облегченный транспорт и активный перенос за счет энергии, освобождающейся при гидролизе АТФ. Транспорт глюкозы из просвета тонкой кишки через энтероциты осуществляется с помощью белкового натрий- глюкозного транспортера. Глюкоза связывается с ионами натрия, освобождаясь от него на внутренней поверхности мембраны, в этом процессе принимает участие мембраносвязанная Na,K–АТФаза. Кроме того, имеется собственный транспортер глюкозы GluT-5, который помимо глюкозы осуществляет транспорт фруктозы. Глюкоза практически вся всасывается достаточно быстро. Другие сахара, такие как манноза, ксилоза, арабиноза всасываются только пассивной диффузией. На всасывание углеводов влияет функциональное состояние пищеварительного тракта, состав пищевых веществ, витамины, микроэлементы и т.д. Нарушение всасывания (мальабсорбция) диагностируется по целому комплексу клинических, функциональных и лабораторных исследований.
Метаболизм глюкозы в клетках.
В клетки тканей организма глюкоза может поступать как экзогенная из пищи, так образованная эндогенно из депонированного гликогена (в результате гликогенолиза) или из других субстратов, таких как лактат, глицерол, аминокислоты (в результате глюконеогенеза). Всосавшаяся в тонкой кишке глюкоза поступает через воротную вену в печень и попадает в гепатоциты. По своей природе глюкоза является гидрофильным веществом, следовательно она не может свободно поникнуть через фосфолипидную мембрану. Механизм ее транспорта осуществляется с помощью белков-переносчиков. При стимуляции инсулином наблюдается увеличение содержания этих белков в плазматических мембранах в 5-10 раз при одновременном уменьшение их одержания на 50-60% внутри клетки. Для стимуляции передвижения белков-переносчиков к мембране требуется дальнейшее стимулирующие влияние инсулина. На сегодняшний день выделено два класса транспортеров глюкозы:
Na-глюкозный котранспортер, который экспрессируется специальными эпителильными реснитчатыми клетками тонкой кишки и проксимальным отделом почек. Этот белок осуществляет активный транспорт глюкозы из просвета кишки или нефрона против градиента концентрации путем связывания глюкозы с теми ионами натрия, которые транспортируются ниже градиента концентрации.
Собственные транспортеры глюкозы. Это мембранные белки, находящиеся на поверхности всех клеток и осуществляющие транспорт глюкозы ниже градиента концентрации. Транспортеры глюкозы осуществляют перенос глюкозы не только в клетку, но и из клетки и также участвуют во внутриклеточном передвижении глюкозы. В настоящее время описано 6 транспортных белков для глюкозы – GluT.
В клетках глюкоза фосфорилируется в гексокиназной реакции, превращаясь в глюкозо-6-фосфат (Гл-6-Ф), Гл-6-Ф является субстратом нескольких путей метаболизма: с этой молекулы начинается синтез гликогена, пентозофосфатный цикл, гликолитический распад до лактата или аэробное полное расщепление до СО2 и Н2О. В клетках, способных к глюконеогенезу (клетки печени, почек, кишечника), Гл-6-Ф может дефосфорилироваться и в виде свободной глюкозы поступать в кровь и переноситься в другие органы и ткани.
Особенно важна глюкоза для клеток мозга. Клетки нервной системы зависят от глюкозы как от основного энергетического субстрата. В то же время в мозге нет запасов глюкозы, она там не синтезируется, нейроны не могут потреблять другие энергетические субстраты, кроме глюкозы и кетоновых тел, глюкоза практически полностью может исчерпываться из внеклеточной жидкости, так как клетки нервной системы потребляют глюкозу инсулин-независимым путем.
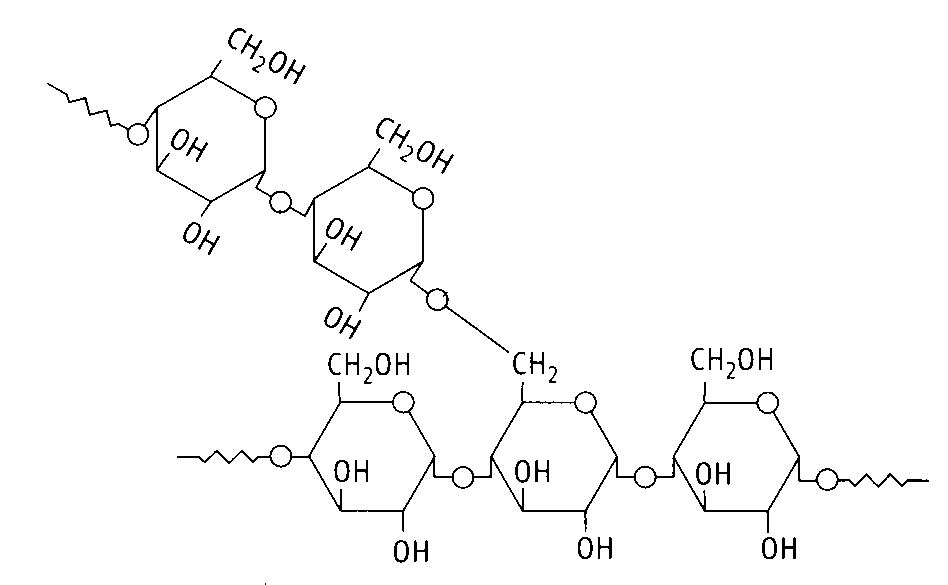
Гликоген. Из Гл-6-Ф в результате сочетанного действия гликогенсинтетазы и «ветвящего» фермента синтезируется гликоген - полимер, напоминающий по виду дерево. В молекуле гликогена может содержаться до миллиона моносахаридов. При этом происходит как бы кристаллизация гликогена и он не обладает осмотическим эффектом. Такая форма пригодна для хранения в клетке. Если бы такое количество молекул глюкозы было растворено, то из-за осмотических сил клетку бы разорвало. Гликоген является депонированной формой глюкозы и энергии. Он содержится практически во всех тканях, в клетках нервной системы его минимальное количество, в печени и мышцах его особенно много. Гликоген содержит только 2 типа гликозидных связей: (14)-тип и (16)-тип. Связь (14)-тип формируется через каждые 8-10 остатков D-глюкозы (рис 4).
|
Рис. 4. Структура гликогена. За счет (14)- и (16)-гликозидных связей формируется ветвистая молекула гликогена, содержащая до 1 млн. остатков D-глюкозы |
Гликогенолиз. Это путь расщепления гликогена. Гликоген в организме в основном сохраняется в печени и скелетных мышцах. Гликоген мышц используется в качестве источника энергии при интенсивной физической нагрузке. Гликогенолиз в печени активируется в ответ на снижение глюкозы при перерывах в приеме пищи или как стрессовая реакция. Основными гормонами, активирующими гликогенолиз, являются глюкагон, адреналин (эпинефрин) и кортизол (таблица 2 ).
Таблица 2
Гормональная регуляция гликогенолиза
|
|||
Гормон
|
Место образования |
Инициатор |
Эффект на гликогенолиз |
Глюкагон |
клетки поджелудочной железы |
гипогликемия |
быстрая активация |
Адреналин |
мозговой слой надпочечника |
стресс, гипогликемия |
быстрая активация |
Инсулин |
клетки поджелудочной железы |
гипергликемия |
подавление |
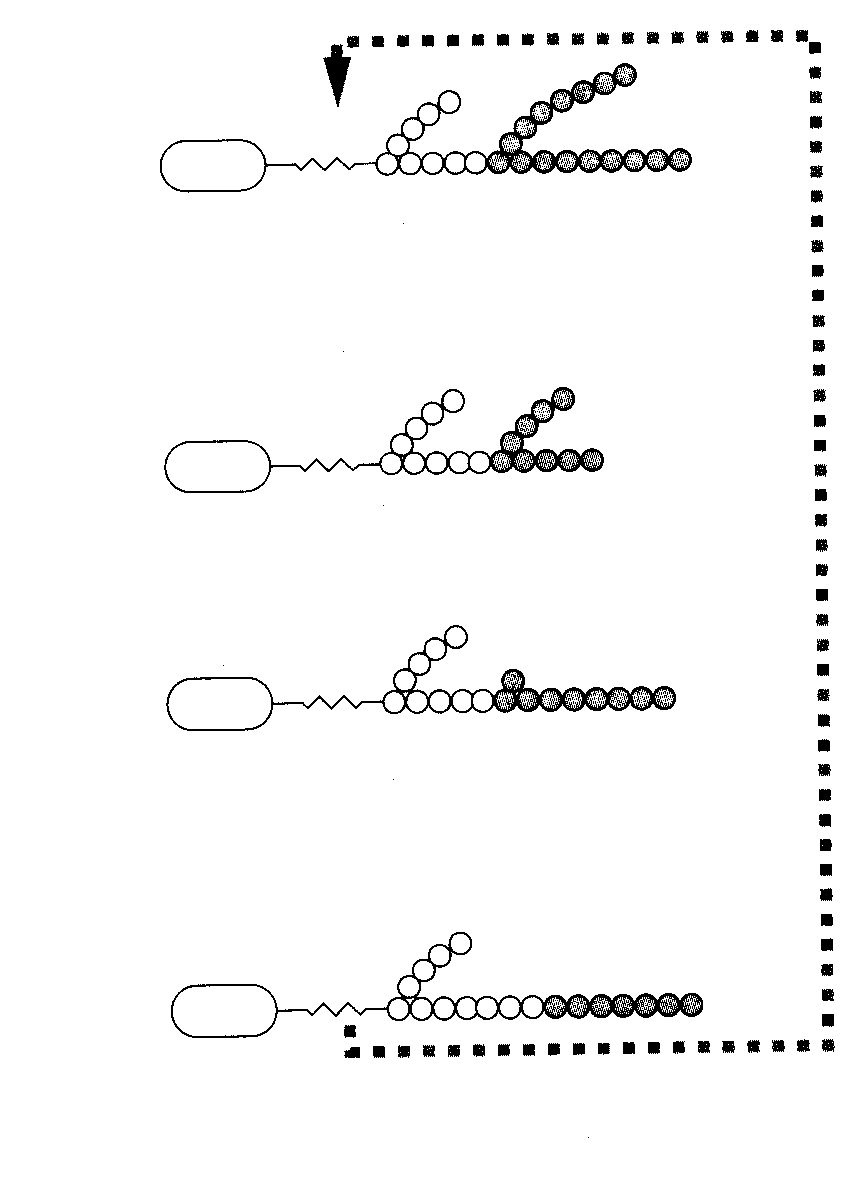
Гликогенолиз начинается с отщепления концевых остатков глюкозы по связям (14), в этом процессе ключевым ферментом является гликогенфосфорилаза (рис 5.). Активация фосфорилазы осуществляется фосфорилированием с участием цАМФ-зависимой протеинкиназы и киназы фосфорилазы. Контролируют активацию фосфорилазы катехоламины (печень, мышцы) и глюкагон (печень). Эти гормоны способствуют расщеплению гликогена в печени и тем самым гипергликемическому ответу. Продуктом фосфорилазной реакции является глюкозо-1-фосфат (Г-1-Ф), который превращается в Г-6-Ф при участии фермента фосфоглюкомутазы. В печени глюкоза образуется из Г-6-Ф и Г-1-Ф при участии соответственно ферментов Г-6-Фтазы и Г-1-Фтазы. Фермент фосфорилаза специфичен только для связей (14). Он расщепляет гликоген до тех пор, пока в конце ветви не останется 3-4 углеводных остатка. Затем действует ферментный комплекс из трансглюкозилазы и глюкозидазы. Первый из этих ферментов переносит (транслоцирует) короткий сегмент углеводных остатков в конец цепи (14), второй отщепляет глюкозу по связи (16). Цикл с участием фосфорилазы и ферментного комплекса, разрушающего ветвления гликогена, повторяется. Около 90 % глюкозы освобождается из гликогена в виде Г-1-Ф при разрушении связи (14), 10 % в виде свободной глюкозы при разрушении связи (16). Глюкоза может образовываться из гликогена при участии амило-1,6-глюкозидазы, расщепляющей боковые цепи гликогена.
ядро
ядро
Г-6-Фаза
Трансглюкозилаза
Фосфорилаза
«Ветвящий»
фермент
Фосфоглюкомутаза
Глюкозидаза
Синтез гликогена
кровь
Глюкоза
Г-6-Ф
Г-1-Ф
II
тип
I
тип
III
тип
IV
тип
мышцы V
тип,
печень - VI тип |
Рис. 5. Дефекты ферментов метаболизма гликогена, приводящих к гликогенозам разного типа. |
Гликогенозы. Это группа наследственных заболеваний, связанных с дефектами ферментов, при которых нарушен распад гликогена (рис. 5) и, несмотря на огромный запас гликогена в органах, у больных детей развивается гипогликемия (таблица 3).
Таблица 3.
Гликогенозы - болезни накопления гликогена
|
|||
Тип |
Название болезни |
Дефект фермента |
Структурные и клинические проявления дефекта |
I |
von Gierke’s ( Гирке ) |
глюкозо-6-фосфатаза |
тяжелая постабсорбционная гипогликемия, лактоацидоз, гиперлипидемия |
II |
Pompe’s ( Помпе ) |
лизосомальная -глюкозидаза |
гранулы гликогена в лизосомах |
III |
Cori’s ( Кори ) |
трансглюкозилаза/ глюкозидаза |
измененная структура гликогена, гипогликемия |
IV |
Andersen’s ( Андерсен ) |
«ветвящий» фермент |
измененная структура гликогена
|
V |
McArdle’s ( Мак-Ардль ) |
мышечная фосфорилаза |
отложение гликогена в мышцах, судороги при физической нагрузке |
VI |
Hers’ ( Геру ) |
фосфорилаза печени |
гипогликемия, но не такая тяжелая, как при I типе |
Наиболее изучена болезнь Гирке (гликогеноз I типа), при этом заболевании блокировано расщепление гликогена из-за отсутствия фермента глюкозо-6-фосфатазы, структура гликогена нормальная. Нарушено образование свободной глюкозы, образуется много лактата. Гипогликемия приводит к активации жирового обмена, окисление липидов сопровождается образованием кетоновых тел. Гипогликемия проявляется ярко при определении глюкозы в крови глюкозоксидазным и гексокиназным методами, в то время как редуктометрическим методом по Хагедорну из-за присутствия в крови восстанавливающих веществ результаты определения глюкозы значительно искажаются. Велика ценность адреналиновой и глюкагоновой пробы, так как адреналин и глюкагон не повышают уровень глюкозы в крови из-за неспособности печени поставлять свободную глюкозу из гликогена.
ИСТОРИЯ БОЛЕЗНИ № 1