
- •Рекомендовано до друку
- •Укладачі: с. Мягкота, х. Василів, м. Марків, я. Білий, п. Панасюк, о. Кушнір, о. Вовк, т. Куречко
- •Визначення питомої потужності електричної лампи
- •І. Теоретичні відомості
- •Іі. Опис приладів і методика вимірювання
- •III. Хід роботи
- •Контрольні питання
- •Вивчення тонкої лінзи
- •І. Теоретичні відомості
- •III. Хід роботи
- •IV. Завдання науково-дослідного характеру
- •Контрольні питання
- •Вивчення аберацій лінз
- •І. Теоретичні відомості
- •II. Хід роботи
- •Контрольні питання
- •Визначення числової апертури та роздільної здатності мікроскопа
- •І. Опис приладів і методика вимірювання
- •Іі. Завдання
- •III. Хід роботи
- •Контрольні питання
- •Визначення радіуса кривизни лінзи за допомогою кілець ньютона
- •І. Теоретичні відомості
- •Іі. Опис приладів і методика вимірювання
- •Ііі. Завдання
- •IV. Хід роботи
- •Контрольні питання
- •Визначення довжини світлової хвилі за допомогою біпризми френеля
- •І. Теоретичні відомості
- •Іі. Опис приладів і методика вимірювання
- •Ііі. Завдання
- •IV. Хід роботи
- •Контрольні питання
- •Визначення сталої дифракційної гратки та довжини світлової хвилі
- •І. Теоретичні відомості
- •Ііі. Завдання
- •IV. Хід роботи Завдання 1. Визначення сталої дифракційної гратки
- •Завдання 2. Визначення довжини світлової хвилі
- •Контрольні питання
- •Визначення довжини хвилі випромінювання оптичного квантового генератора
- •І. Теоретичні відомості
- •Іі. Опис приладів і методика вимірювання
- •Ііі. Завдання
- •IV. Хід роботи
- •Контрольні питання
- •Вивчення основних явищ поляризації на приладі норенберга
- •I. Теоретичні відомості
- •Іі. Завдання
- •Ііі. Хід роботи
- •Контрольні питання
- •Вивчення явищ обертової поляризації світла
- •І. Теоретичні відомості
- •Іі .Опис приладів і методика вимірювання
- •Ііі. Завдання
- •IV. Хід роботи
- •Контрольні питання
- •Дослідження режимів газового розряду у ртутно-кварцовій лампі
- •І. Теоретичні відомості
- •Іі. Опис приладів і методика вимірювання
- •Ііі. Завдання
- •IV. Хід роботи
- •Контрольні питання
- •Визначення концентрації розчинів за допомогою фотоелектричного колориметра-нефелометра фек-56
- •І. Теоретичні відомості
- •Іі. Опис приладів і методика вимірювання
- •III. Завдання
- •IV. Хід роботи
- •Контрольні питання
- •Вивчення характеристик фотоелементів
- •І. Теоретичні відомості
- •Іі. Опис приладів і методика вимірювання
- •III. Завдання
- •IV. Хід роботи
- •Контрольні питання
- •Вивчення магнітного обертання площини поляризації
- •І. Теоретичні відомості
- •Іі. Опис приладів і методика вимірювання
- •III. Завдання
- •IV. Хід роботи
- •Контрольні питання
- •Визначення вольт-амперних і світлових характеристик фотоопору
- •І. Теоретичні відомості
- •Іі. Опис приладів і методика вимірювання
- •III. Завдання
- •IV. Хід роботи
- •Контрольні питання
- •Визначення концентрації розчину цукру за допомогою рефрактометра
- •І. Теоретичні відомості
- •Іі .Опис приладів і методика вимірювання
- •Ііі. Завдання
- •IV. Хід роботи
- •Контрольні питання
- •Визначення сталої стефана-больцмана
- •І. Теоретичні відомості
- •Іі. Опис приладів і методика вимірювання
- •Ііі. Завдання
- •IV. Хід роботи
- •Контрольні питання
- •Визначення коефіцієнта поглинання твердих тіл
- •І. Теоретичні відомості
- •Іі. Опис приладів і методика вимірювання
- •Ііі. Завдання
- •IV. Хід роботи
- •Контрольні питання
- •Градуювання спектроскопа та визначення довжин хвиль спектральних ліній досліджуваної речовини
- •І. Теоретичні відомості
- •Іі. Опис приладів і методика вимірювання
- •Ііі. Завдання
- •IV. Хід роботи
- •Контрольні питання
- •Визначення показника заломлення прозорих твердих тіл за допомогою мікроскопа
- •І. Теоретичні відомості
- •Іі. Опис приладів і методика вимірювання
- •Ііі. Завдання
- •IV. Хід роботи
- •Вивчення водневих спектрів та визначення сталої рідберга
- •І. Теоретичні відомості
- •Спектр водню і будова атома водню. Енергетичні рівні в атомі водню.
- •Іі. Опис приладів і методика вимірювання
- •Ііі. Завдання
- •IV. Хід роботи
- •Контрольні питання
- •Визначення сталої планка за спектром водню
- •І. Теоретичні відомості
- •Іі. Опис приладів і методика вимірювання
- •Ііі. Завдання
- •IV. Хід роботи
- •Контрольні питання
- •Вивчення взаємодії радіоактивного -випромінювання з речовиною
- •І. Теоретичні відомості
- •Іі. Опис приладів і методика вимірювання
- •Ііі. Завдання
- •IV. Хід роботи
- •Контрольні питання
- •Вивчення взаємодії радіоактивного -випромінювання з речовиною та вивчення його кількісних характеристик
- •І. Теоретичні відомості
- •Іі. Опис приладів і методика вимірювання
- •Ііі. Завдання
- •IV. Хід роботи
- •Контрольні запитання
- •Бібліографічний список
- •Додаток
Вивчення водневих спектрів та визначення сталої рідберга
Прилади і матеріали: спектроскоп, установка з газорозрядними лампами.
Мета роботи: навчитися градуювати спектроскоп та визначити постійну Рідберга.
І. Теоретичні відомості
Експериментальне дослідження спектрів випромінювання різних розріджених газів (тобто спектрів випромінювання атомів) виявили лінійчасті спектри, для яких справджуються певні закономірності.
Для водню було виявлено, що спектри випромінювання в енергетичному діапазоні розміщуються серіями ліній, котрі відносяться до однієї серії і зв’язані між собою функціональними залежностями.
Для видимої частини спектру випромінювання водню Бальмер виявив серію ліній (серію Бальмера), частота яких виражається емпіричною формулою:
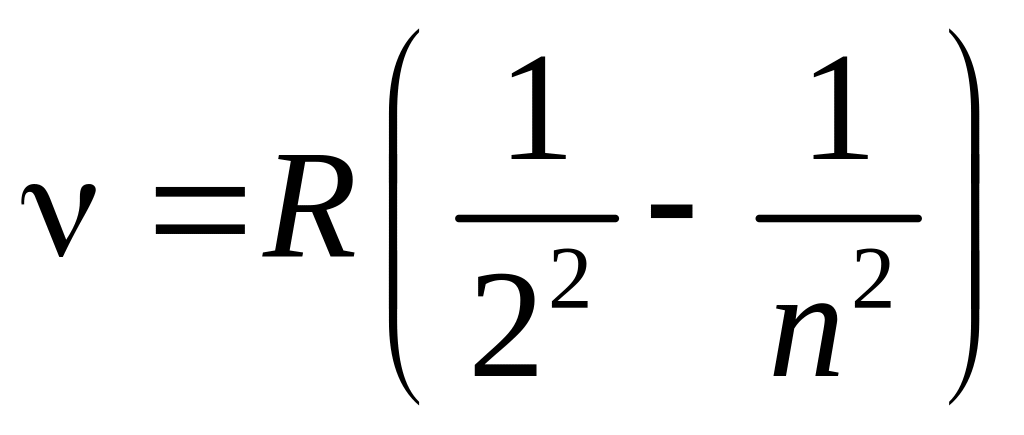 , (1)
, (1)
де n
=3, 4, 5, 6... ; R=3,28![]() –
стала Рідберга.
–
стала Рідберга.
У спектрі водню знаходиться ще декілька серій, зокрема серія Лаймана в ультрафіолетовій частині спектра і серія Пашена в інфрачервоній частині спектра (рис. 1). Серія Лаймана описується формулою:
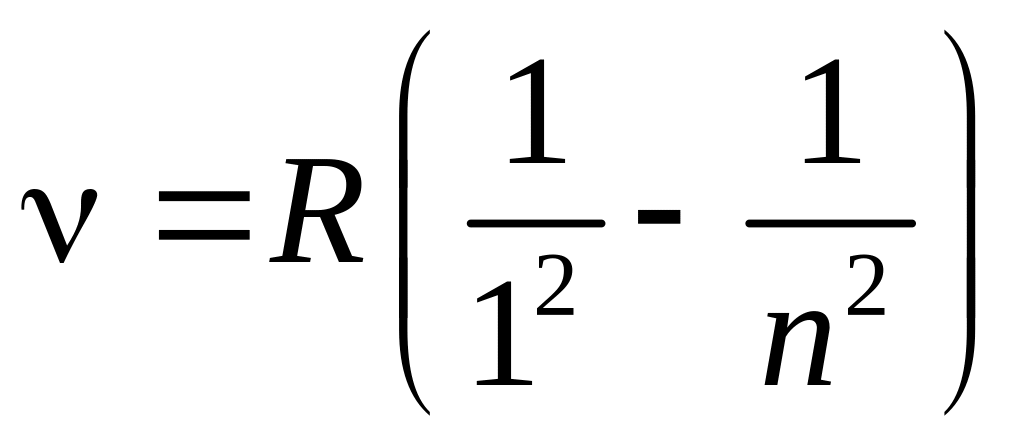 , (2)
, (2)
де n = 2, 3, 4; а серія Пашена – формулою:
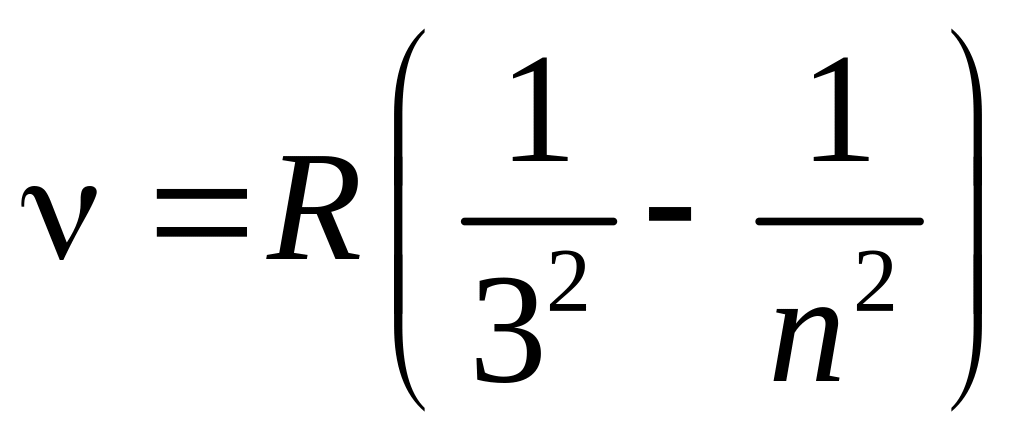 , (3)
, (3)
д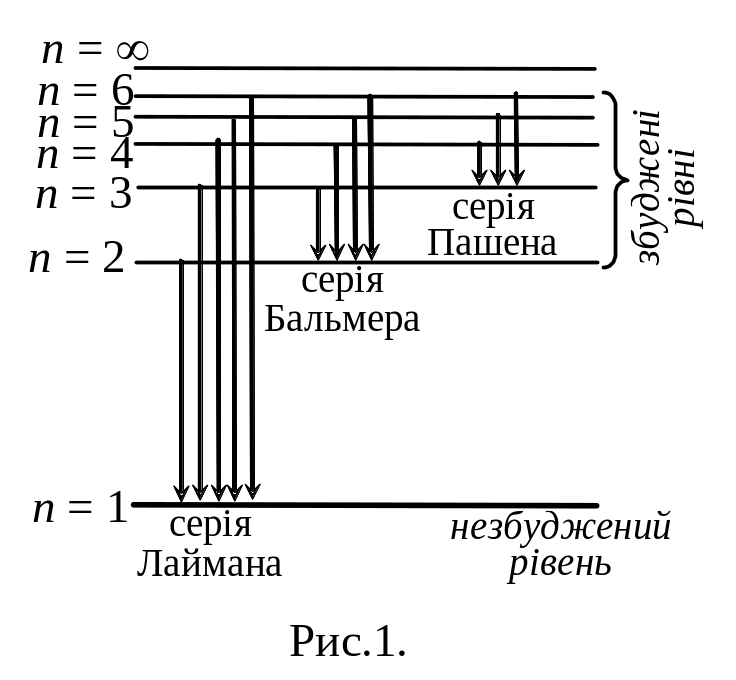 е
n
= 4, 5, 6.
е
n
= 4, 5, 6.
Серії Бальмера, Лаймана і Пашена схематично зображені на рис.1.
Лінійчастий характер спектрів випромінювання (і поглинання) атомів вказує на те, що атом може випромінювати (і поглинати) енергію тільки певними порціями – квантами. Тобто, звідси випливає, що атом може знаходитися лише в певних дискретних енергетичних станах. Переходячи з одного стану в інший, він випромінює або поглинає квант енергії, який дорівнює різниці енергій початкового і кінцевого станів (до випромінювання і після цього).
Виходячи з уявлень про дискретність енергетичних станів атома Н. Бор (1913 р., датський фізик) створив квантову теорію будови атома. В основу поклав три постулати (постулати Бора):
Електрони можуть рухатися в атомі тільки по орбітах цілком певного радіуса. Момент кількості руху електрона на цих орбітах кратний величині
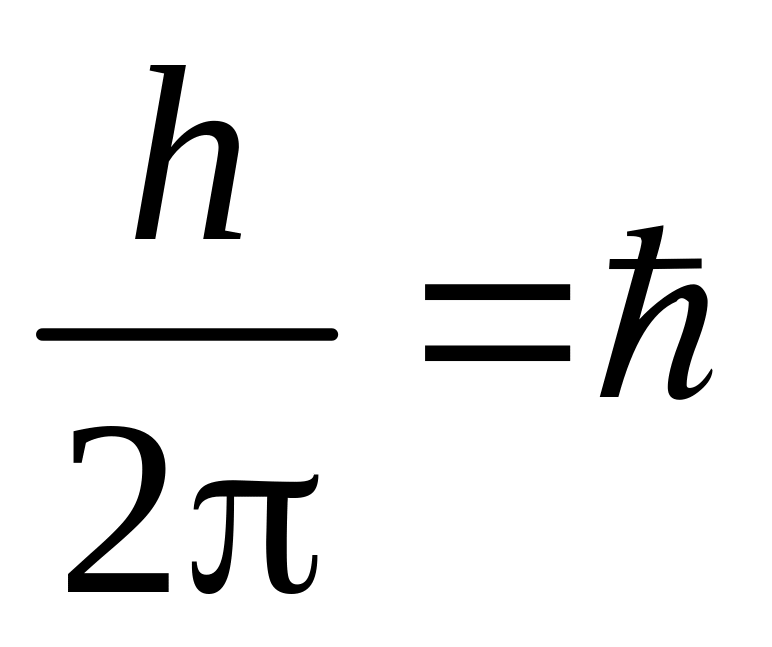 :
:
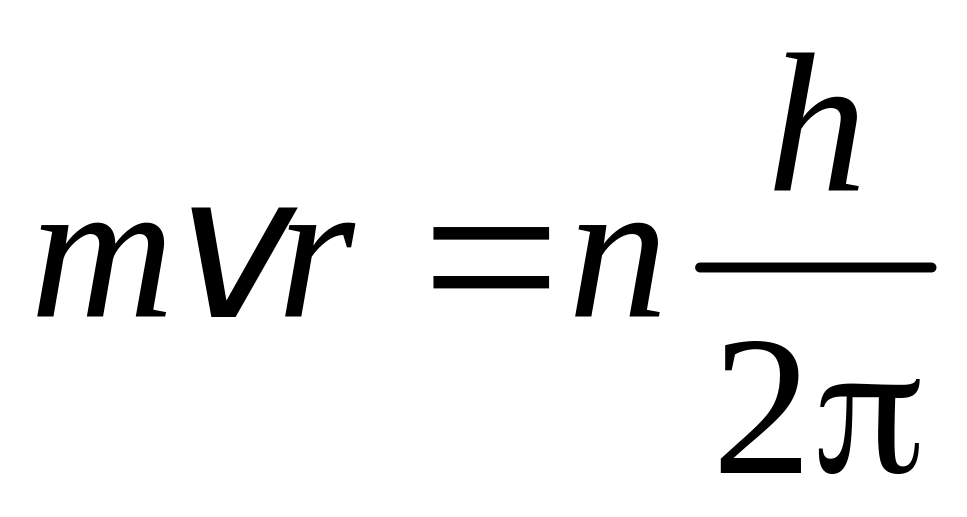 , (4)
, (4)
де m – маса електрона, v – швидкість електрона, r – радіус орбіти, n – головне квантове число (n – 1, 2, 3...), h – стала Планка.
Рух електронів на стаціонарних орбітах не супроводжується випромінюванням (поглинанням) енергії.
Перехід електрона з однієї стаціонарної орбіти на іншу супроводжується випромінюванням (або поглинанням кванта енергії).
Величина цього кванта hv дорівнює різниці енергії (W1 і W2) стаціонарних станів атома до і після випромінювання (поглинання):
hv = W1 - W2 . (5)
Умову (4) називають умовою квантування радіуса орбіт, а умову (5) – умовою частот.
Отже, частота електромагнітних хвиль, які випромінюються атомом, визначається не частотою обертання електрона навколо атома, а різницею енергій стаціонарних станів атома.
Таким чином, постулати Бора суттєво доповнили модель Резерфорда, позбавивши її від протиріч з експериментом щодо стійкості атомів.
Спектр водню і будова атома водню. Енергетичні рівні в атомі водню.
В атомі водню навколо ядра (протона) рухається один електрон. Враховуючи суттєво більшу масу протона відносно маси електрона (в 1840 разів), можна допустити, що ядро є нерухомим, а орбіти електрона – кругові. На електрон, що обертається навколо протона, діє дві сили: доцентрова і кулонівська, які себе взаємно зрівноважують. Тобто:
![]() , (6)
, (6)
де
![]() Ф/м. Розв’язуючи рівняння (6) і (4),
отримаємо:
Ф/м. Розв’язуючи рівняння (6) і (4),
отримаємо:
![]() , (7)
, (7)
Використовуючи
вираз (7), можна розрахувати радіус
будь-якої стаціонарної орбіти електрона.
Для прикладу радіус першої орбіти
![]() А.
А.
Визначимо повну
енергію W
електрона в атомі водню. Вона дорівнює
сумі кінетичної енергія
![]() електрона (за його поступального руху
на орбіті) і потенціальної енергії Wп
(притягання електрона до ядра).
електрона (за його поступального руху
на орбіті) і потенціальної енергії Wп
(притягання електрона до ядра).
Використавши рівняння (6), отримаємо:
![]() . (8)
. (8)
Потенціальна енергія електрона є від’ємною і чисельно дорівнює:
![]() . (9)
. (9)
Враховуючи вирази (8) і (9), отримаємо:
![]() . (10)
. (10)
Підставимо в рівняння (10) вираз для r із формули (7). Отримаємо:
![]() . (11)
. (11)
За умови переходу електрона з однієї стаціонарної орбіти на іншу (ближчу до ядра), випромінюється квант енергії, який дорівнює різниці енергій енергетичних рівнів атома до випромінювання і після нього.
Самовільного переходу електрона на більш високу орбіту не буває. Для такого переходу необхідно надати атому певну порцію енергії.
Розглянута теорія енергетичних станів атома водню може бути застосована і для водневоподібних атомів, тобто до іонів, в яких на зовнішній орбіті знаходиться один електрон (He, Li+, Be2+).
Квантова теорія Бора дала можливість кількісно пояснити особливості спектрів поглинання та випромінювання атомів водню та іонів водневоподібних атомів, однак не годилася для розрахунку спектрів поглинання та випромінювання багатоелектронних атомів. Подальший розвиток теорії, підвалини якої заклав Н. Бор, привів до створення сучасної квантової механіки, котра може кількісно пояснити особливості будови і властивості різних багатоелектронних атомів і молекул.
