
- •Решение задач егэ части с: мкт
- •Возможное решение:
- •Возможное решение:
- •Возможное решение:
- •Возможное решение
- •Возможное решение
- •Возможное решение:
- •Возможное решение:
- •Возможное решение
- •Возможное решение
- •Возможное решение:
- •Возможное решение:
- •Возможное решение:
- •Возможное решение:
- •Возможное решение:
- •Возможное решение:
- •Возможное решение:
- •Возможное решение:
- •В озможное решение:
- •Возможное решение:
- •Возможное решение:
- •Возможное решение:
- •Возможное решение:
- •Возможное решение:
- •Возможное решение:
- •В озможное решение:
- •Возможное решение:
- •Возможное решение:
- •Возможное решение:
Возможное решение:
П усть
т
-
масса
одного газа.
усть
т
-
масса
одного газа.
Тогда плотность смеси:
![]()
где V- объем сосуда.
Отсюда
![]()
Запишем закон Менделеева-Клапейрона для каждого газа (например, для гелия; для остальных - аналогично):
![]()
где P1 - парциальное давление в данном случае гелия.
Следовательно,
![]()
Для парциальных давлений других газов получим такое же выражение, только в знаменателе будет стоять соответствующая молярная масса.
По закону Дальтона давление смеси равно сумме парциальных давлений газов:
![]()
To есть:
![]()
Ответ: 38 кПа.
При электролизе воды образуется кислород O2 и водород Н2. Газы отводят в сосуд объёмом 100 л, поддерживая в нём температуру 300 К. Чему равна масса воды, которая разложилась в результате электролиза, чтобы суммарное давление в сосуде достигло 0,1 атм? Считать, что ничего не взрывается.
Возможное решение:
З апишем
уравнение
Менделеева-Клапейрона для
каждого газа:
апишем
уравнение
Менделеева-Клапейрона для
каждого газа:
![]()
Где P1 и P2 - парциальные давления кислорода и водорода.
По закону Дальтона давление смеси равно сумме парциальных давлений газов:
![]()
Следовательно, сложив уравнения в системе, получаем:
![]()
где v1 — количество кислорода,
v2 — количество водорода.
При электролизе две молекулы воды дают одну молекулу кислорода и две молекулы водорода:
![]()
то есть, если распалось N молекул воды, то получилось N молекул водорода и N/2 молекул кислорода. Иными словами,
v2 = v, v1= v/2,
где v- количество воды.
Тогда уравнение Менделеева-Клапейрона для смеси будет выглядеть так:
![]()
Откуда,
![]()
Ответ: 4,8 г.
В горизонтальной трубке постоянного сечения, запаянной с одного конца, помещен столбик ртути длиной 15 см, который отделяет воздух в трубке от атмосферного воздуха. Трубку расположили вертикально запаянным концом вниз и нагрели на 60 К. При этом объем, занимаемый воздухом, не изменился. Давление атмосферного воздуха в лаборатории - 750 мм. рт. ст. Какова температура воздуха в лаборатории?
Возможное решение:
Условие механического равновесия столбика ртути определяет давление воздуха в вертикальной трубке:
р = р0 + ρgd,
где р0 + ρgd — давление атмосферы. Здесь H = 750 мм.
Поскольку нагревание воздуха в трубке происходит до температуры Т и первоначального объема, то по уравнению Клапейрона-Менделеева:
![]()
![]()
Отсюда
![]()
Ответ: Tо = 300 К.
В горизонтально расположенной трубке постоянного сечения, запаянной с одного конца, помещен столбик ртути длиной 15 см, который отделяет воздух в трубке от атмосферы. Трубку расположили вертикально запаянным концом вниз. На сколько градусов следует нагреть воздух в трубке, чтобы объём, занимаемый воздухом, стал прежним? Температура воздуха в лаборатории 300 К, а атмосферное давление составляет 750 мм.рт.ст.
Возможное решение:
З апишем
для газа, находящегося внутри трубки,
уравнение
Менделеева-Клапейрона для
двух состояний:
апишем
для газа, находящегося внутри трубки,
уравнение
Менделеева-Клапейрона для
двух состояний:
P1V = vRT1 - когда трубка горизонтальна, и
P 2V
= vRT2
- когда
трубка вертикальна, а воздух в трубке
нагрет до некоторой новой температуры
T.
2V
= vRT2
- когда
трубка вертикальна, а воздух в трубке
нагрет до некоторой новой температуры
T.
По условию объём газа V и количество воздуха ν остаются неизменными.
В горизонтальном положении столбик ртути на воздух никакого влияния не оказывает. Следовательно, давление внутри трубки равно давлению воздуха снаружи, то есть атмосферному:
Р= Ратм
Когда же трубка вертикальна, то к атмосферному давлению добавляется давление столбика ртути:
![]() ,
,
Так как атмосферное давление выражено в мм. ртутного столба, то имеет смысл и давление столбика ртути не считать в Паскалях (как в системе СИ), а также рассчитать в мм. ртутного столба. Тогда
![]()
Поделив второе уравнение Менделеева-Клапейрона на первое, выразим конечную температуру
![]()
![]() .
.
Значит,
![]()
Ответ: 60 К
Р
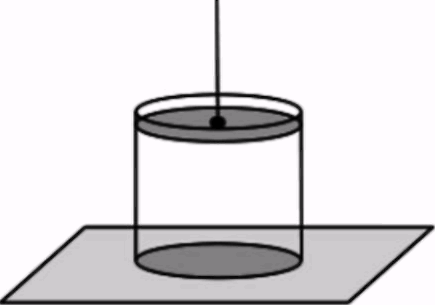 азогретый
сосуд прикрыли поршнем, который с
помощью вертикальной нерастяжимой
нити соединили с потолком. На сколько
процентов от начальной понизится
температура воздуха в сосуде к моменту,
когда сосуд оторвется от поверхности,
на которой он расположен? Масса сосуда
5
кг.
Поршень может скользить по стенкам
сосуда без трения. Площадь дна сосуда
125
см2.
Атмосферное давление 105
Па.
Тепловым расширением сосуда и поршня
пренебречь.
азогретый
сосуд прикрыли поршнем, который с
помощью вертикальной нерастяжимой
нити соединили с потолком. На сколько
процентов от начальной понизится
температура воздуха в сосуде к моменту,
когда сосуд оторвется от поверхности,
на которой он расположен? Масса сосуда
5
кг.
Поршень может скользить по стенкам
сосуда без трения. Площадь дна сосуда
125
см2.
Атмосферное давление 105
Па.
Тепловым расширением сосуда и поршня
пренебречь.
