
- •Содержание
- •1.8.6. Описание явлений переноса в газах……………………………………………………37
- •2.2. Работа в термодинамике…………………………………………………………………..46
- •1. Молекулярно-кинетические представления
- •1.1. Число степеней свободы.
- •1.2. Температура и ее измерение.
- •1.3. Шкалы температур
- •1.4. Уравнение состояния идеального газа
- •1.5. Изопроцессы. Законы Бойля-Мариотта, Гей-Люссака, Шарля.
- •1.6. Закон Дальтона для смеси газов
- •1.7. Основные понятия классической и квантовой статистики
- •1.7.1. Барометрическая формула
- •1.7.2. Распределение Больцмана.
- •1.7.3. Распределение Максвелла.
- •1.7.4. Распределение Максвелла-Больцмана.
- •1.7.5. Опыт Штерна. Скорость частиц вещества
- •1.7.6. Уравнение состояния для газа Ван-дер Вальса.
- •1.8. Явления переноса.
- •1.8.1. Эффективный диаметр молекулы.
- •1.8.2. Средняя длина пробега молекул.
- •1.8.3. Диффузия.
- •1.5.4. Теплопроводность.
- •1.8.5.Вязкость или внутреннее трение
- •1.8.6. Описание явлений переноса в газах
- •2. Основи термодинаміки
- •2.1. Внутренняя энергия идеального газа
- •2.2. Работа в термодинамике.
- •2.3. Количество теплоты
- •2.4. Первое начало термодинамики. Применение для изопроцессов.
- •2.5. Теплоемкость идеального газа
- •2.6. Адиабатическое изменение объёма газа.
- •2.7. Внутренняя энергия газа Ван-дер-Ваальса
- •2.8. Эффект Джоуля – Томсона.
- •2.9. Тепловая машина. Холодильная машина. Кпд.
- •2.10. Цикл Карно. Идеальная тепловая машина
- •2.11. Второе начало термодинамики. Энтропия.
- •2.12. Третий закон термодинамики (тепловой закон Нернста)
- •3. Жидкое состояние
- •Строение жидкостей
- •Явления на границе раздела газа, жидкости и твердого тела
- •Явление смачивания и несмачивания
- •3.4. Давление под изогнутой поверхностью жидкости
- •Капиллярные явления.
- •Кристаллическое состояние
- •Кристаллические и аморфные тела
- •Кристаллическая решетка
- •Физические типы кристаллов
- •4.3. Дефекты кристаллического строения
- •4.4. Тепловое движение в кристаллах.
- •4.6. Теплоемкость кристаллов.
- •5. Фазовые равновесия и превращения
- •5.1. Испарение и конденсация
- •5.2. Насыщенные и ненасыщенные пары
- •5.3. Равновесие жидкости и насыщенного пара
- •5.4. Влажность.
- •5.5. Плавление и кристаллизация
- •5.6. Критическое состояние
- •5.6. Пересыщенный пар и перегретая жидкость. Метастабильное состояние вещества.
- •5.8. Уравнение Клапейрона –Клаузиуса
- •5.9. Диаграмма состояния. Тройная точка.
- •Литература
2. Основи термодинаміки
Термодинамика – раздел физики, изучающий соотношения и превращения теплоты и других форм энергии. В термодинамике имеют дело не с отдельными молекулами, а с макроскопическими телами, состоящими из огромного числа частиц. Эти тела называются термодинамическими системами. В термодинамике тепловые явления описываются макроскопическими величинами – давлением, температурой, объёмом, …, которые не применимы к отдельным молекулам и атомам.
Современную феноменологическую термодинамику принято делить на равновесную (термодинамику равновесных процессов, она же термодинамика квазистатических процессов, она же классическая термодинамика) и неравновесную (термодинамику неравновесных процессов, она же термодинамика необратимых процессов).
Равновесная термодинамика вводит в рассмотрение переменные, такие как внутренняя энергия, температура, энтропия, химический потенциал, а также комбинации перечисленных величин. Все они носят название термодинамических параметров (величин). Предметом рассмотрения классической термодинамики служат связи термодинамических параметров друг с другом и с физическими переменными, вводимыми в рассмотрение в других разделах физики (масса, давление, поверхностное натяжение, сила тока и т. д.). Химические и фазовые реакции (фазовые переходы первого рода) также есть предмет изучения классической термодинамики, поскольку в этом случае рассматриваются связи между массами компонентов системы и их химическими потенциалами. Классическая термодинамика рассматривает такие относительно медленно протекающие (квазистатические) процессы, для которых в каждый данный момент времени систему можно считать находящейся в состоянии термодинамического равновесия (равновесные процессы). Процесс можно считать квазистатическим, если время его протекания много больше времени релаксации рассматриваемой системы.
В неравновесной термодинамике переменные рассматриваются как локальные не только в пространстве, но и во времени, т. е. в её формулы время может входить в явном виде.
2.1. Внутренняя энергия идеального газа
Внутренняя энергия идеального газа равна суммарной кинетической энергии всех молекул, составляющих систему (напомним, что потенциальной энергией взаимодействия молекул идеального газа пренебрегают),
![]() ,
,
где
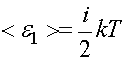 -
средняя кинетическая энергия одной
молекулы, N - число молекул в системе,
i – число степеней свободы.
Число молекул N может
быть найдено из формулы (1.8),
-
средняя кинетическая энергия одной
молекулы, N - число молекул в системе,
i – число степеней свободы.
Число молекул N может
быть найдено из формулы (1.8),
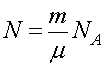 ,
,
где m - масса газа, μ - молярная масса, NA - число Авогадро.
Следовательно, внутренняя энергия идеального газа равна
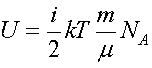 .
.
Учтем, что
![]() -
газовая постоянная. Тогда внутренняя
энергия идеального газа равна
-
газовая постоянная. Тогда внутренняя
энергия идеального газа равна
 (2.1)
(2.1)
Изменение внутренней энергии зависит от изменения температуры, т. е.
 (2.2)
(2.2)
В дифференциальной форме эта формула запишется следующим образом
 (2.3)
(2.3)
Внутренняя энергия системы может
измениться за счет двух различных
процессов: 1). Совершения над системой
работы A/ и 2). Сообщения
количества теплоты
![]() .
Заметим, что работа, совершаемая над
системой внешними силами, и работа,
совершаемая системой против внешних
сил, равны по величине и противоположны
по знаку A/ = - A.
.
Заметим, что работа, совершаемая над
системой внешними силами, и работа,
совершаемая системой против внешних
сил, равны по величине и противоположны
по знаку A/ = - A.
