
1





2





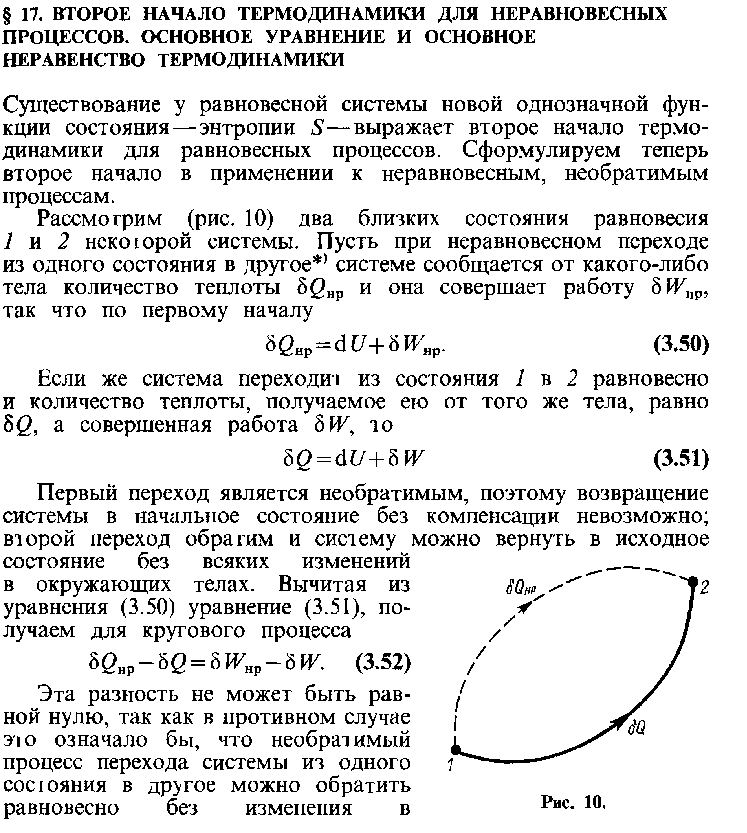
3



4


5



6






7




8




9

![]()



10




11


12





13








14



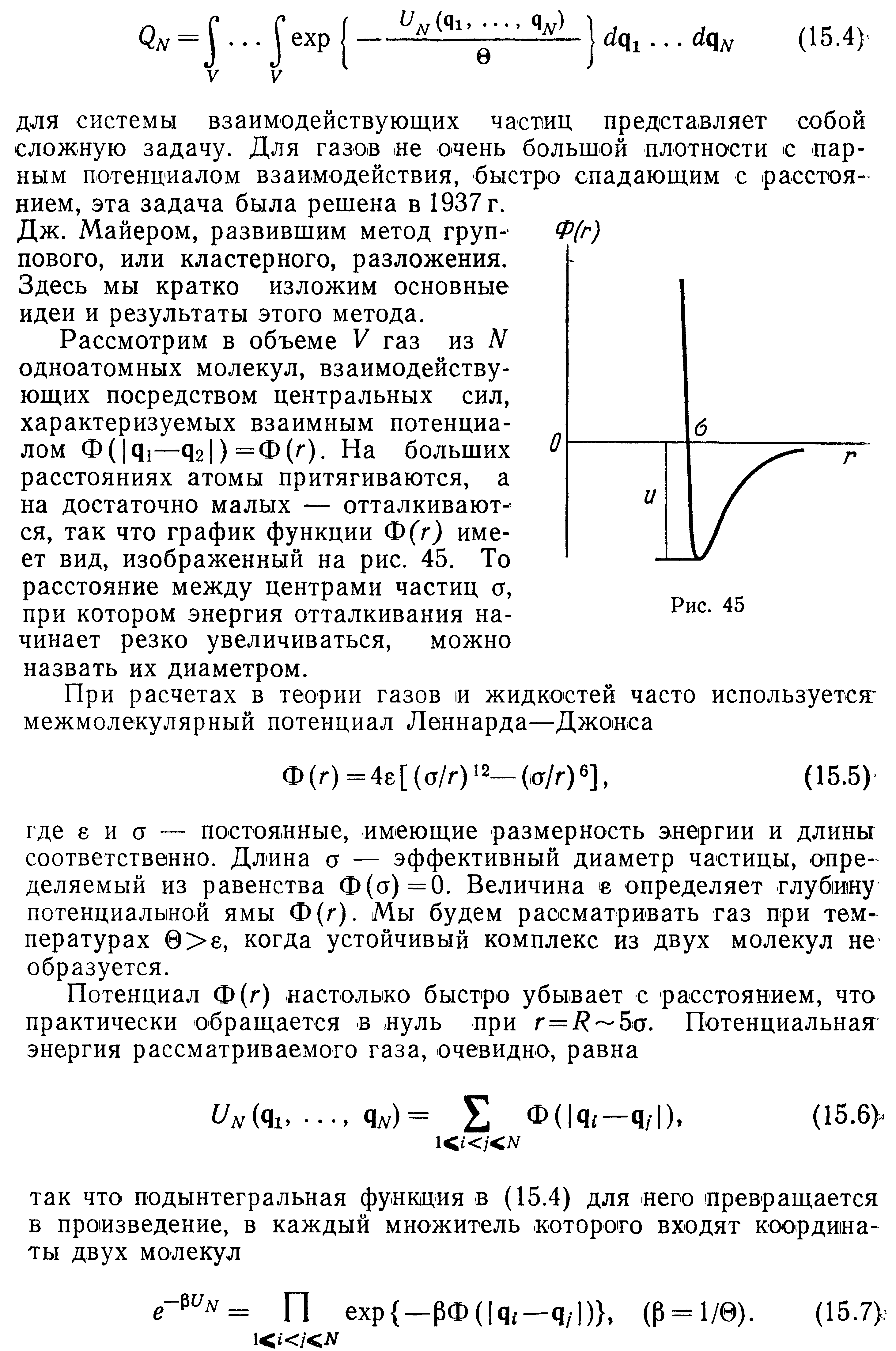
15




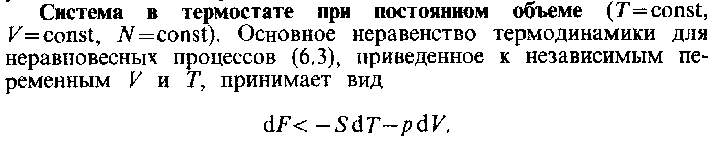


16






17



18


19

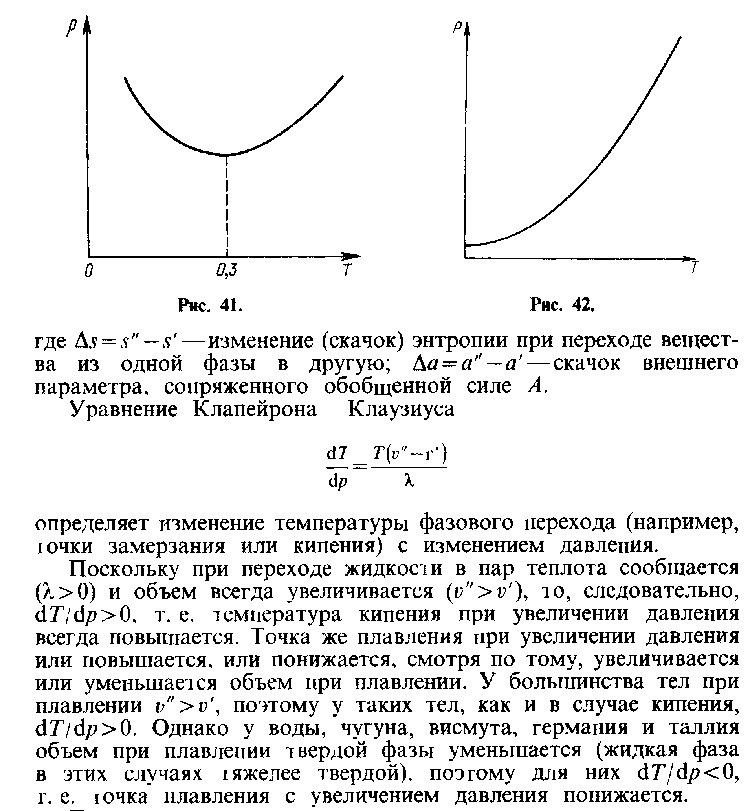



20

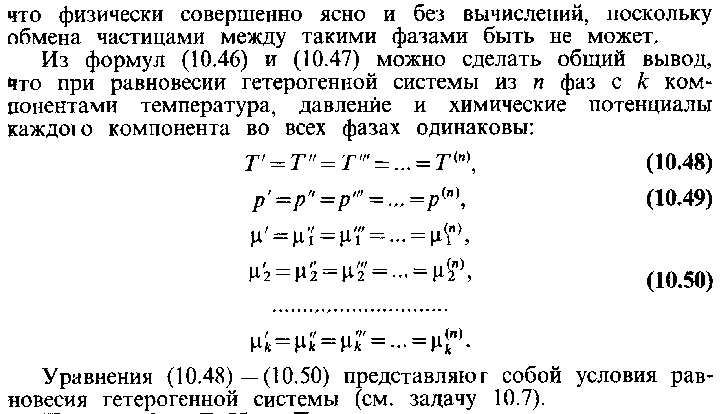



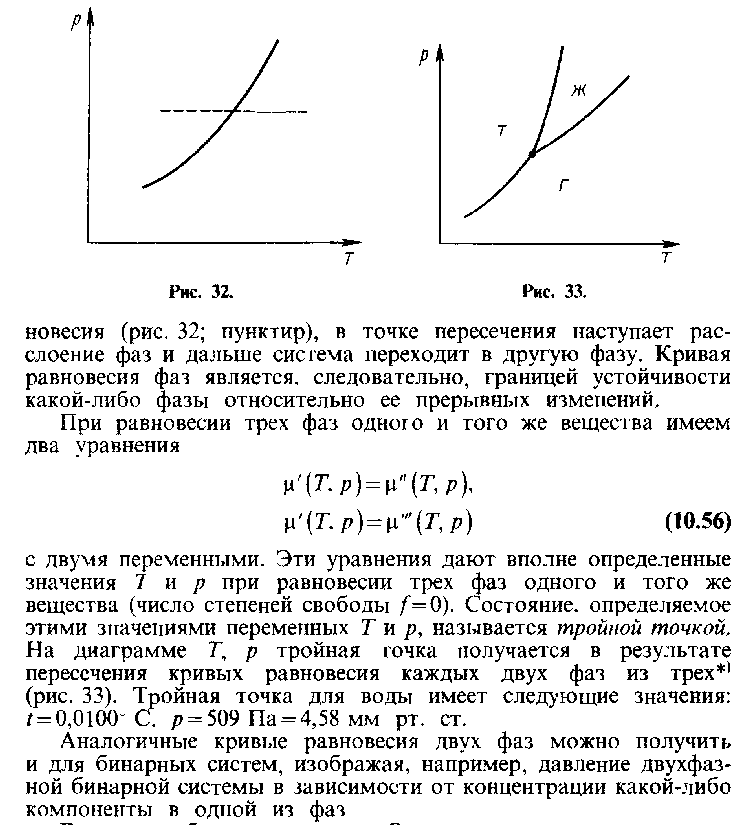
21


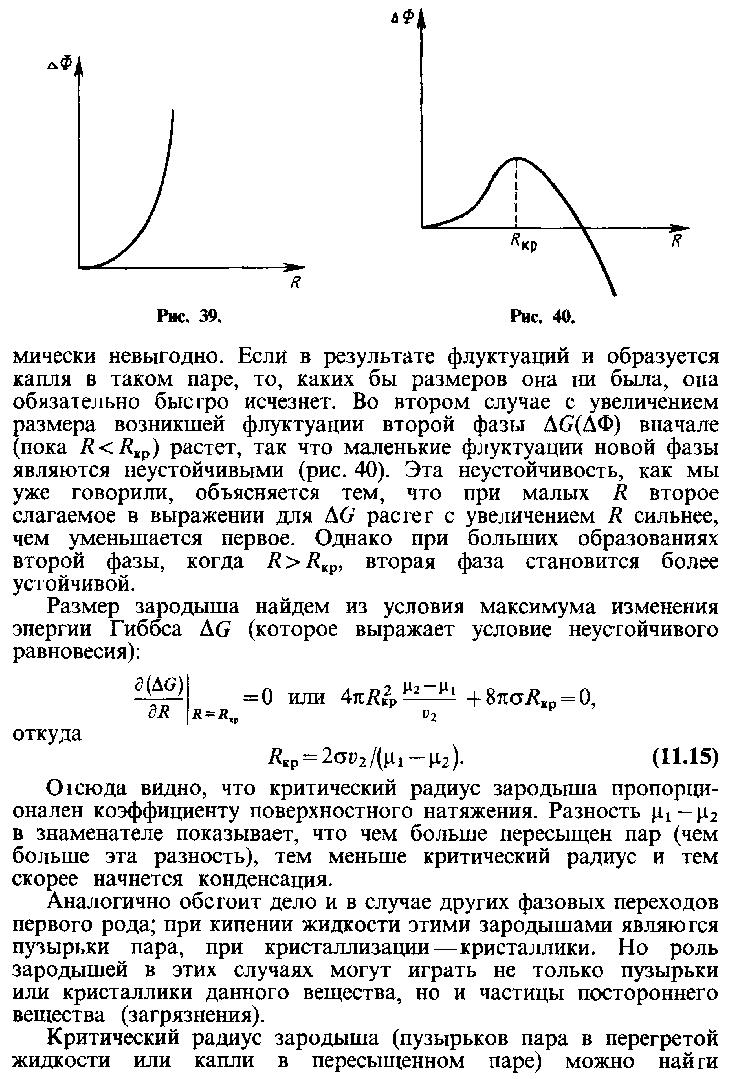

22


23


Теоре́ма Лиуви́лля, названная по имени французского математика Жозефа Лиувилля, является ключевой теоремой в математической физике, статистической физике и гамильтоновой механике. Теорема Лиувилля гласит
Функция распределения гамильтоновой системы постоянна вдоль любой траектории в фазовом пространстве.
Теорема утверждает сохранение во времени фазового объема, или плотности вероятности в фазовом пространстве.
Уравнение Лиувилля
Уравнение
Лиувилля описывает эволюцию во
времени функции
распределения (плотности
вероятности)
гамильтоновой системы в ![]() -мерном
фазовом пространстве (
-мерном
фазовом пространстве (![]() —
количество частиц в системе). Рассмотрим
гамильтонову систему с координатами
—
количество частиц в системе). Рассмотрим
гамильтонову систему с координатами ![]() и
сопряжёнными импульсами
и
сопряжёнными импульсами ![]() ,
где
,
где ![]() ,
, ![]() .
Тогда распределение в фазовом
пространстве
.
Тогда распределение в фазовом
пространстве ![]() определяет
вероятность
определяет
вероятность ![]() того,
что система будет находиться в элементе
объёма
того,
что система будет находиться в элементе
объёма ![]() своего
фазового пространства.
своего
фазового пространства.
Уравнение
Лиувилля описывает эволюцию ![]() во
времени
во
времени ![]() согласно
правилу нахождения полной
производной функции с
учётом несжимаемости потока
в фазовом пространстве:
согласно
правилу нахождения полной
производной функции с
учётом несжимаемости потока
в фазовом пространстве:
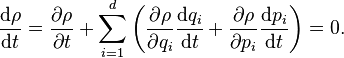
Производные фазовых координат по времени для гамильтоновых систем описываются согласно уравнениям Гамильтона:
![]()
![]()
Простое
доказательство теоремы состоит в
наблюдении, что эволюция ![]() определяется уравнением
неразрывности (непрерывности):
определяется уравнением
неразрывности (непрерывности):
![]()
где ![]() —
скорость перемещения исследуемого
объёма фазового пространства:
—
скорость перемещения исследуемого
объёма фазового пространства:
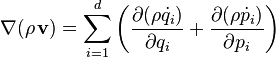
и замечанием, что разность между этим выражением и уравнением Лиувилля определяется только слагаемым описывающим дивергенцию, а именно её отсутствие, что означает отсутствие источников или стоков плотности вероятности:
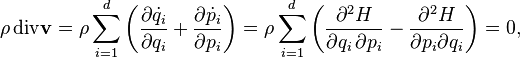
где ![]() — гамильтониан,
и были использованы уравнения
Гамильтона.
Это можно представить как движение
через фазовое пространство «потока
жидкости» точек системы. Теорема
означает, что производная
Лагранжа илисубстанциональная
производная плотности
— гамильтониан,
и были использованы уравнения
Гамильтона.
Это можно представить как движение
через фазовое пространство «потока
жидкости» точек системы. Теорема
означает, что производная
Лагранжа илисубстанциональная
производная плотности ![]() равна
нулю. Это следует из уравнения
непрерывности,
так как поле скоростей
равна
нулю. Это следует из уравнения
непрерывности,
так как поле скоростей ![]() в
фазовом пространстве бездивергентно,
что в свою очередь вытекает из
гамильтоновых уравнений для консервативных
систем.
в
фазовом пространстве бездивергентно,
что в свою очередь вытекает из
гамильтоновых уравнений для консервативных
систем.
Запись через скобку Пуассона
Используя скобку
Пуассона,
имеющее в канонических
координатах ![]() вид
вид
![]()
уравнение Лиувилля для гамильтоновых систем приобретает вид
![]()
Запись с использованием оператора Лиувилля
При помощи оператора Лиувилля
![]()
для гамильтоновых систем уравнение приобретает вид
![]()
24




25





26
Статистический смысл энтропии. Энтропия идеального газа. Флуктуации.
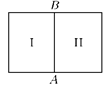
Рассмотрим
закрытый сосуд, разделенный перегородкой
![]() ,
на две одинаковые части
,
на две одинаковые части
![]() и
и
![]() .
Пусть в части сосуда
находится
.
Пусть в части сосуда
находится
![]() молекул идеального газа, а в части
– ни одной. В момент времени
молекул идеального газа, а в части
– ни одной. В момент времени
![]() мгновенно удалим перегородку. Молекулы
из части
начнут переходить в часть
.
В какой-то момент времени количества
молекул в первой и второй частях примерно
выровняются. Так же выровняются потоки
туда и обратно. Мы будем наблюдать
динамическое
равновесие,
а не статистическое.
мгновенно удалим перегородку. Молекулы
из части
начнут переходить в часть
.
В какой-то момент времени количества
молекул в первой и второй частях примерно
выровняются. Так же выровняются потоки
туда и обратно. Мы будем наблюдать
динамическое
равновесие,
а не статистическое.
Статистическое
равновесие
предполагает, что
![]() ,
а в нашем случае это правила почти
никогда не соблюдается. Для такой
системы нужно оперировать не мгновенными
значениями
,
а в нашем случае это правила почти
никогда не соблюдается. Для такой
системы нужно оперировать не мгновенными
значениями
![]() и
и
![]() ,
а их средними значениями, взятыми за
достаточно длительный промежуток
времени:
,
а их средними значениями, взятыми за
достаточно длительный промежуток
времени:
![]() .
Самопроизвольные отклонения чисел
и
,
а так же любых других физических величин
от их средних значений, обусловленные
тепловым движением, называются
флуктуациями.
.
Самопроизвольные отклонения чисел
и
,
а так же любых других физических величин
от их средних значений, обусловленные
тепловым движением, называются
флуктуациями.
Рассмотрим
сосуд всего с одной молекулой идеального
газа. Она равновероятно может попасть
в часть сосуда
или
.
Вероятность такого попадания
![]() .
Введем в сосуд вторую молекулу. Молекулы
идеального газа не взаимодействуют
между собой и их попадания в ту или иную
часть сосуда – события независимые.
Вероятность того, что они обе окажутся
в части сосуда
(по теореме умножения вероятностей):
.
Введем в сосуд вторую молекулу. Молекулы
идеального газа не взаимодействуют
между собой и их попадания в ту или иную
часть сосуда – события независимые.
Вероятность того, что они обе окажутся
в части сосуда
(по теореме умножения вероятностей):
![]() .
Если в сосуде
молекул, то вероятность их общего
попадания в часть
будет
.
Если в сосуде
молекул, то вероятность их общего
попадания в часть
будет
![]() .
Если полный объем сосуда
.
Если полный объем сосуда
![]() ,
то вероятность попадания отдельной
молекулы идеального газа в некоторый
объем
,
то вероятность попадания отдельной
молекулы идеального газа в некоторый
объем
![]() ,
выделенный из общего объема, равна
,
выделенный из общего объема, равна
![]() .
Вероятность того, что в
окажутся
молекул, равна
.
Вероятность того, что в
окажутся
молекул, равна
![]() .
.
Предположим,
что между энтропией
![]() и вероятностью
и вероятностью
![]() есть связь,
выражающаяся формулой
есть связь,
выражающаяся формулой
![]() ,
где
,
где
![]() – одна и та
же для всех тел. Рассмотрим две независимые
подсистемы в состояниях с вероятностями
– одна и та
же для всех тел. Рассмотрим две независимые
подсистемы в состояниях с вероятностями
![]() и
и
![]() .
Энтропии этих состояний –
.
Энтропии этих состояний –
![]() и
и
![]() .
Объединим подсистемы в систему и
обозначим вероятность ее состояния
через
.
Объединим подсистемы в систему и
обозначим вероятность ее состояния
через
![]() ,
а энтропию через
,
а энтропию через
![]() .
Т.к. подсистемы независимы, то
.
Т.к. подсистемы независимы, то
![]() ,
значит
,
значит
![]() .
Учтем, что энтропия
сложной системы должна быть равна сумме
энтропий составляющих ее независимых
подсистем
.
Учтем, что энтропия
сложной системы должна быть равна сумме
энтропий составляющих ее независимых
подсистем
.
Из этого следует, что
![]() .
Предположим,
что переменные
и
изменяются
так, что
.
Предположим,
что переменные
и
изменяются
так, что
![]() ,
тогда
,
тогда
![]() .
Продифференцируем оба выражения и
получим:
.
Продифференцируем оба выражения и
получим:
![]() ,
при условии
,
при условии
![]() .
После почленного деления –
.
После почленного деления –
![]() .
.
Т.к. в левой и правой частях разные , то можно сделать вывод, что функция
![]()
не
изменяется при изменении аргумента.
Это значит она является некой
универсальной постоянной
(обозначим ее через
![]() ),
одной и той же для всех тел.
),
одной и той же для всех тел.
![]()
![]()
![]()
![]() .
.
Подставим последнее соотношение в уравнение и получим
![]() ,
,
откуда
![]() .
.
Значит
![]() – уравнение
Больцмана.
– уравнение
Больцмана.
Пусть
![]() и
и
![]() – объемы моля газа в начальном и конечном
состоянии при одной и той же температуре.
Отношения вероятностей найдем по
формуле
,
поочередно предположив:
– объемы моля газа в начальном и конечном
состоянии при одной и той же температуре.
Отношения вероятностей найдем по
формуле
,
поочередно предположив:
![]() ,
,
![]() .
Далее найдем разность энтропий
.
Далее найдем разность энтропий
![]() .
.
Из
определения энтропии известно, что
если теплоемкость
![]() не зависит от температуры, то
не зависит от температуры, то
![]() ,
,
тогда
![]() .
.
Сравнивая
два уравнения для
![]() ,
получим
,
получим
![]() – постоянная
Больцмана.
– постоянная
Больцмана.
27


28






29


30



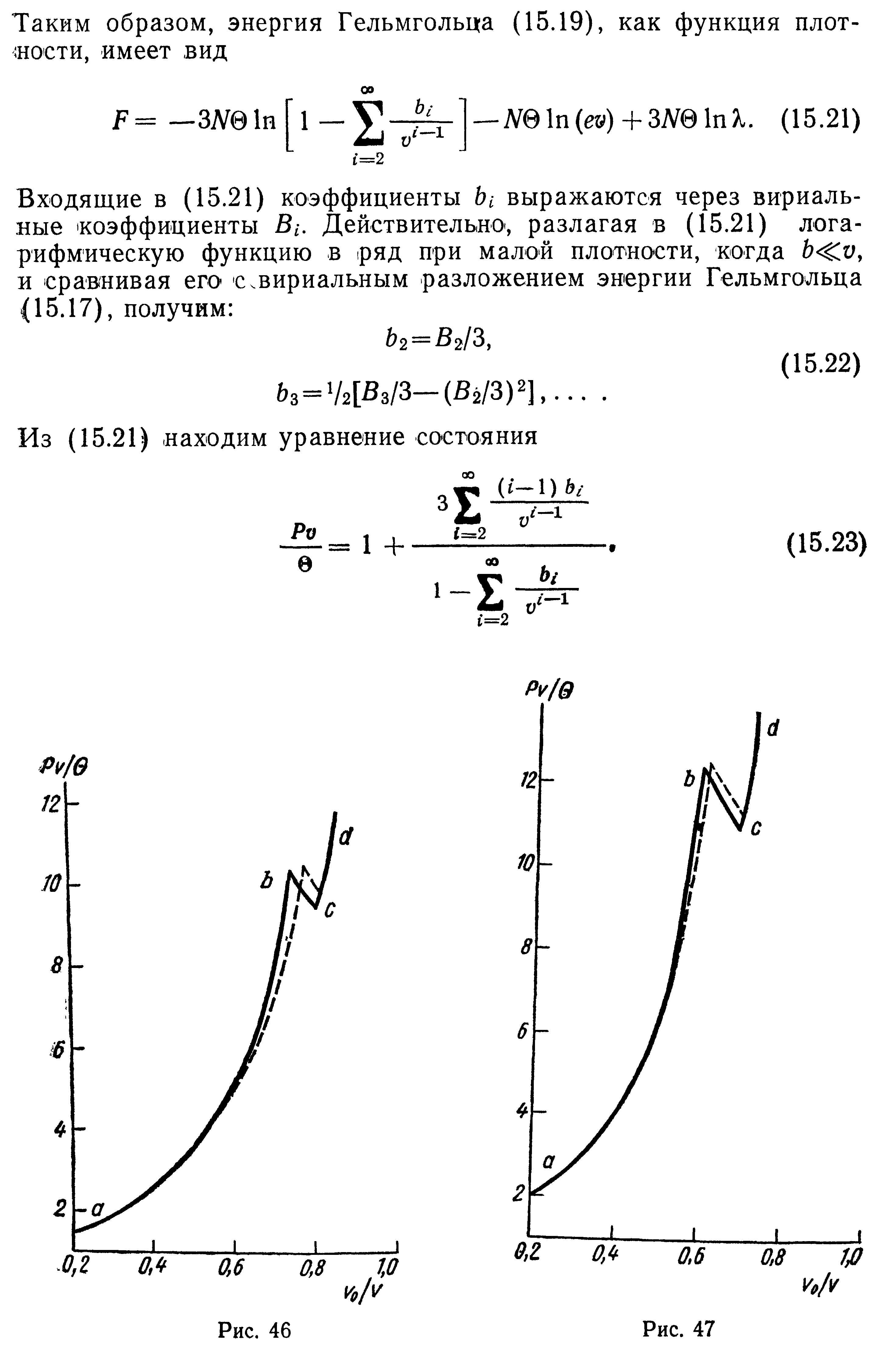



31



32,33
