
- •Курс “ технологія конструкційних матеріалів і матеріалознавство” зміст курсу
- •Глава I Будова металів
- •§ 1. Матеріалознавство як наука про властивості металів і сплавів.
- •§ 2. Історія розвитку науки.
- •§ 3. Класифікація металевих і
- •§ 4. Методи дослідження металів і сплавів.
- •§ 5. Типи зв'язків у металевих тілах.
- •§ 6. Атомно-кристалічна будова металів.
- •§ 7. Анізотропія властивостей металів.
- •§ 8. Особливості кристалічної будови реальних кристалів.
- •§ 8. Дифузія.
- •§ 9. Кристалізація металів.
- •§ 10 Механізм процесу кристалізації.
- •§ 11. Число центрів кристалізації й швидкість
- •§ 12. Немимовільна кристалізація.
- •§ 13. Будова металевого злитка.
- •§ 14. Аллотропия.
- •§ 15. Поліморфні перетворення.
- •Глава II
- •§ 1. Сплав, система, компонент, фаза.
- •§ 2. Фази в металевих сплавах.
- •§ 3. Механічні суміші.
- •§ 4. Правило фаз.
- •§ 5. Діаграми стану подвійних сплавів.
- •§ 6. Методика побудови діаграм стану.
- •§ 7. Правило відрізків.
- •§8. Діаграма стану другого типу
- •§ 9. Діаграма стану III типу (для випадку обмеженої розчинності компонентів у твердому стані)
- •§10. Діаграма стану VI типу для сплавів,
- •§11. Діаграма стану V типу для сплавів, компоненти
- •§12. Зв'язок між діаграмами стану,
- •§13. Поняття про діаграми стану
- •Глава III Залізо і його сплави
- •§ 1. Компоненти й фази в системі залізо-вуглець.
- •§ 2. Діаграма стану залізо-цементит
- •§ 3. Первинна кристалізація сплавів.
- •§ 4 . Вторинна кристалізація залізовуглецевих сплавів.
- •§ 6. Класифікація чавунів.
- •§ 7 . Класифікація углеродистых сталей
§ 7. Правило відрізків.
Для характеристики будови сплаву часто потрібно не тільки якісне, але й кількісне визначення складових. Наприклад, доэвтектические сплави Pb - Sb при кімнатній температурі все будуть мати кристали Pb і эвтектику, але кількість цих складових буде по-різному, тому й властивості їх також будуть різні.
Для кількісного визначення користуються правилом відрізків.
Для визначення кількості рідкої й твердої фази сплаву по діаграмі варто надійти в такий спосіб:
П
 ровести
лінію сплаву заданий^-ний концентрації;
ровести
лінію сплаву заданий^-ний концентрації;При заданій температурі про^-вести горизонтальну лінію (ізотерму, каноду) до пересече-ния з лініями діаграми, ог-раничивающими дану обла-сть;
Знайти крапки перетинання з-терми з лініями діаграми. Визначити сполука рідкої й твердої фази.
4. Співвідношення між рідкою й твердою частинами сплаву буде назад пропорційно відрізкам, на які лінія сплаву ділить ізотерму:
![]() =
=![]()
5. Тоді кількість твердої фази визначається по формулі:
![]() =
=![]() ,
,
а кількість рідкої фази:
![]() =
=![]()
![]() =100%
=100%
§8. Діаграма стану другого типу
(для випадку повної взаємної розчинності)
Ця діаграма характерна для сплавів з необмеженою розчинністю компонентів як у рідкому, так і у твердому стані. Для цих сплавів характерне утворення необмежених твердих розчинів.
Рис.

Лінія
АmВ – лінія ліквідус, лінія АnВ – солідус.
Вище лінії АmВ всі сплави перебувають
у рідкому стані. Між лініями ліквідус
і солідус всі сплави перебувають у
двофазному стані – ж + кристали твердого
розчину
![]() . Перетворення це відбувається з
виділенням тепла, тому вповільнення
швидкості охолодження на кривій
охолодження. Після затвердіння нижче
т. 2 відбувається охолодження твердого
розчину, що протікає вже більш швидко.
Сполука твердої фази змінюється по
лінії солідус, а рідкої - ліквідус.
. Перетворення це відбувається з
виділенням тепла, тому вповільнення
швидкості охолодження на кривій
охолодження. Після затвердіння нижче
т. 2 відбувається охолодження твердого
розчину, що протікає вже більш швидко.
Сполука твердої фази змінюється по
лінії солідус, а рідкої - ліквідус.
При затвердінні твердих розчинів сплав має дендритна будова. Центральні частини кристала (осі перших порядків), що утворяться при більше високих температурах, будуть найбільш багаті тугоплавким компонентом, а периферійні частини й осі вищих порядків - збагачені менш тугоплавким. Для вирівнювання концентрації по об'єму потрібна дифузія атомів усередині кристалів. Дифузійні процеси в реальних умовах охолодження протікають повільно, тому сполука в різних місцях кристала не встигає вирівнюватися.
Розходження сполуки в тому самому кристалі наз. дендритною або внутрікристалічною ліквацією.
Чим більше відстань між лініями ліквідус і солідус, тим більше можлива дендритна ліквація сплаву.
Дендритну ліквацію можна в значній мірі усунути шляхом нагрівання сплаву у твердому стані до температур отжига, у результаті чого виходить однорідна зерниста структура.
§ 9. Діаграма стану III типу (для випадку обмеженої розчинності компонентів у твердому стані)
Обмежена розчинність найбільше часто зустрічається в металевих сплавах.
При утворенні обмежених твердих розчинів розрізняють два типи діаграм: з эвтектическим перетворенням і з перитектическим.
Діаграма стану сплавів, що утворять обмежені
тверді розчини й эвтектику.
Р ис.
ис.
Лінія АСВ - ліквідус
АДСКВ - солідус
ДСК - эвтектического перетворення
Крапка Д - гранична розчинність компонента В у А
Лінія ДМ - зміна розчинності В у А
Крапка ДО - гранична розчинність А в У
Лінія КN зміна розчинності А в У
Крапка З - крапка эвтектического перетворення
Э![]()
![]()
![]() А(В)
А(В)
![]() В(А)
В(А)
Кристалізація
сплаву I іде подібно кристалізації
сплавів по діаграмі II типу. У результаті
виходить однорідний твердий розчин
А(В).
Кристалізація сплаву III іде аналогічно
кристалізації сплавів по діаграмі I
типу. У результаті сплав має надлишкові
кристали
+
эвтектику
![]() .
.
Розглянемо кристалізацію сплаву II. Від т.1 до т.2 в інтервалі температур з рідини виділяються кристали твердого розчину . У т.2 кристалізація закінчується й від т.2 до т.3 іде охолодження сплаву.
При
температурі т.3 у сплаві починається
вторинна кристалізація.
Внаслідок того, що розчинність У в А
міняється по лінії ДМ, нижче т.3 не може
розчинитися стільки компонента В скільки
його перебуває в сплаві. Ця надлишкова
частина компонента стає розчинником і
утворяться кристали твердого розчину
![]() .
Вторинні кристали, виділяючись із
твердого розчину, розташовуються по
границях зерен
або усередині
самого зерна.
В эвтектике ці вторинні кристали
зливаються з первинними й при
мікродослідженні не виявляються.
.
Вторинні кристали, виділяючись із
твердого розчину, розташовуються по
границях зерен
або усередині
самого зерна.
В эвтектике ці вторинні кристали
зливаються з первинними й при
мікродослідженні не виявляються.
Якщо розчинність компонентів зі зниженням температури не змінюється, то вторинних кристалів не утвориться.
Діаграма стану сплавів, що утворять
обмежені тверді розчини й перитектику.
Утворення твердого розчину можливо не тільки з рідини , а й за допомогою взаємодії рідкої й твердої фаз. Такий процес утворення нової фази наз. перитектическим, а температура, при якій він відбувається – перитектической.
Р
III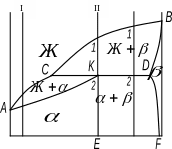 ис.
ис.
Лінія АСВ - лінія ліквідус, АКДВ - солідус, КЕ й ДF - лінія розчинності компонентів(залежно від температури не змінюється).
Розглянемо
кристалізацію перитектического сплаву
I1. У т.1 з рідини починають випадати
кристали твердого розчину
![]() .Концентрація
рідини міняється по лінії СВ, а
-розчину
по лінії ВД. По досягненні температури
т.До відбувається перитектическая
реакція:
.Концентрація
рідини міняється по лінії СВ, а
-розчину
по лінії ВД. По досягненні температури
т.До відбувається перитектическая
реакція:
![]()
![]()
Для сплавів находящихся між крапками С и К перитектическая реакція відбувається при надлишку рідини:
![]()
Тому
після перитектической реакції
кристалізація не закінчується й сплав
має двофазну будову:![]() . При подальшому зниженні температури
з рідини кристалізується твердий розчин
.
Після затвердіння структура сплаву
буде складатися тільки із твердого
розчину
.
. При подальшому зниженні температури
з рідини кристалізується твердий розчин
.
Після затвердіння структура сплаву
буде складатися тільки із твердого
розчину
.
Для сплавів між т.К и т.Д перитектическая реакція проходить при надлишку :
![]()
![]()
У
результаті після затвердіння сплави
будуть мати структуру складається з
![]() .
Розміри й форма кристалів
і
і їхнє взаємне розташування залежить
від умов кристалізації. Найбільше часто
ця структура складається з розвинених
кристалів, що
чергуються,
і й наз. перитектикою.
Перитектическое перетворення характерно
для сплавів заліза з вуглецем, міді із
цинком.
.
Розміри й форма кристалів
і
і їхнє взаємне розташування залежить
від умов кристалізації. Найбільше часто
ця структура складається з розвинених
кристалів, що
чергуються,
і й наз. перитектикою.
Перитектическое перетворення характерно
для сплавів заліза з вуглецем, міді із
цинком.
