
- •6.051301 “Хімічна технологія” денної і заочної форм навчання
- •6.051301 “Хімічна технологія” денної і заочної форм навчання
- •Передмова
- •Вимоги до звіту лабораторних робіт
- •Техніка безпеки в хімічній лабораторії
- •Методи визначення аміаку в газах
- •1. Теоретичні відомості
- •2. Обладнання і хімічні реактиви
- •3 Опис лабораторної установки
- •4. Послідовність виконання роботи і проведення розрахунків
- •5. Техніка безпеки
- •6 Контрольні питання
- •7 Література
- •Конверсія оксиду вуглецю (II)
- •1 Теоретичні відомості
- •2 Обладнання і хімічні реактиви
- •3 Опис лабораторної установки, послідовність виконання роботи і проведення розрахунків
- •Опис приладу
- •Підготовка приладу до роботи
- •Відбір проби на аналіз
- •Проведення аналізу
- •4. Техніка безпеки
- •5. Контрольні питання
- •6. Література
- •Аналітичний контроль нітрозних газів
- •1. Теоретичні відомості
- •2 Обладнання і хімічні реактиви
- •3. Опис лабораторної установки
- •4 Послідовність виконання роботи і проведення розрахунків
- •5 Техніка безпеки
- •6 Контрольні питання
- •7 Література
- •Каталітичне окиснення аміаку
- •1 Теоретичні відомості
- •2 Обладнання і хімічні реактиви
- •3 Опис лабораторної установки
- •4 Порядок виконання роботи і проведення розрахунків
- •5 Техніка безпеки
- •2. Обладнання та хімічні реактиви
- •3. Порядок виконання роботи
- •4 Опрацювання результатів
- •5 Техніка безпеки
- •6 Контрольні питання
- •7 Література
- •Абсорбція оксидів азоту в пінному апараті
- •1 Теоретичні відомості
- •2 Обладнання і хімічні реактиви:
- •3 Опис лабораторної установки
- •4. Порядок виконання роботи і проведення розрахунків
- •5 Техніка безпеки
- •6 Контрольні питання
- •7 Література
- •Аналіз азотної кислоти
- •1 Теоретичні відомості
- •2 Обладнання і хімічні реактиви:
- •3 Опис лабораторної установки
- •4. Техніка безпеки
- •5. Контрольні питання
- •6. Література
- •1 Умови виконання вимірювань
- •2 Приготування розчинів
- •3. Приготування градуювальних розчинів
6 Контрольні питання
Фізико-хімічні основи поглинання оксидів азоту лужними розчинами.
Порядок проведення роботи на лабораторній установці.
Аналітичний контроль нітрозних газів.
Метод розрахунку показників роботи пінного апарата.
7 Література
Атрощенко В.И., Каргин С.И. Технология азотной кислоты. М.: Химия, 1970. С. 175 184.
Пенный режим и пенные аппараты / Под ред. И.П. Мухлёнова и Э.Я. Тароста. Л.: Химия, 1977. с. 12 - 25.
Позин М.Е. Технология минеральных удобрений. 4-е. изд. Л.: Химия, 1974. С. 229 231.
Лабораторна робота № 6
Абсорбція оксидів азоту в пінному апараті
Мета роботи: практично вивчити процес лужного поглинання оксидів азоту в пінному апараті.
1 Теоретичні відомості
Лужним поглиначем найчастіше служить розчин соди, а в результаті реакції одержують NaNO2 і NaNO3. Їх утворення проходить дві стадії: взаємодія оксидів азоту з водою і нейтралізація утворених кислот:
2NO2 + H2O HNO2 + HNO3
2HNO3 + Na2CO3 2NaNO3 + H2O + CO2
2HNO2 + Na2CO3 2NaNO2 + H2O + CO2
2NO2 + NaCO3 NaNO2 + NaNO3 + CO2
Під час взаємодії еквімолекулярної суміші NO і NO2 з розчином соди відбуваються такі реакції:
NO + NO2 + H2O 2HNO2
2HNO2 + Na2CO3 2NaNO2 + H2O + CO2
NO + NO2 + Na2CO3 2NaNO2 + CO2
Швидкість лужного поглинання визначається швидкістю реакції взаємодії оксидів азоту з водою і залежить від співвідношення між NO і NO2. Максимальна швидкість поглинання спостерігається для еквімолекулярної суміші оксидів NO i NO2 .
Коефіцієнт швидкості абсорбції (коефіцієнт абсорбції) оксидів азоту рівномірно зростає з підвищенням концентрації оксидів азоту в газі. Зі зростанням концентрації Na2CO3 у поглиначі коефіцієнт абсорбції падає; максимальна швидкість поглинання спостерігається в середовищі, близькому до нейтрального.
Лужну абсорбцію оксидів азоту можна проводити в абсорбційних апаратах різних типів, баштах з насадкою, механічних скруберах, пінних апаратах тощо.
2 Обладнання і хімічні реактиви:
пінний апарат;
ротаметри для заміру витрат повітря і рідини;
піч трубчаста СУОЛ-0,5;
колба круглодонна з термічно стійкого скла (місткістю 4000 см3), ГОСТ 25336-82Е;
колби мірні ( місткістю 100 см3), ГОСТ 1770-74Е;
фарфорові чашки, ГОСТ 9147-80Е;
перекис водню (3 %-й розчин), ГОСТ 10929-76;
гідроксид натрію (0,1Н розчин та 30 %-й розчин), ГОСТ 4328-77;
кислота саліцилова (10 %-й спиртовий розчин), ГОСТ 624-70;
кислота сірчана (концентрована = 1,84 г/см 3 ),ГОСТ 4204-77;
кислота сірчана (0,1 Н розчин), ГОСТ 4204-66;
метиловий оранжевий (0,1 %-й розчин), ГОСТ 10816-64;
розчин Na2CO3 (10 %-й), ГОСТ 1302-73.
3 Опис лабораторної установки
Суміш NO+NO2 отримують за методикою, описаною в лабораторній роботі № 4. Нітрозні гази змішуються з киснем і проходять через об’єм окислення 2 для отримання еквімолекулярної суміші NO i NO2. У разі отримання еквімолекулярної суміші на стадії окислення аміаку вищезгадана стадія може бути відсутня. Далі суміш направляється у вхідний канал пінного апарата 3 під решітку. Суміш повинна вміщувати приблизно 1 % оксидів азоту. Нітрозні гази проходять через решітку ( на яку подається розчин Na2CO3 з ємності 5 через штуцер для подання розчину) і, контактуючи на ній з розчином соди, поглинаються Na2CO3 у шарі утвореної піни. Відходячи, гази проходять через вихідний штуцер пінного апарата, бризковловлювач 7 і направляються в атмосферу. Надлишок утвореної піни в апараті проходить через посудину для руйнування піни 4, а утворений з піни розчин збирається в резервуарі 8, звідки насосом 10 перекачується в ємність 5. Крани 11 служать для відбору проб газу на вході і виході з пінного апарата. У верхній і нижній частині апарата є штуцери для заміру тиску в апараті за допомогою манометрів 9 (рис. 6.1).
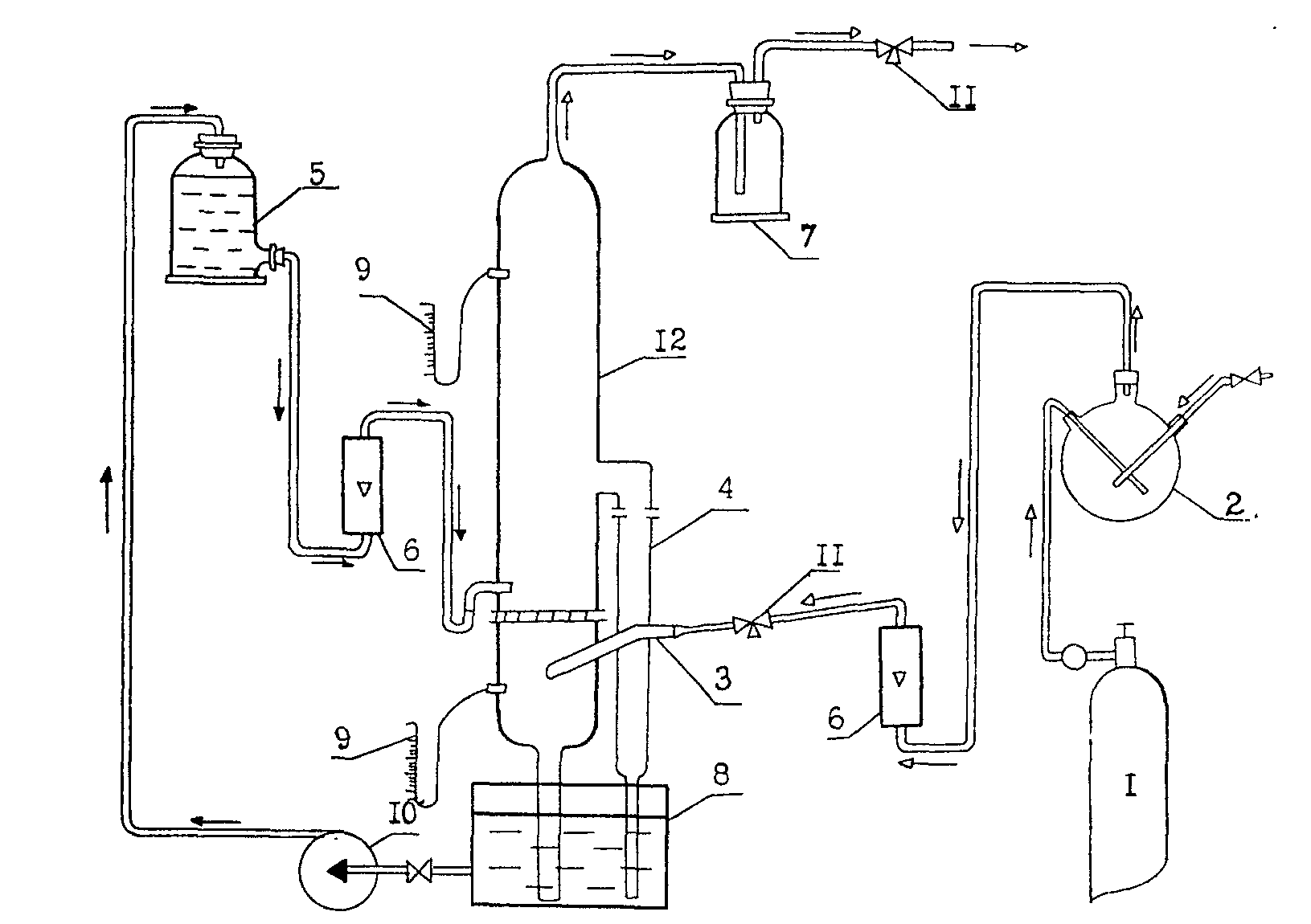
1 – балон із киснем; 2 – об’єм для окиснення; 3 – вхідний канал пінного апарата; 4 – сосуд для руйнування піни; 5 – ємність з поглинальним розчином; 6 – ротаметри; 7 – бризкоуловлювач; 8 – резервуар; 9 – манометри; 10 – насос; 11 – триходові крани; 12 – пінний апарат
Рисунок 6.1 – Схема установки для поглинання газів у пінному апараті
