- •Биологическая роль белков и пептидов: ферментативная, интегративная, иммунологическая, структурная, сократительная, гемостатическая.
- •Методы разделения и очистки белков.
- •Ферменты – белки, выполняющие роль катализаторов.
- •Биологическая роль активных форм кислорода:
- •Гормональная регуляция уровня глюкозы в крови. Гипергликемические гормоны: адреналин, глюкагон, глюкокортикоиды. Гипогликемические: инсулин.
- •Концентрация глюкозы как интегральный показатель углеводного обмена в организме.
- •Липопротеины – транспортная форма липидов. Это комплекс из липидов и апобелков.
- •Липолиз. Бета-окисление высших жирных кислот:
- •Переваривание белков в желудке.
- •Основные пути использования аминокислот в организме.
- •Дезаминирование аминокислот.
- •Глютамин как транспортная форма аммиака. Система глутамин-глутаминаза в клетках печени и почечных канальцев, биороль, связь с образованием конечных продуктов обмена аммиака.
- •Образование катехоламинов. Роль гидроксилирования, декарбоксилирования и метилирования в этом процессе. Биологическая роль катехоламинов.
- •Понятие о нуклеопротеидах, их превращения в желудочно-кишечном тракте. Строение, биологическая роль, особенности обмена мононуклеотидов в организме человека.
- •Регуляция клеточного цикла и репликации. Роль циклинов и белка р53.
- •Вот что говорит Вика.
- •Механизмы регуляции транскрипции. Примеры воздействия на процессы биосинтеза белка лекарственными препаратами.
- •ВитаминВ1 (тиамин). Активная форма витамина. Участие в биохимических реакциях. Проявление недостаточности.
- •В2 (рибофлавин). Активная форма витамина. Участие в биохимических реакциях. Проявление недостаточности.
- •Витамин в5 (никотинамид). Активные формы витамина. Участие в биохимических реакциях. Проявление недостаточности. Фармакологическое действие витамина в5.
- •Витамин в6 (пиридоксин), Витамин в9 (фолиевая кислота) и в12 (цианокобаламин). Активные формы витаминов. Участие в биохимических реакциях. Проявление недостаточности.
- •Витамин с (аскорбиновая кислота). Участие в биохимических реакциях. Проявление недостаточности.
- •Витамин а (ретинол). Роль в процессах светоощущения, обмена эпителия, эндотелия и соединительной ткани. Проявления недостаточности.
- •Белки межклеточных контактов и адгезии. Хемокины.
- •Гистогормоны (гистамин, серотонин, гастрин, секретин, холецистокинин, натрийуретический пептид). Клетки-продуценты, пути передачи сигналов, биологическая роль.
- •Инсулин. Глюкагон. Химическая природа, образование, ткани-мишени. Влияние инсулина на углеводный, белковый и липидный обмены.
- •Глюкокортикоиды. Химическая природа, образование, ткани-мишени. Влияние глюкокортикоидов на углеводный, белковый и липидный обмены.
- •Гормоны щитовидной железы. Химическая природа, образование, ткани-мишени. Регуляция тироксином обмена веществ.
- •Гормональная регуляция репродуктивной функции организма.
- •Основные компоненты внеклеточного матрикса соединительных тканей: коллагеновые волокна, эластиновые волокна, глюкозамингликаны, протеогликаны. Структура и роль.
- •Механизм синтеза и распада коллагена. Промежуточные продукты маркеры резорбции и образования костной ткани.
- •Костная ткань как твердая разновидность соединительной ткани, ее основные функции. Особенности структуры гидроксиапатита и их связь с биологической функцией костной ткани.
- •Понятие об остеомаляции и остеопорозе, возможных причинах их развития.
- •Участие печени в обмене белков.
- •Желчеобразующая функция печени. Состав и функции желчи. Гепатоэнтеральная циркуляция желчных кислот. Биосинтез желчных кислот и их роль.
- •Экзогенные и эндогенные субстраты детоксикации. Реакции гидроксилирования (микросомальная система окисления) и конъюгации.
- •Общая схема регуляции эндотелием адаптивных реакций сосудистой стенки. Роль эндотелия в регуляции структурных изменений сосудистой стенки, ангиогенезе, гемостаза.
- •Оксид азота и супероксид. Пути образования и инактивации. Эндотелин 1. Схема образования, эффекты на тонус сосудов в норме и при повышенной продукции.
- •Метаболические особенности миокарда: механизм сокращения миоцитов, основные энергетические субстраты и пути их утилизации. Роль миоглобина и креатинфосфата в энергетическом обмене миокарда.
- •Эритроциты, место образования и распада. Регуляция эритропоэза эритропоэтином. Особенности метаболизма эритроцитов и структуры их мембран.
- •Обмен железа. Лабораторные показатели дефицита железа в организме. Понятие о физиологической желтухе новорожденных.
- •Механизм адгезии и агрегации тромбоцитов. Фактор Виллебранда: структура, участие в гемостазе. Тромбоксан простациклин: схема синтеза, участие в гемостазе.
- •Связывание с рецептором
- •Модуляция синаптической нейротрансмиссии
- •Интеграция синаптических входов
- •Гамма-аминомасляная кислота
- •Гематоэнцефалический барьер
Гормональная регуляция уровня глюкозы в крови. Гипергликемические гормоны: адреналин, глюкагон, глюкокортикоиды. Гипогликемические: инсулин.
Глюкагон. Образуется в альфа клетках островков Лангерганса поджелудочной железы. Полипептид (29 аминокислотных остатков). Образуется из проглюкагона путём ограниченного протеолиза.
Клетки мишени – печень, жировая ткань, мышцы (чутка).
Действие на углеводный обмен противоположно инсулину (просто поменяйте местами слова стимулирует и подавляет).
Глюкокортикоиды – гормоны, которые выделяются пучковой зоной коры надпочечников, из которых наиболее известен кортизол. О нём и поговорим.
Стероидной природы (холестерол – прегненолон – прогестерон – кортизол).
Ткани мишени – почти все ткани, в основном – мышцы, жировая ткань, печень, почки, лимфатическая ткань. Выделяется в ответ на андренокортикотропный гормон, который выделяется в ответ на кортиколиберин, который выделяется в ответ на стресс.
Транспортная форма – транскортин
Стимулирует глюконеогенез (фосфоенолпируваткарбоксиназы)
Стимулирует распад гликогена (гликогенфосфорилазу)
Адреналин: Стимулирует распад гликогена (гликогенфосфорилазу)
Концентрация глюкозы как интегральный показатель углеводного обмена в организме.
Все углеводы, которые поступают к нам с пищей распадаются либо до глюкозы, либо до других моносахаридов, которые в печени в итоге переходят в глюкозу. Все пути метаболизма глюкозы содержат глюкозу как исходный или как конечный субстрат. Это всё позволяет нам определить глюкозу как главный показатель обмена углеводов.
Глюкозо-6-фосфат – центральный метаболит внутриклеточного обмена глюкозы: как только глюкоза проникает в ткани она сразу же фосфорилируется в глюкозо-6-фосфат под воздействием глюкокиназы (в печени), гексокиназы (во всех остальных клетках). Это обусловлено несколькими причинами: 1. Фосфорилированная глюкоза уже не может выйти из клетки. 2. Поскольку глюкоза переходит в глюкозо-6-фосфат, то количество глюкозы в клетке падает, что создаёт хороший градиент для диффузии глюкозы в клетку. 3. Реакция превращения глюкозы в глюкозо-6-фосфат ингибируется АТФ. Значит, если у нас много АТФ, то энергия как бы и не нужна, тогда концентрация глюкозы в клетке и в крови выравнивается и глюкоза перестаёт поступать в клетку.
Возможные причины гипергликемии: переел глюкозы, диабет обоих типов, избыток глюкагона или глюкокортикоидов.
Гипогликемии: голодание, недостаток глюкагона, избыток инсулина, физические нагрузки интенсивные.
Нарушения углеводного обмена при сахарном диабете: поскольку углеводы не депонируются в ткани, то нарушается синтез гликогена в печени и мышцах, а также замедляется их переход в жиры. На самом деле, поскольку глюкоза не попадает в ткани, страдают любые пути ката- или анаболизма углеводов.
Механизм развития нарушений: есть два типа диабета – инсулинзависимый – когда нарушена выработка инсулина бета клетками островков Лангерганса поджелудочной железы (воспаления, аутоимунные реакции), и инулиннезависимый – когда инсулин нормально вырабатывается, но его воздействия на клетку нарушено.(дефекты рецепторов)
Лабораторные показатели: Тест толерантности к глюкозе, определение гликозилированного гемоглобина, определение количества инсулина и С-пептида в моче, по количеству альбумина в моче (альбуминурии), определение количества кетоновых тел.
Неэнзиматическая гликация – неферментное, ковалентное встраивание глюкозы или фруктозы в структуру мембраны белков при гипергликемии. В норме происходит в ничтожно малых количествах, при гипергликемии гликации подвергается всё и вся.
Роль в механизме развития осложнений гипергликемии: образуются гликозилированный гемоглобин (в принципе это не особо беда, но гемоглобин уже свою функцию не выполняет), гликозилированные кристаллины (белки хрусталика, из-за этого возникает катаракта), гликозилирование белков мембран сосудов, из-за чего развиваются ангиопатии, нефропатии и ретинопатии.
Клинико-диагностическое значение исследования фруктозамина и гликозилированного гемоглобина: ну, раз гликозилирование белков наблюдается при гипергликемии, значит мы может диагностировать гипергликемию определяя фруктозами (гликозилированный альбумин) и гликозилированный гемоглобин в крови. Причём гемоглобин живёт от 90 до 120 дней. Значит у нас уже 3 месяца как может и не быть гипергликемии, а гемоглобин останется. Про это любят задавать вопрос, так что будьте во всеоружии.
Чё это? Становление процессов переваривания в онтогенезе… Врождённая недостаточность…. Обмен глюкозамингликанов… А-а-а, для студентов педиатрического факультета! Ну что ж чуваки, облом, не судьба, не повезло, не фортануло.
Классификация, строение и биологическая роль липидов.
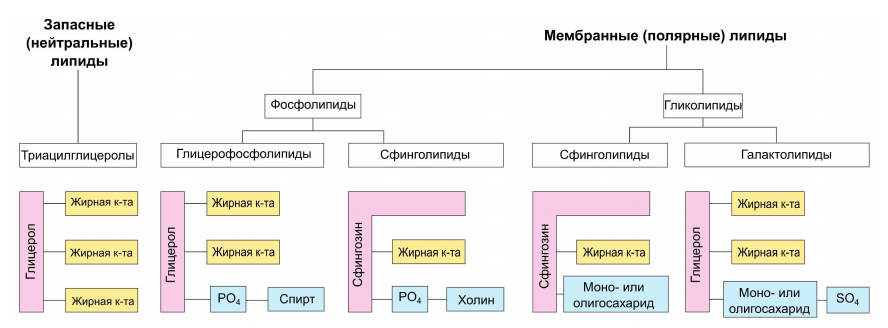
Триацилглицериды – депонируются в жировой ткани. Являются энергетическим запасом организма.
Фосфолипиды – являются структурной основой мембран клеток и мицелл.
Сфингомиелины – основной компонент миелина в нервной ткани, также субстрат для синтеза церамидов и сфингозинов, регулирующих метаболизм.
Гликолипиды (цереброзиды и ганглиозиды) – содержатся в нервной ткани, где отвечают за образование межклеточных контактов.
Переваривание липидов в желудочно-кишечном тракте. Роль желчных кислот и панкреатических липаз: желчные кислоты эмульгируют жиры, а липазы разрушают сложные липиды до более простых.
Значение эмульгирования в переваривании триацилглицеридов: суть в том, что жиры липофильмы и гидрофобны, и потому в водной среде стремятся образовывать крупные капли. Эти крупные капли переваривать можно, но сложно. Желчные кислоты как бы разбивают эти крупные капли на множество мелких, что увеличивает площадь контакта между липидами и ферментами, благодаря чему переваривание проходит хорошо.
Продукты
переваривания триацилглицеринов,
фосфолипидов, эфиров холестерина:
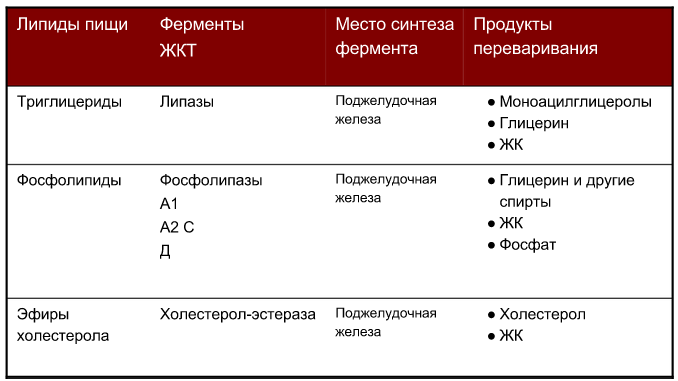
Нарушения переваривания липидов в желудочно-кишечном тракте: 1. Нарушение секреции желчи. При этом липиды не эмульгируются и поэтому хуже перевариваются и всасываются, из-за чего возникает стеаторея.
2. Нарушение секреции сока поджелудочной железы, что также приводит к стеаторее.
Стеаторея – Повышенной содержание жиров в кале (выше 5 %). При стеаторее нарушается всасывание жирорастворимых витаминов и незаменимых жирных кислот, также нарушается переваривание веществ нелепиднйо природы, поскольку жир обволакивает эти вещества, не давая ферментам расщепить их.
Всасывание продуктов переваривания липидов в тонком кишечнике. Продукты распада жиров (жирные кислоты, 2-моноглицериды, холестерол) при участии солей желчных кислот образуют смешанные мицеллы. Когда мицеллы сближаются с щеточной каёмкой клеток кишечника – липидные компоненты мицелл диффундируют через мембрану. Таким же образом всасываются жирорастворимые витамины и сами соли желчных кислот.
Ресинтез липидов в энтероцитах и его биологическое значение. Всосавшиеся жирные кислоты и 2-моноацилглицерины подвергаются ресинтезу. Вначале ЖК активируются путём связывания с КоА (фермент тиокиназа), затем образовавшийся таким образом ацил-КоА участвует в реакции этерификации 2-моноацилглицерола с образованием вначале диацилглицерола, а потом и триацилглицерола. Реакцию катализирует ацилтрансферазы. Ресинтез нужен нам для того, чтобы всосавшиеся липиды стали «своими».
Гепатоэнтеральная циркуляция желчных кислот. Из холестерина образуются глико(тауро)хенодезоксихолевая и глико(тауро)холевая кислоты, которые первичные желчные кислоты. В кишечнике, под воздействием микрофлоры, первичные желчные кислоты преобразуются во вторичные желчные кислоты (дезоксихолевая и литохолевая кислоты). 95% вторичных желчных кислот всасываются и по воротной вене возращаются в печень, где достраиваются до первичных и снова идут в ход. 5% выводятся с калом.
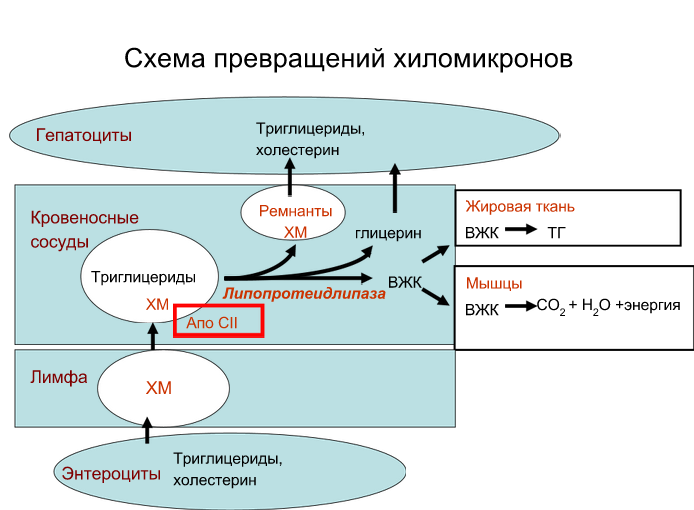
Основные пути превращения хиломикронов.