
- •Биологическая роль белков и пептидов: ферментативная, интегративная, иммунологическая, структурная, сократительная, гемостатическая.
- •Методы разделения и очистки белков.
- •Ферменты – белки, выполняющие роль катализаторов.
- •Биологическая роль активных форм кислорода:
- •Гормональная регуляция уровня глюкозы в крови. Гипергликемические гормоны: адреналин, глюкагон, глюкокортикоиды. Гипогликемические: инсулин.
- •Концентрация глюкозы как интегральный показатель углеводного обмена в организме.
- •Липопротеины – транспортная форма липидов. Это комплекс из липидов и апобелков.
- •Липолиз. Бета-окисление высших жирных кислот:
- •Переваривание белков в желудке.
- •Основные пути использования аминокислот в организме.
- •Дезаминирование аминокислот.
- •Глютамин как транспортная форма аммиака. Система глутамин-глутаминаза в клетках печени и почечных канальцев, биороль, связь с образованием конечных продуктов обмена аммиака.
- •Образование катехоламинов. Роль гидроксилирования, декарбоксилирования и метилирования в этом процессе. Биологическая роль катехоламинов.
- •Понятие о нуклеопротеидах, их превращения в желудочно-кишечном тракте. Строение, биологическая роль, особенности обмена мононуклеотидов в организме человека.
- •Регуляция клеточного цикла и репликации. Роль циклинов и белка р53.
- •Вот что говорит Вика.
- •Механизмы регуляции транскрипции. Примеры воздействия на процессы биосинтеза белка лекарственными препаратами.
- •ВитаминВ1 (тиамин). Активная форма витамина. Участие в биохимических реакциях. Проявление недостаточности.
- •В2 (рибофлавин). Активная форма витамина. Участие в биохимических реакциях. Проявление недостаточности.
- •Витамин в5 (никотинамид). Активные формы витамина. Участие в биохимических реакциях. Проявление недостаточности. Фармакологическое действие витамина в5.
- •Витамин в6 (пиридоксин), Витамин в9 (фолиевая кислота) и в12 (цианокобаламин). Активные формы витаминов. Участие в биохимических реакциях. Проявление недостаточности.
- •Витамин с (аскорбиновая кислота). Участие в биохимических реакциях. Проявление недостаточности.
- •Витамин а (ретинол). Роль в процессах светоощущения, обмена эпителия, эндотелия и соединительной ткани. Проявления недостаточности.
- •Белки межклеточных контактов и адгезии. Хемокины.
- •Гистогормоны (гистамин, серотонин, гастрин, секретин, холецистокинин, натрийуретический пептид). Клетки-продуценты, пути передачи сигналов, биологическая роль.
- •Инсулин. Глюкагон. Химическая природа, образование, ткани-мишени. Влияние инсулина на углеводный, белковый и липидный обмены.
- •Глюкокортикоиды. Химическая природа, образование, ткани-мишени. Влияние глюкокортикоидов на углеводный, белковый и липидный обмены.
- •Гормоны щитовидной железы. Химическая природа, образование, ткани-мишени. Регуляция тироксином обмена веществ.
- •Гормональная регуляция репродуктивной функции организма.
- •Основные компоненты внеклеточного матрикса соединительных тканей: коллагеновые волокна, эластиновые волокна, глюкозамингликаны, протеогликаны. Структура и роль.
- •Механизм синтеза и распада коллагена. Промежуточные продукты маркеры резорбции и образования костной ткани.
- •Костная ткань как твердая разновидность соединительной ткани, ее основные функции. Особенности структуры гидроксиапатита и их связь с биологической функцией костной ткани.
- •Понятие об остеомаляции и остеопорозе, возможных причинах их развития.
- •Участие печени в обмене белков.
- •Желчеобразующая функция печени. Состав и функции желчи. Гепатоэнтеральная циркуляция желчных кислот. Биосинтез желчных кислот и их роль.
- •Экзогенные и эндогенные субстраты детоксикации. Реакции гидроксилирования (микросомальная система окисления) и конъюгации.
- •Общая схема регуляции эндотелием адаптивных реакций сосудистой стенки. Роль эндотелия в регуляции структурных изменений сосудистой стенки, ангиогенезе, гемостаза.
- •Оксид азота и супероксид. Пути образования и инактивации. Эндотелин 1. Схема образования, эффекты на тонус сосудов в норме и при повышенной продукции.
- •Метаболические особенности миокарда: механизм сокращения миоцитов, основные энергетические субстраты и пути их утилизации. Роль миоглобина и креатинфосфата в энергетическом обмене миокарда.
- •Эритроциты, место образования и распада. Регуляция эритропоэза эритропоэтином. Особенности метаболизма эритроцитов и структуры их мембран.
- •Обмен железа. Лабораторные показатели дефицита железа в организме. Понятие о физиологической желтухе новорожденных.
- •Механизм адгезии и агрегации тромбоцитов. Фактор Виллебранда: структура, участие в гемостазе. Тромбоксан простациклин: схема синтеза, участие в гемостазе.
- •Связывание с рецептором
- •Модуляция синаптической нейротрансмиссии
- •Интеграция синаптических входов
- •Гамма-аминомасляная кислота
- •Гематоэнцефалический барьер
Биологическая роль активных форм кислорода:
Физиологический оксидативный стресс: возникает при временной гипоксии, например в душном помещении. Проходят при нормализации концентрации кислорода в окружающей среде.
Патологический оксидативный стресс: возникает в следствии различных вредных воздействий (радиация, чрезмерной УФ излучение), при этом антиоксидантная система не справляется со свободными радикалами, что приводит к структурным и функциональным нарушениям.
Механизм повреждающего действия: нужно знать и иметь ввиду, что свободным радикалам очень не нравятся неспаренные электроны на их внешней мембране, и она стремятся во что бы то ни стало ликвидировать эту неспаренность, вытаскивая электроны у других молекул. Та молекула, у которой отобрали электрон, сама становится свободным радикалом и отбирает электрон ещё у чего-нибудь. Таким образом запускается цепная реакцию и могут повреждать всякие ферменты, липиды мембран или даже ДНК. Вот повредится у вас ДНК и появится раковая клетка – чё вы будете тогда делать?
Свободно-радикальное окисление – одноэлектронное окисление.
Метаболические и ферментативные антиоксиданты: Метаболические антиоксиданты – неферментные вещества, которые при взаимодействии со свободным радикалом восстанавливают его, но сами становятся свободными радикалами, которые нужно обезвредить. К таким антиоксидантам относятся токоферол, аскорбиновая кислота,
Ферментативные антиоксиданты – ферменты, которые способны нейтрализовать свободные радикалы и сами при этом не становиться ими.
Супероскиддисмутаза – фермент, содержащий в качестве кофермента двухвалентную медь. Нейтрализует кислородный супероксид.
Каталаза – содержит железо, нейтрализует перекись водорода.
Глутатионпероксидаза – нейтрализует перекись водорода, гидроксильный радикал, гидроперекиси липидов.
Строение углеводов: углеводы – органические соединения, содержащие несколько гидроксильных групп и одну карбонильную.
Биологическая роль: пластическая (гетерополисахариды) и энергетическая. Классификация: моносахариды – производные многоатомных спиртов, содержащие карбоксильную группу. Делятся на кетозы (содержат кетонную группу – рибулоза и фруктоза) и альдозы (содержат альдегидную группу – галактоза, рибоза, глюкоза, манноза и тд.). Олигосахариды – содержат от 2 до 10 остатков моносахаридов, соединённых гликозидной связью. К олигосахаридам относятся ,в частности, дисахариды – сахароза (глюкоза и фруктоза с альфа-бета 1,2 гликозидной связью), лактоза (галактоза и глюкоза бета 1,4, связь), мальтоза (две глюкозы альфа1,4 связь), изомальтоза (две глюкозы альфа1,6 связь). Полисахариды – больше 10 остатков моносахаридов. Различают гомополисахариды (все мономеры одинаковы) и гетерополисахариды (мономеры различны). Самые известные – крахмал – резервный гомополисахарид растений. Состоит из глюкозы. В нём различают амилозу – прямую цепь с альфа 1,4 связью, и амилопектин – места ветвления крахмала с альфа1,6 связью в месте ветвления. (дальше снова альфа 1,4 связь); Целлюлоза – структурный гомополисахарид растений. Состоит из глюкозы с бета 1,4 гликозидной связью. Не расщепляется в ЖКТ, но нужен для нормального пищеварения; Гликоген. Тоже самое что и крахмал, только встречается у животных и ветвится чаще.
Переваривание углеводов в желудочно-кишечном тракте. Пищеварительные ферменты: место синтеза, субстрат, гидролизуемые химические связи, продукты переваривания.

Механизмы всасывания продуктов переваривания углеводов в желудочно-кишечном тракте:
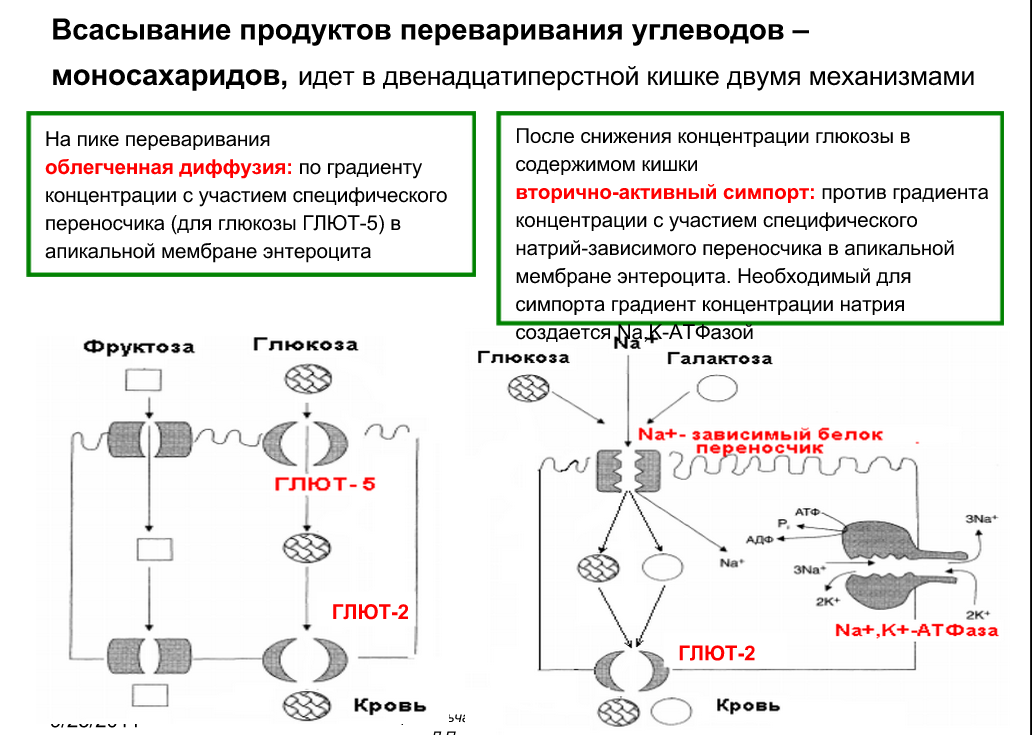
Гликоген. Строение, биологическая роль: животный гомополисахарид, состоит из глюкозы, включает в себя амилозу – неразветлённый полисахарид из глюкозы с альфа 1,4 гликозидной связью, и амилопектина – ветвления гликогена, который в месте ветвления имеют альфа 1,6 связь. Ветвится примерно каждые 10 мономеров. Гликоген есть во многих тканях, но известен своим пребыванием в скелетных мышцах и печени. Роль – резервный полисахарид (позволяет нам хранить глюкозу).
Синтез
и распад гликогена, ключевые ферменты,
регуляция процесса: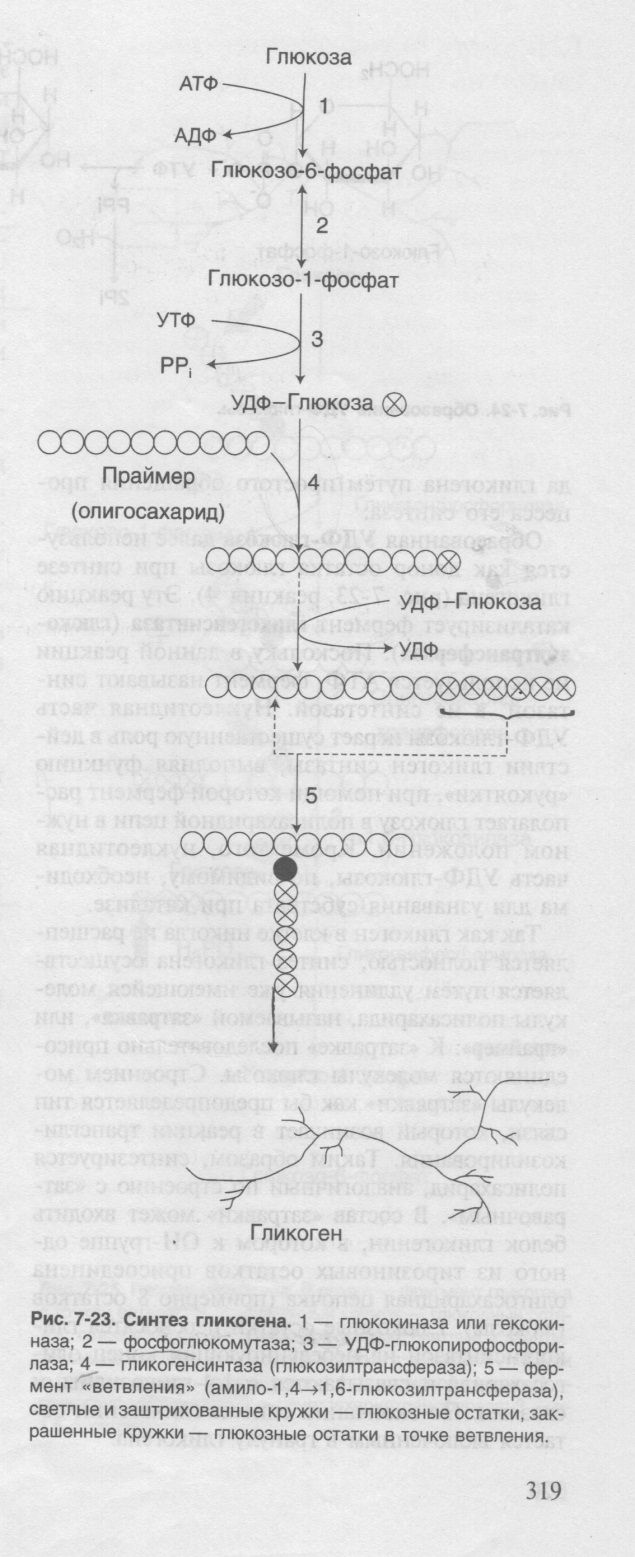
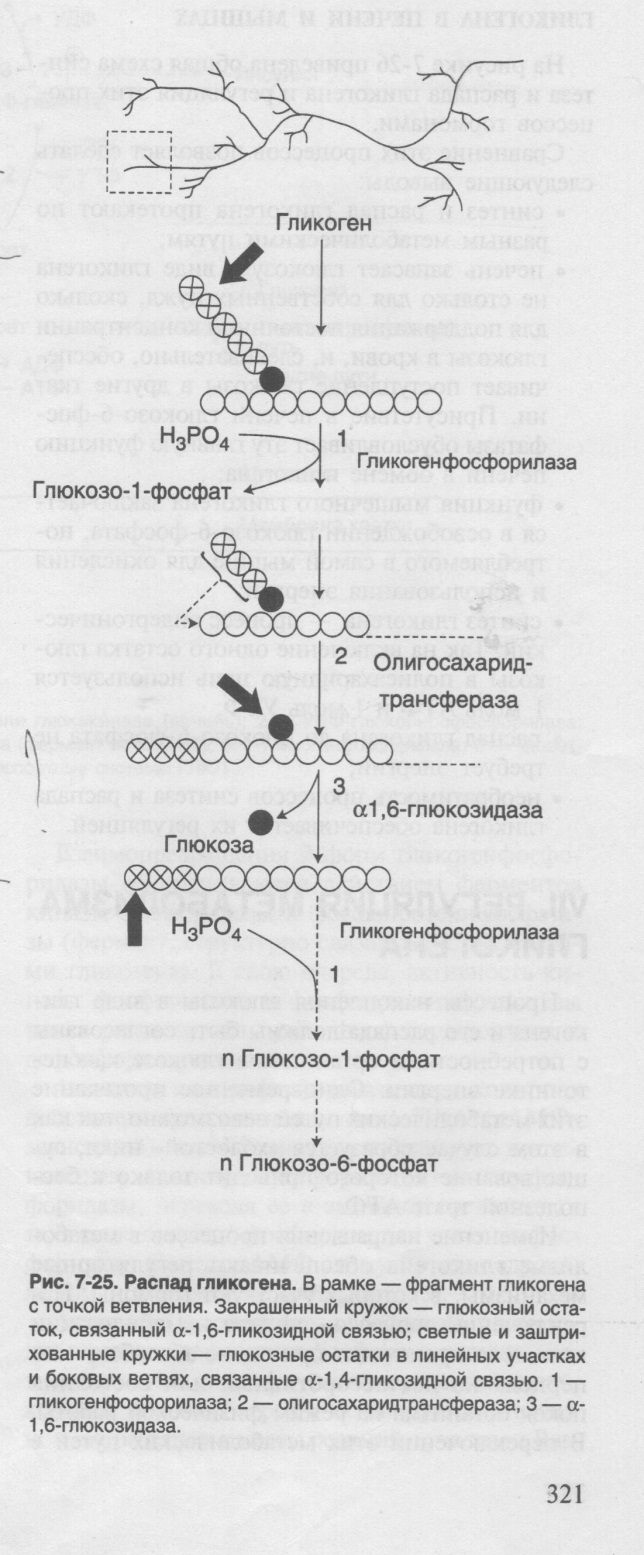
Ключевой фермент синтеза – гликогенсинтаза, распада – гликогенфосфорилаза. У обоих ферментов есть активная и неактивная форма. Гликогенфосфорилаза активируется путём фосфорилирования, гликогенсинтаза – путём дефосфорилирования. Инсулин – стимулирует синтез гликогена в мышцах и печени, глюкагон – распад гликогена в печени, адреналин – распад гликогена в печени и мышцах.
Аэробный распад глюкозы. Биологическая роль, схема, конечные продукты, ключевые ферменты.
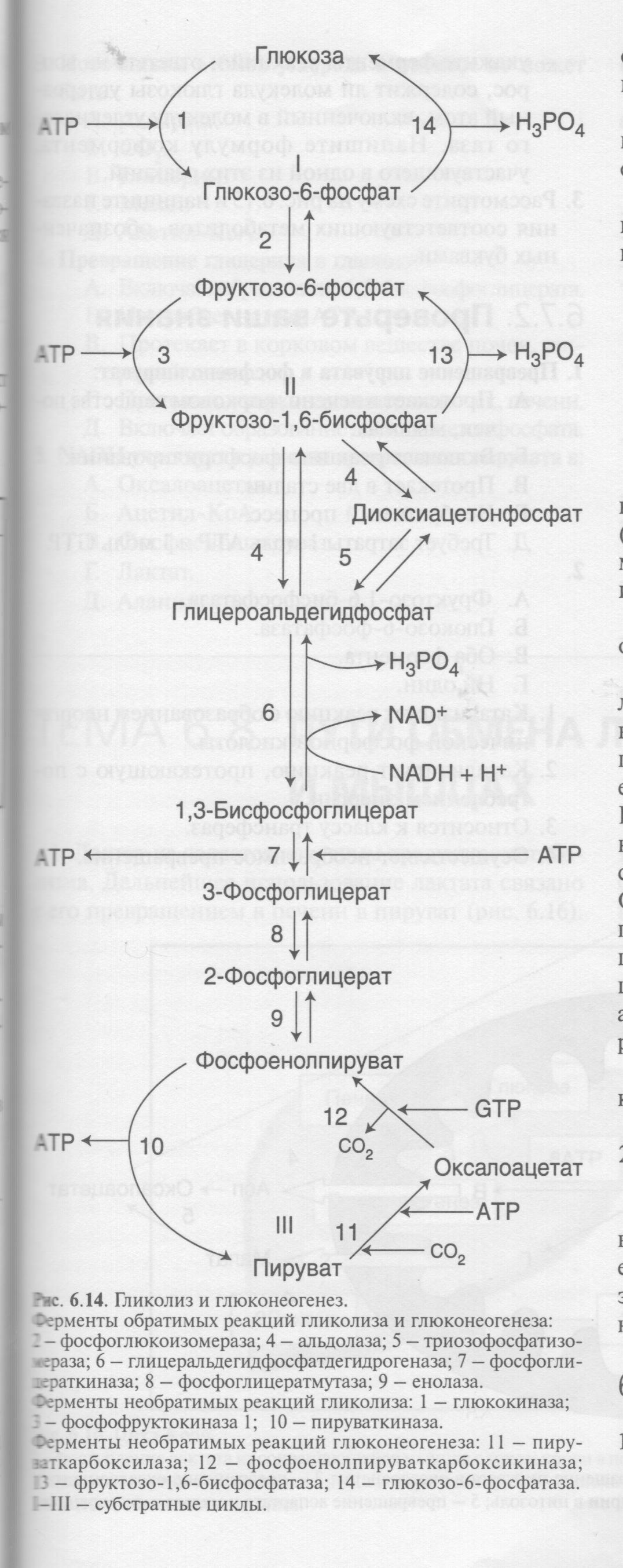
Смотрим на схему сверху вниз. Помним, что результатом 6 реакции являются два 1,3-бисфосфоглицерата. Биологическая роль – основной путь распада глюкозы, даёт 8 АТФ при распаде до пирувата и ещё плюс 15 АТФ после окисления пирувата в ЦТК, а пирувата из одной глюкозы образуется аж два штуки, так это целых 30 АТФ, и того целых 38 АТФ!!! Конечный продукт – пируват. Ключевые ферменты: гексокиназа (или глюкокиназа) – ингибируется глюкозо-6-фосфатом, фосфофруктокиназа – ингибируется АТФ и NADH, активируется АМФ, пируваткиназа – ингибируется АТФ и NADH.
Анаэробный распад глюкозы. Биологическая роль, схема, конечные продукты, ключевые ферменты.
Анаэробный гликолиз происходит тогда, когда у ткани нету кислорода, а энергия нужна. Биологическая роль – обеспечить клетку энергией в условиях гипоксии. Образуется целых 2 АТФ. Хоть что-то.
Схема: все 10 реакций аэробного гликолиза, плюс реакция восстановления пирувата до лактата при участии лактатдегидрогеназы. Эта 11 реакция нам нужна, чтобы NADH, образующийся в 6 реакции, отдал свой водород пирувату и мог снова участвовать в 6 реакции. Конечный продукт – лактат. В печени переходит в глюкозу, может перейти обратно в пируват при доступности кислорода. Ключевые ферменты – теже что и при аэробном гликолизе.
Эффект Пастера: В 6 реакции гликолиза образуется NADH. В присутствии кислорода NADH идёт в дыхательную цепь, где даёт 3 АТФ. Но если кислорода нет (гипоксия или просто митохондрии отсутствуют, как, например, в эритроцитах) NADH тратится на реакцию преобразования пирувата в лактат. Эффект Пастера заключается в том, что когда у нас гипоксия, то клетка переходит на анаэробный гликолиз (NADH тратится на превращение пирувата в лактат). Но когда доступ к кислороду возобнавляется, то NADH перехватывается дыхательнйо цепочкой, что лежит в основе переключения анаэробного гликолиза на анаэробный. Если коротко: эффект Пастера – это переход анаэробного глюколиза в аэробный, когда возобнавляется доступ к кислороду
Пентозофосфатный путь: состоит из 2 этапов – окислительного – глюкозо-6-фосфат переходит в рибулозу-5-фосфат, и неокислительного – рибулозо-5-фосфат переходит в рибозо-5-фосфат. Продукты – рибозо-5-фосфат, который служит для синтеза пуриновых и пиримидиновых нуклеотидов, и NADPH, который используется в восстановительных процессах (синтез холестерина, восстановление цитохрома P450). Локализация – жир, печень, кора надпочечников, эритроциты, молочные железы в период лактации, семенники. Биологическое значение смотри в продуктах.
Глюкуронатный: глюкозо-6-фосфат + УТФ →пирофосфорилаза УДФ-глюкоза →УДФ-глюкодегидрогеназа УДФ-глюкуроновая кислота. Роль: глюкуроновая кислота входит в состав гликозамингликанов, участвует в детоксикации токсичных веществ. Локализован в печени.
Полиольный путь: глюкозо-6-фосфат →альдозоредуктаза(NADPH) сорбит →сорбитолдегидрогеназа(NAD) фруктоза Значение: фруктоза – источник энергии в семенных пузырьках, сорбит – поддерживает осмолярность в клетках почек. При избыточном накоплении сорбита и фруктозы наблюдается набухание и разрушение клеток, а истощение NADPH приводит к снижению антитоксической функции. Локализация – почки, семенные канальцы.
Глюконеогенез – синтез глюкозы из различных соединений.
Локализация: в основе своей в печени, слабо в почках и слизистой кишечника.
Исходные субстраты: некоторые аминокислоты, глицерол, лактат, пируват.
Ключевые ферменты: – все 4 обходные реакции.
Обходные реакции: Образование фосфоенолпирувата из пирувата через окаслоацетат, гидролиз фруктозо-1,6,-бифосфата и глюкозо-6-фосфата.
Биологическое значение: синтез глюкозы когда она не поступает с пищей, а энергия нужна.
Взаимосвязь гликолиза в мышцах и глюконеогенеза в печени. (цикл Кори)
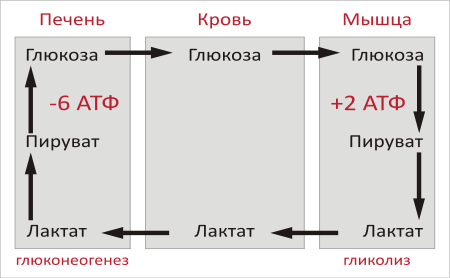
Лактат образуется в любом случае при мышечной работе в мышцах и по дефолту в эритроцитах. И организм подумал: если уж лактат и так всегда образуется, то почему бы не переводить его в глюкозу в печени с помощью глюконеогенеза и снова транспортировать обратно в ткани? Что и было сделано и названо циклом Кори.
Гормональная регуляция уровня глюкозы в крови. Гипергликемические гормоны: адреналин, глюкагон, глюкокортикоиды. Гипогликемические: инсулин.
Инсулин – Полипептид, состоящий из двух полипептидных цепей. Инсулин образуется в результате ограниченного протеолиза вначале как препроинсулин, а затем в проинсулин. Причём проинсулин распадается на инсулин и С-пептид, который имеет диагностическое значение при диабете.(если его мало, то значит и инсулина мало, значит у нас инсулинзависимый диабет). Образуется в бета-клетках островков Лангерганса в поджелудочной железе. Выделяется в ответ на гипергликемию.
Клетки мишени – Мышцы, жировая ткань, печень (частично)
Углеводы: Активирует гликолиз (глюкокиназа, фосфофруктокиназа, пируваткиназа)
Стимулирует гликогенсинтазу
Подавляет гликогенфосфорилазу
Подавляет фосфоенолпируваткарбоксиназы (глюконеогенез)
Короче делает всё, чтобы сахара стало мало в крови, много в тканях.
