
- •Лекция 6. Спектроскопические методы. Фотометрические методы анализа.
- •Спектроскопические методы анализа, классификация, характеристика и особенности методов.
- •1.3. Происхождение молекулярных спектров
- •1.4. Классификация методов спектроскопии
- •1.4.1. Атомная спектроскопия
- •1.4.2. Молекулярно - спектроскопические методы
- •1.4.3. Молекулярная абсорбционная спектроскопия
- •1.5.1. Закон Бугера - Ламберта - Бера
- •1.5.2. Ограничения и условия применимости закона Бугера - Ламберта - Бера
- •1.5.3. Закон аддитивности
- •1.6. Спектры поглощения
- •1.7. Типы спектров поглощения
- •1.7.1. Вращательные спектры
- •1.7.2. Колебательные спектры
- •1.7.2.1. Простые молекулы
- •1.7.2.2. Многоатомные молекулы
- •1.7.3. Электронные спектры
- •1.8. Аппаратура в абсорбционной спектроскопии
- •1.8.1. Блок - схема приборов
- •1.8.2. Источники излучения
- •1.8.3. Монохроматизация излучения
- •1.8.4. Приемники излучения
- •Устройство а принципы работы спектрофотометра сф - 46
- •Фотометр фотоэлектрический кфк-3
- •1. Описание прибора
- •1.9.2. Спектроскопия в ультрафиолетовой и видимой областях
- •1.10. Количественный анализ методами абсорбционной спектроскопии
- •1.10.1. Реакции в фотометрическом анализе
- •1.10.2. Основные этапы количественного анализа в фотометрии
- •1.10.3. Метрологические характеристики метода
- •Основные методы определения концентрации одного светопоглощающего вещества
- •1.13 Количественный анализ по инфракрасным спектрам
- •1.14. Другие области применения молекулярной абсорбционной спектроскопии
1.10. Количественный анализ методами абсорбционной спектроскопии
Абсорбционная спектроскопия, особенно в видимой и УФ - областях - один из наиболее распространенных методов количественного анализа. Фотометрические методы используют для определения веществ с собственным поглощением (органические вещества с хромофорными группами, переходные металлы и некоторые другие вещества, которые обладают характерным поглощением, например, нитрат - ионы, оксиды азота, элементные галогены, озон), а также для определения непоглощающих веществ. Большое число реагентов взаимодействует с непоглощающими веществами, образуя продукты с интенсивным поглощением в УФ - и видимой областях.
1.10.1. Реакции в фотометрическом анализе
В фотометрическом анализе количество вещества определяется по интенсивности окраски или светопоглощению окрашенных соединений. В видимой области цвет раствора обусловлен длиной волны излучения, не поглощенного этим раствором. Другими словами, цвет, который мы видим, является дополнительным к цвету поглощенного света. Например, раствор, поглощающий излучение в синей части спектра (~ 475 нм), окрашен в желтый цвет, т. е. синий цвет является дополнительным.
При определении неорганических компонентов для получения окрашенных соединений чаще всего используют реакции образования (иногда - разрушения) комплексных соединений; значительно реже применяются реакции окисления - восстановления. Для фотометрического определения органических компонентов чаще всего используют реакции синтеза окрашенных соединений.
Основные требования к реакциям сводятся к следующему: избирательное действие реагента, высокая скорость реакции, большое значение константы равновесия, постоянство состава и устойчивость окрашенных соединений во время проведения анализа. Важное значение в связи с этим имеет рН среды.
1.10.2. Основные этапы количественного анализа в фотометрии
Прежде чем приступить к выполнению фотометрического определения необходимо выбрать условия анализа. Можно рекомендовать следующую схему:
1. Выбор фотометрической формы вещества и проведение химических реакций для получения окрашенного соединения.
2. Установление области концентраций, в которой выполняется основной закон светопоглощения:
а) приготовление серии стандартных растворов исследуемого вещества (Сст) и раствора сравнения;
б) выбор оптимальной аналитической длины волны; в отсутствие поглощающих примесей это, как правило, максимум поглощения. Если в спектре имеется несколько полос, выбор останавливают на более интенсивной. При наличии в растворе нескольких светопоглощающих веществ выбор аналитической длины волны сложнее. Он будет рассмотрен отдельно;
в) измерение оптической плотности стандартных растворов и
построение
градуировочного графика![]()
3. Измерение
оптической плотности исследуемого
раствора![]()
4. Расчет
концентрации вещества в анализируемой
пробе![]()
1.10.3. Метрологические характеристики метода
Чувствительность характеризуется углом наклона градуировочного графика. Тангенс угла наклона равен молярному коэффициенту поглощения. Чем больше значение 8 вещества, тем чувствительнее его определение. Если принять минимальное значение оптической плотности, измеренное с необходимой точностью, Аmin = 0,01, можно рассчитать минимально определяемую концентрацию:
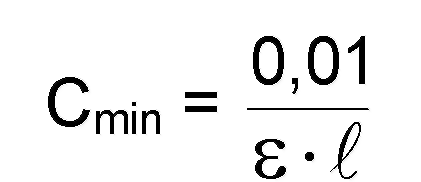 (1.10.1.).
(1.10.1.).
При величинах
![]() чувствительность
определения может составлять 10-6-10-7
М.
чувствительность
определения может составлять 10-6-10-7
М.
Воспроизводимость. Для получения воспроизводимых результатов необходимо учитывать погрешности при измерении оптической плотности.
Измерительное
устройство фотометрического прибора
обычно имеет постоянную по всей шкале
погрешность измерения![]() в
величине
пропускания Т, погрешность измерения
величины А не будет одинакова, т. к.
А = - lg
Т
в
величине
пропускания Т, погрешность измерения
величины А не будет одинакова, т. к.
А = - lg
Т
Относительная
погрешность определения концентрации![]() имеет минимальное значение при Т = 0,37
или оптической плотности А= 0,435. Для
измерения концентрации с погрешностью,
не превышающей удвоенной минимальной,
нужно проводить измерение А в интервале
0,1 ^ 1,0.
Для снижения случайной погрешности
измерения в области больших и малых
значений А существуют специальные
приемы, один из них - дифференциальный
метод анализа.
имеет минимальное значение при Т = 0,37
или оптической плотности А= 0,435. Для
измерения концентрации с погрешностью,
не превышающей удвоенной минимальной,
нужно проводить измерение А в интервале
0,1 ^ 1,0.
Для снижения случайной погрешности
измерения в области больших и малых
значений А существуют специальные
приемы, один из них - дифференциальный
метод анализа.
Правильность. Систематические погрешности в фотометрии могут возникнуть в связи с отклонениями от закона Бера, в связи с немонохроматичностью светового потока и химическими взаимодействиями в измеряемой системе, а также при наличии примесей, которые поглощают свет в данной области спектра. Для снижения систематической ошибки существуют специальные приемы, как, например, приготовление раствора сравнения, содержащего все компоненты, кроме определяемого.
Точность фотометрических методов зависит от индивидуальных особенностей фотометрической реакции, характеристик применяемого прибора и других факторов. Обычная относительная погрешность фотометрических методов составляет 1 - 2 %.
