
- •Синтез 2,6-бис(фениламинометил)пиридина
- •Оглавление
- •Введение
- •Обзор литературы Методы получения альдегидов
- •Окисление первичных спиртов
- •Восстановление карбоновых кислот и их производных
- •Получение альдегидов из оксиранов
- •Методы получения иминов
- •Методы синтеза аминов
- •Обсуждение результатов
- •Экспериментальная часть
- •Синтез 2,6-диформилпиридина [7]
- •Синтез 2,6-бис((фенилимино)метил)пиридина [12]
- •Синтез 2,6-бис(фениламинометил)пиридина [11]
- •Список литературы
Обсуждение результатов
Целью данной работы являлся синтез 2,6-бис(фениламинометил)пиридина (4).
Синтез осуществлялся по следующей трехстадийной схеме:
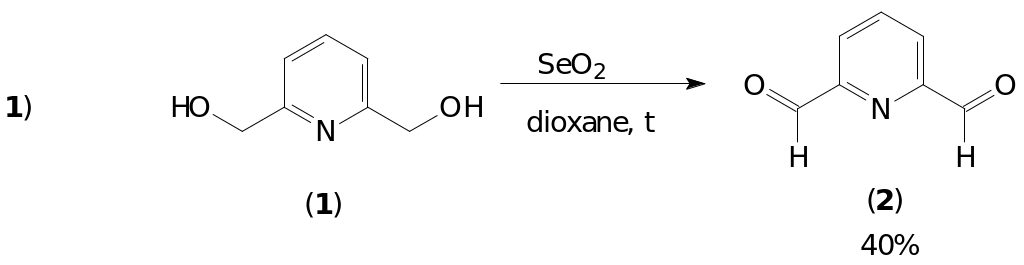
Исходный 2,6-ди(гидроксиметил)пиридин (1) являлся коммерчески доступным соединением. Согласно литературному обзору известно два способа окисления этого спирта до альдегида – с помощью диоксида марганца или с помощью диоксида селена [6, 7]. Нами был выбран второй метод, т.к. окисление диоксидом марганца требует десятикратного избытка окислителя, что в значительной степени затрудняет процедуру выделения и очистки продукта. Кроме того, при использовании SeO2 выходы альдегида более высокие. Таким образом, соединение (2) было получено с приемлемым выходом.
Температура плавления 2,6-диформилпиридина (2) хорошо согласуется с литературными данными. Структура полученного вещества была подтверждена данными спектроскопии ЯМР 1Н. Продукт реакции был получен с выходом 40%.
В спектре ЯМР 1Н (рис. 1) синглет при 10.15 м.д. соответствует атомам водорода карбонильной группы. Величина интегральной интенсивности доказывает наличие двух карбонильных групп. Два мультиплета в интервале 8.18 – 8.14 м.д. и 8.10 – 8.03 м.д. соответствуют атомам водорода пиридинового кольца. Сигнал в интервале 8.18 – 8.14 м.д. принадлежит двум атомам водорода, находящимся в мета-положениях по отношению к атому азота, сигнал при 8.10 – 8.03 м.д. отвечает протону в пара-положении.
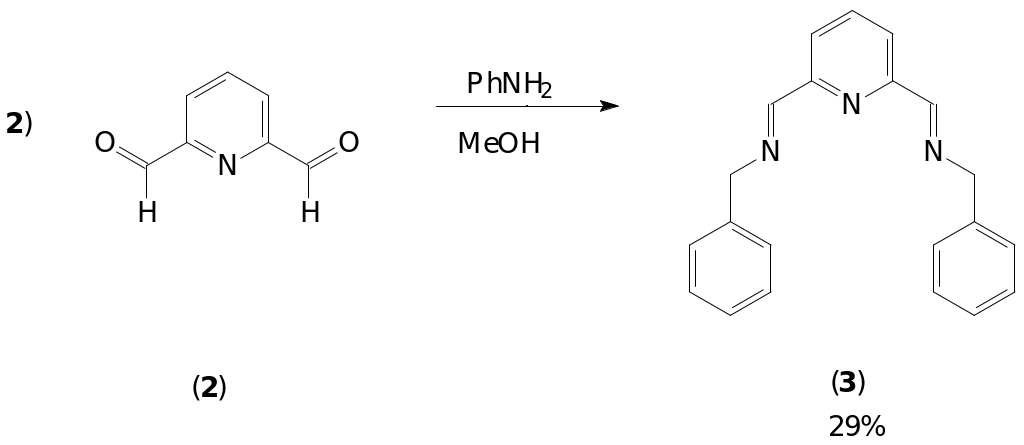
Вторая стадия синтеза заключалась в конденсации 2,6-диформилпиридина (2) с двумя эквивалентами анилина с образованием основания Шиффа. Методика получения бис(иминоарил)пиридинов описана во многих источниках [2, 11, 12, 19, 20]. Нами был выбран способ, согласно которому реакция проводится в мягкий условиях, при комнатной температуре [12]. Синтез проводился в атмосфере сухого аргона во избежание возможных процессов окисления анилина и имина. Продукт (3) был получен с выходом 29%.
Предполагаемую структуру соединения подтверждает вид спектра ЯМР 1Н (рис. 2). Мультиплет в интервале 8.65 – 8.69 м.д. соответствует двум атомам водорода при иминиевых атомах углерода. Сигналы при 8.25 – 8.19 м.д. и 7.92 – 7.86 м.д. принадлежат атому водорода в мета- и пара-положениях пиридинового кольца соответственно. Мультиплеты в области 7.42 – 7.33 м.д. и 7.30 – 7.23 м.д. отвечают сигналам ароматических протонов.
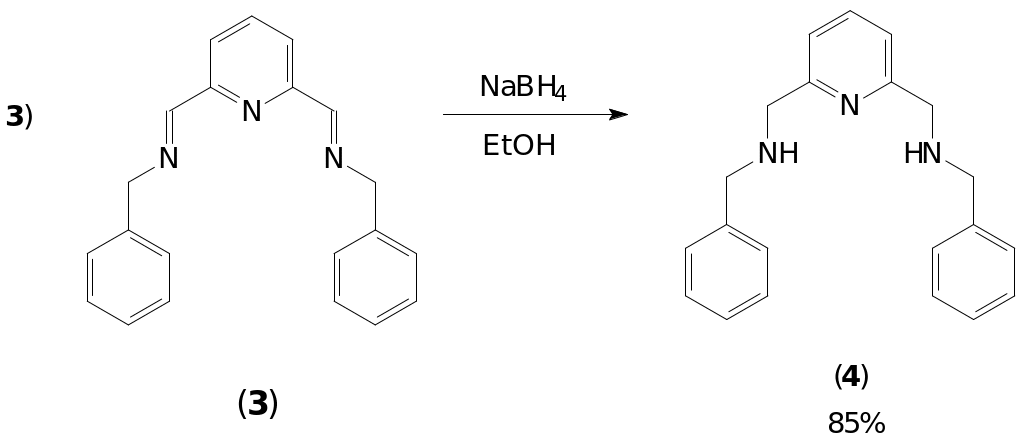
Последняя стадия заключалась в восстановлении полученного имина. В большинстве случаев для этой цели используется боргидрид натрия [2, 11]. Альтернативным вариантом является восстановление водородом на палладиевом катализаторе. Однако при этом необходимо работать при повышенном давлении, что усложняет осуществление эксперимента в лабораторных условиях. Восстановление боргидридом натрия проводилось при комнатной температуре. Целевое соединение было получено с выходом 85%.
Спектр ЯМР 1Н (рис. 3) 2,6-бис(фениламинометил)пиридина (4) содержит две группы сигналов. Первая группа объединяет сигналы CH2- и NH-групп. Синглет в алкильной области (δ=4.48 м.д., 4Н) соответствует двум СН2-группам. Широкий синглет (δ=4.74 м.д., 2Н) отвечает двум протонам NH-групп. Уширение вызвано обменными процессами с молекулами растворителя. Вторая группа сигналов характеризует ароматические протоны. Триплет при 7.59 – 7.55 м.д. соответствует атому водорода, находящемуся в пара-положении пиридинового кольца. Мультиплет в области 7.24 – 7.16 м.д. принадлежит мета- и пара-протонам ароматического кольца. Сигнал в области 6.79 – 6.71 м.д. представляет собой триплет триплетов. Сигнал соответствует двум протонам в мета-положении пиридинового кольца. Мультиплет в области 6.70 – 6.65 м.д. относится к атомам водорода, находящихся в орто-положениях бензольного кольца.
