
- •Синтез 2,6-бис(фениламинометил)пиридина
- •Оглавление
- •Введение
- •Обзор литературы Методы получения альдегидов
- •Окисление первичных спиртов
- •Восстановление карбоновых кислот и их производных
- •Получение альдегидов из оксиранов
- •Методы получения иминов
- •Методы синтеза аминов
- •Обсуждение результатов
- •Экспериментальная часть
- •Синтез 2,6-диформилпиридина [7]
- •Синтез 2,6-бис((фенилимино)метил)пиридина [12]
- •Синтез 2,6-бис(фениламинометил)пиридина [11]
- •Список литературы
Методы получения иминов
Синтез тридентатных лигандов – 2,6–бис(ариламинометил)пиридинов осуществляется в две стадии. Первой стадией является конденсация 2,6–диформилпиридина с анилином или его производными с образованием основания Шиффа. В большинстве случаев [2, 11] полученный имин сразу вводят в реакцию с NaBH4, однако описаны методики с выделением образующегося имина в индивидуальной форме [12, 13]. Например, в работе [12] описан синтез 2,6-бис((фенилимино)метил)пиридина.

В работе [13] описан синтез лигандов, полученных конденсацией производных пиридина и пирролидина. В этом случае также выделяют полученный имин в индивидуальной форме. Так, например, два эквивалента N-винилпирролидин–2–она и один эквивалент диэтилпиридин-2,6-дикарбоксилата добавляют к NaH. Гидролиз приводит к образованию имина.

Помимо конденсации карбонильных соединений с аминами существуют и другие способы получения иминов. Так, например, имины образуются при восстановлении нитрилов действием ДИБАЛ-Н в нейтральной среде [14].

Методы синтеза аминов
Методы синтеза азотосодержащих тридентатных лигандов разнообразны. Распространённым способом является конденсация 2,6-пиридиндикарбальдегида с первичными ароматическими аминами с последующим восстановлением боргидридом натрия [2, 11].

Другим вариантом восстановления основания Шиффа является гидрирование в присутствии катализатора Pd/C при давлении водорода 5 атм [13]. Стоит отметить, что проведение гидрирования при повышенном давлении ограничивает применение этого метода в лаборатории. Кроме того, выходы в данном случае невелики (39%).

Описано [3, 15, 16, 17, 18] множество методик синтеза тридентатных лигандов с использованием в качестве исходных веществ бромометилпиридинов. Суть метода заключается в замещении брома на аминогруппу.
Наиболее простым методом получения 2,6–бис(аминоалкил)пиридинов является взаимодействие 2,6–бис(бромометил)пиридина с соответствующим амином по механизму нуклеофильного замещения. Так, например, в работе [17] описаны методики получения различных производных пиридина.

Особенность синтеза заключается в том, что реакция проводится с избытком RNH2 во избежание образования третичных аминов. Однако отделение продуктов реакции от избыточных количеств исходного соединения сопряжено с методическими сложностями.
Аналогичный метод известен для синтеза 2,6–бис(аминоарил)пиридинов [3, 19, 20]. В данном случае реакция проводится при высокой температуре (120°С).

2,6-Бис(аминометил)пиридин можно также получать взаимодействием 2,6-бис(бромометил)пиридина с гексаметилентетраамином (уротропином). В ходе реакции образуется промежуточный продукт – комплекс бромометилпиридина с уротропином. Синтез проводят при кипячении в хлороформе. Однако, выходы в этой реакции низкие (23%) [15, 16].

Более простой метод синтеза [18] 2,6–бис(аминометил)пиридина основывается на реакции бромометилпиридина с фталимидом калия (синтез Габриэля). Исходным реагентом является 2,6–бис(бромометил)пиридин. Реакция проводится в ДМФА при нагревании (90-100°С). При этом сначала образуется промежуточный продукт 2,6–бис(фталимидометил)пиридин. Его выделяют, затем обрабатывают гидразином в этиловом спирте и 6N HCl. Следует отметить, что выход в этом случае гораздо выше (88%), чем при использовании гексаметилентетраамина.

Недостатком вышеприведённых методик является то, что исходное вещество, 2,6-бис(бромометил)пиридин, проявляет канцерогенные свойства.
Для синтеза 2,6-бис(ариламинометил)пиридинов, где арильная группа имеет сильные электроноакцепторные заместители, описан [21] метод синтеза, основанный на нуклеофильном ароматическом замещении. Реагентами в данном случае являются 2,6–бис(аминометил)пиридин и гексафторбензол. Реакцию проводят в ДМСО при 80°С в присутствии карбоната калия.
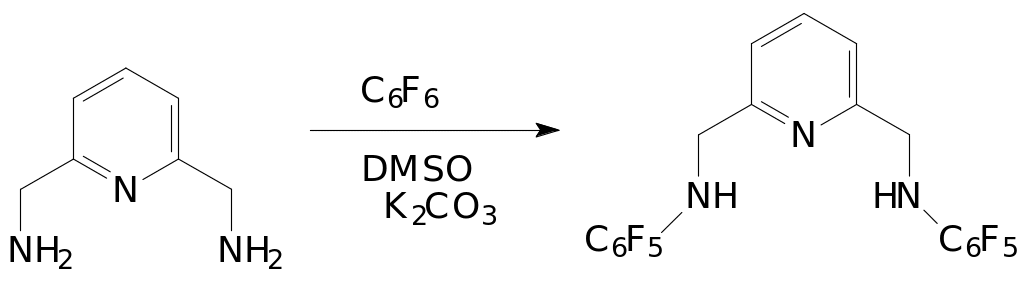
Альтернативным методом синтеза тридентаных лигандов, содержащих пиридин, является реакция с цианидами. Описана [22] методика получения 2,6–бис(α–аминоизопропил)пиридина. В качестве исходных реагентов используются 2,6–дицианопиридин и триметилцерий.

Синтез триметилцерия осуществляется in situ. Навеску гидрата CeCl3·7H2O дегидратируют путём длительного нагревания при 160°С в вакууме, затем вводят в реакцию с CH3Li. Однако соединения церия очень неустойчивы. Сложность заключается также в том, что полное обезвоживание гидрата церия осуществить крайне затруднительно. Присутствие молекул воды создаёт значительные помехи в ходе синтеза, что приводит к низким выходам.
