
- •Лекция № 3 Тема:
- •Резистентность и восприимчивость макроорганизма
- •Классификация инфекционных болезней
- •Понятие об эпидемическом процессе и его формах
- •Иммунитет (основы иммунологии)
- •Конституциональные факторы естественной резистентности
- •Антигены
- •Иммунная система
- •Строение и биологическая роль органов иммунитета
- •Антитела (иммуноглобулины)
- •Антителообразование
- •Иммунный ответ
- •Цитокины
- •Спектр действия интерлейкинов
- •Теории антителообразования и взаимодействия антител с антигенами
- •Иммунопатология
- •Аллергия (гиперчувствительность)
- •Типы аллергических реакций
- •Приготовление и применение микробных аллергенов
- •Иммунодефициты
- •Трансплантационный иммунитет
- •Противоопухолевый иммунитет
- •Иммунный статус человека
- •Принципы иммунотерапии
- •Иммунные сыворотки
- •Титрование антитоксических лечебных сывороток.
- •Вакцины
- •Традиционные вакцины
- •Вакцины нового типа
Иммунная система
Материальным субстратом иммунной системы является инкапсулированная (лимфоузлы) и диффузно рассеянная лимфоидная ткань. Ввиду этого иммунную систему нередко отождествляют с лимфоидной системой. В иммунной системе выделяют центральные (первичные) и периферические (вторичные) органы иммунитета. Центральными называют те органы, в которых происходит формирование и созревание В- и Т-клеток, способных распознавать антиген, а периферическими - органы, где эти клетки затем функционируют.
Центральными органами иммунитета являются тимус и фабрициева бурса (сумка) у птиц, а у млекопитающих -
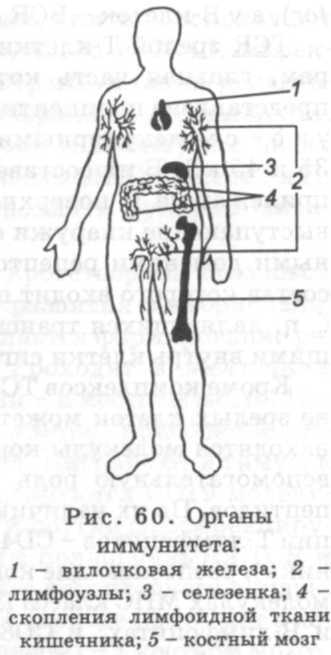
костный мозг; периферическими - лимфатические узлы, селезенка, а также скопление лимфоидной ткани слизистых оболочек (рис. 60).
Функционирующей основой иммунной системы являются Т-, В-клетки, макрофаги, дендритные и другие вспомогательные антигенпрезентирующие клетки (АПК).
Структура, формирование и происхождение клеток иммунной системы
Т- и В-клетки. Являются эффекторными клетками иммунной системы. По форме, структуре и размерам покоящиеся Т- и В-клетки в отсутствие контакта с чужеродными веществами напоминают собой обычные лимфоциты крови диаметром 7-9 мкм с круглым или бобовидным ядром и узким ободком цитоплазмы, бедной цитоплазматическими гранулами (см. рис. 55). Их характерной особенностью является наличие на внешней мембране уникального рецептора для распознавания одного антигена, которые у Т-клеток сокращенно обозначают TCR (Т cell receptor), а у В-клеток - BCR (В cell receptor).
TCR зрелой Т-клетки является белковым гетеродимером, главная часть которого у одного типа рецептора представлена полипептидными цепями α и β, а у другого -γ и δ - с молекулярными массами соответственно 27 и 32, 35 и 45 кД. В их составе имеется по два домена (глобул): прилежащие к поверхности мембраны, константные, и выступающие кнаружи от нее - вариабельные. Константными доменами рецептор нековалентно связан с CD3, в состав которого входит пять полипептидных цепей у, 6, е, £, л, являющихся трансмембранными белками, передающими внутрь клетки сигналы о связывании антигена.
Кроме комплексов TCR-CD3, число которых на мембране зрелых клеток может составлять 30-40 тыс. молекул, находятся молекулы-корецепторы CD4 и CD8, играющие вспомогательную роль при распознавании антигенных пептидов. По их наличию выделяют две основные популяции Т-лимфоцитов — СБ4+-клетки, или Т-хелперы (помощники), распознающие комплексы антигенных пептидов на молекулах МНС класса II макрофагов, дендритных клеток и В-лимфоцитах, и СБ8+-клетки, или Т-киллеры (убийцы), часто называемые цитотоксическими лимфоцитами (ЦТЛ), которые распознают пептиды на молекулах МНС класса I всех ядерных клеток. Большое участие в процессе распознавания антигена Т-клетками имеют еще две дополнительные молекулы-корецепторы, в частности однотипная CD28 и различные изоформы (варианты) CD45. Самая крупная изоформа CD45RA с молекулярной массой 220 кД, свойственная ранее не контактировавшим с антигеном «наивным» Т-лимфоцитам, при антигенной дифференциации последовательно преобразуется в другие изоформы вплоть до формирования CD45RO, специфичной клеткам памяти (см. «Иммунный ответ»). Что касается CD28, то она присутствует на всех СБ4+-клетках и на 60-70 % СБ8+-лимфоцитах, но связывается с рецепторным комплексом только в процессе распознавания ими антигена.
BCR имеет иммуноглобулиновую природу и в зрелой покоящейся В-клетке представлен мономерным IgM (сывороточный IgM пентамер) в комплексе с IgD и дополнительными молекулами Iga и Ig(3, участвующими в передаче сигнала о связывании антигена в клетку.
Помимо иммуноглобулиновых рецепторов для распознавания антигена, число которых может составлять около 150 000 молекул, зрелые В-лимфоциты располагают мембранными молекулами CD80, CD86 и CD40, эффективно контактирующими с Т-хелперами, а также рецепторами для Fc фрагмента IgG, СЗЬ фракции комплемента, интерлейкинов 1 и 4, интерферона γ. К тому же на их мембранах экспрессированы антигены МНС классов I и II, позволяющие В-лимфоцитам выполнять функцию анти-генпрезентирующих клеток.
Т- и В-клетки происходят от кроветворной стволовой клетки. Начальные этапы своего развития в эмбриональном периоде, основой которого является формирование рецепторного аппарата, Т-клетки проходят в желточном мешке и печени, а В-клетки у птиц - в костном мозге. Появляющиеся предшественники Т-клеток, приобретающие маркерные молекулы CD7 или CD4, мигрируют в тимус, а преВ-клетки, на которых экспрессируются CD19 молекулы, - в фабрициеву сумку, где те и другие дифференцируются в зрелые Т- и В-лимфоциты с полноценными TCR и BCR. У млекопитающих созревание рецепторного аппарата В-лимфоцитов в эмбриональном периоде протекает в печени, а в постнатальном (послеродовом) — в костном мозге.
Созревшие клетки расселяются затем в лимфатические узлы и селезенку, занимая в них относительно обособленные места: В-клетки - кортикальные зоны лимфоузлов, а Т-клетки - паракортикальные или соответствующие зоны лимфоидных фолликулов селезенки. Правда, Т-клетки постоянно рециркулируют, т. е. покидают иммунные органы, проникают в кровоток, а из него - вновь в лимфоид-ные органы.
Популяция Т-лимфоцитов весьма многочисленна. Больше всего их в тимусе и грудном лимфатическом протоке, где они составляют соответственно 95-100 и 80-90 % ,в крови и лимфатических узлах - 55-85 % , в селезенке и лимфоидной ткани слизистых оболочек - 25-40 %. Практически отсутствуют Т-клетки в костном мозге. Большая часть Т-лимфоцитов - долгоживущие клетки, нередко функционирующие на протяжении всей жизни организма. Высокочувствительны к радиации. По отношению к циклофосфамиду Т-киллеры более устойчивы, чем Т-хелперы.
Пул В-лимфоцитов в организме животных тоже значителен: 40-60 % от общей массы клеток находится в групповых лимфатических фолликулах, костном мозге, крови, селезенке и 25 % - в лимфатических узлах и грудном лимфатическом протоке. Практически нет В-лимфоцитов только в тимусе. Продолжительность жизни зрелых В-лимфоцитов, не подвергающихся воздействию антигенов, составляет несколько месяцев.
Субпопуляции Т- и В-клеток. Популяции Т- и В-клеток неоднородны не только по структуре рецепторного аппарата, но также и по эффектам действия и участию в иммунном ответе. Так, СБ4+-Т-хелперы, или ТхО-клетки, под воздействием антигенов могут дифференцироваться на две субпопуляции - в направлении воспалительных хелперов Txl, выполняющих посредническую функцию в формировании Т-киллеров и участвующих в цитотоксических клеточных реакциях, или в направлении иммунных хелперов Тх2 гуморального ответа, индуцирующих трансформацию В-лимфоцитов в плазмоциты. Пути дихотомии (dicha - на две части, tome - сечение) ТхО определяются, прежде всего, природой антигена-индуктора, его дозой, антигенпрезентирующими клетками и микроокружением. Так, микобактерии, вирус гриппа, стрептокиназа, интерлейкин 12 (ИЛ-12) направляют дифференциацию ТхО-клеток в сторону Txl, а ИЛ-4 и аллергены - в направлении Тх2; действие высоких и низких доз антигена приводит к возникновению Txl, а средних - к Тх2; при контакте ТхО с В-лимфоцитами развиваются Txl, а при контакте с дендритными клетками и макрофагами - Тх2; развитию Txl благоприятствует микроокружение лимфоузлов, а Тх2 - микроокружение слизистых оболочек.
В популяции СБ8+-Т-лимфоцитов различают прецитотоксическую и цитотоксическую субпопуляции. Относительно индукции формирования ЦТЛ существует три предположения: 1) СВ8+-клетки активируются антигенпрезентирующими дендритными клетками, вырабатывающими необходимый им для размножения интерлейкин 2 при условии экспрессии большого числа костимулирующих молекул CD80 и CD86; 2) тот же механизм активации СВ8+-клеток может достигаться с помощью воздействия на дендритные клетки интерферона γ, продуцируемого Txl-субпопуляцией; 3) допускается, что умеренно стимулируемые СБ8+-клетки на АПК активируются, синтезируя собственный ИЛ-2.
В популяции В-лимфоцитов различают две субпопуляции: самоподдерживающуюся в брюшной полости, сальниковую В1, содержащую молекулу CD5, и костномозговую, обычную В2, не имеющую СБ5-антигена. Основное отличие СБ5-клеток состоит в том, что они в постнаталь-ном периоде остаются потенциально агрессивными в отношении собственных клеток и тканей и могут вырабатывать полиспецифические IgM-аутоантитела, которые участвуют в развитиии аутоиммунных патологических процессов. Не имеющая СТ)5-молекул субпопуляция В2-лимфоцитов, превратившись в антителообразующие плазмоциты, продуцирует не поли-, а видоспецифические IgM, и не к собственным, а к чужеродным антигенам. При этом тимуснезависимые антигены индуцируют трансформацию В2-лимфоцитов в плазмоциты без дополнительных стимуляторов, а тимусзависимые - с помощью Т-хелперов, макрофагов, стромальных отростчатых клеток и выделяемых ими цитокинов (см. «Иммунный ответ»).
Т-супрессоры. Популяция супрессоров (supressum - подавлять) в отличие от эффекторных Т- и В-клеток функционирует как регулятор нормального иммунного ответа, в частности, под ее контролем находится Т-клеточный и тимусзависимый гуморальный ответы, а также поддержание иммунной толерантности к аутоантигенам, к которым, правда, могут иметь отношение и так называемые вето-клетки, являющиеся, по-видимому, аутоспецифическими лимфоцитами.
Основной клеткой-мишенью Т-супрессоров считаются Т-хелперы. Т-супрессоры также оказывают влияние на В-лимфоциты, особенно отчетливо - в процессе регуляции образования IgE. Описано несколько структурных цепей рецепторов Т-супрессоров и гуморальных факторов (в том числе цитокинов), реализующих их действие, но получить клоны негибридомных Т-супрессоров и клонировать их гены гуморальных факторов и МНС не удается. Вследствие этого некоторые исследователи считают, что супрес-сорами является киллерная субпопуляция лимфоцитов, поскольку СВ8+-клетки в ряде экспериментов способны регулировать иммунные ответы. Однако каким образом они распознают антигены, связанные с молекулами МНС класса II, как реализуется супрессорное действие CD8+-клеток в отношении Т-хелперов и В-лимфоцитов и почему они проявляют свое действие только на поздних стадиях развития иммунного ответа — остается не раскрытым. С позиции взаимных ингибирований функций супрессор-ными можно назвать субпопуляцию СБ4+-клеток, ее подклассы Txl и Тх2 и даже - активированные макрофаги. Из этого вытекает, что скептицизм относительно существования Т-супрессоров не развеял реальности механизмов активной иммуносупрессии, опосредованной разновидностью Т-лимфоцитов, которые в 70-х гг. XX в. назвали Т-супрессорами. Как и эффекторные Т-лимфоциты, они очень чувствительны к ионизирующей радиации, но отличаются от них коротким периодом жизни.
Макрофаги. Макрофаги - основной тип клеток моноцитарной системы лимфоцитов. Они представляют собой гетерогенные по функциональной активности клетки диаметром 15-25 мкм с хорошо развитой цитоплазмой (см. рис. 55, а). На их поверхности имеются специфические рецепторы к Fc-фрагменту иммуноглобулинов G, М, А и Е, нескольким субфракциям комплемента, гормонам, нейромедиаторам, гистамину, бактериальным липополисахаридам. Активное взаимодействие макрофагов с окружающими их клетками и межклеточным матриксом определяется наличием на их поверхности ряда адгезивных молекул и рецепторов к цитокинам, в частности хемотаксическим. Макрофаги не имеют собственных рецепторов для распознавания антигенов, но могут осуществлять эту функцию через фиксацию на их поверхности иммуноглобулинов. На всех макрофагах содержатся антигены МНС класса I, а на активированных - МНС класса II, имеющие непосредственное отношение к представлению антигенных пептидов Т-хелперам. Секретируют различные фракции комплемента и цитокины, стимулирующие пролиферацию и дифференциацию стволовых лимфоцитов в гранул оциты. Они обладают высокой микробоцидной активностью. Так, в развитом лизосомальном аппарате макрофагов содержатся лактоферрин и лизоцим, протеиназы, ка-тепсин G, дифензины и другие вещества, повреждающие стенки бактерий и нарушающие их метаболические процессы. Такое же действие на фагоцитированные бактерии оказывают последовательно образующиеся в макрофагах анион супероксид (0~2), пероксид водорода (Н202) и ионы НС10~, в катализе которых участвуют соответственно НАДФ'ОКСИдаза с цитохромом Ъ, дисмутаза и миелоперок-сидаза. При определенных условиях макрофаги проявляют также цитотоксическое действие на опухолевые клетки. Общая численность моноцитов и макрофагов в организме человека - около 2-Ю11. Продолжительность их жизни - от 20 сут до 7 мес. В большинстве случаев срок обновления популяций тканевых макрофагов равен 20-40 дням.
Дендритные клетки. Термином дендритные (dendron -дерево) называют отростчатые клетки эпидермиса и стро-мы органов, в том числе лимфоидных, несущих молекулы МНС класса П.
Точнее говоря, существует шесть разновидностей клеток с дендритной морфологией: белые отростчатые эпидермоциты (клетки Лангерганса); близкие им по свойствам дендритные клетки слизистых оболочек бронхолегочного и пищеварительного трактов-; вуалевые клетки лимфы с вуалями-отростками; дендритные клетки зародышевых центров лимфоузлов; интердигитальные (межпальцевые) клетки тимуса; и, главное, интердигитальные клетки лимфатических узлов. Большая часть их происходит из клеток Лангерганса, которые хорошо связывают и обрабатывают антиген, но практически не осуществляют его презентацию. Полагают, что это связано с отсутствием на их поверхности костимулирующих молекул CD80 и CD86. Эти молекулы приобретаются интердигитальными клетками в результате трансформации клеток Лангерганса в лимфатических узлах, куда они мигрируют в процессе развития воспаления и иммунных реакций. В отличие от своих предшественников интердигитальные клетки утрачивают способность связывать и обрабатывать антиген, но эффективно представляют процессированный антигенный пептид Т-хелперам, вызывая их активацию, деление и секрецию цитокинов. На поверхности этих клеток много продуктов МНС класса II, но нет рецепторов к Fc-фрагменту иммуноглобулинов и субфракциям комплемента. Как и макрофаги, интердигитальные клетки обладают адгезив-ностью, способны к пиноцитозу, но не фагоцитируют. Дендритные клетки имеют костномозговое происхождение и могут возникать как из моноцитарных предшественников, так и из зрелых моноцитов. Точно не установлена лишь природа дендритных клеток зародышевых центров лимфоузлов, которые могут являться «хранилищем» антигена и обеспечивать длительное поддержание иммунологической памяти. Но если они, как полагают, действительно являются потомками фибробластов, то займут особое место среди остальных типов дендритных клеток.
Таким образом, основными клеточными элементами, обеспечивающими приобретенный иммунитет, являются В-лимфоциты, Т-лимфоциты, макрофаги и дендритные антигенпрезентирующие клетки. При этом иммуноциты созревают в центральных органах иммунитета, а функционируют вместе с А-клетками как единое целое в лимфатических узлах, селезенке и других вторичных органах иммунитета.
