
- •Глава 1. Элементы кинематики.
- •§1.1 Механическое движение. Системы отсчёта. Физические модели.
- •§1.2 Уравнение движения.
- •§1.3 Кинематические характеристики вращательного движения.
- •Глава 2. Динамика частиц
- •§2.1 Динамика частиц. 1-й закон Ньютона.
- •§2.2 Силы. 2-й закон Ньютона.
- •§2.3 Импульсная форма 2-го закона Ньютона.
- •Глава 3. Законы сохранения
- •§3.1 Закон сохранения импульса.
- •§3.2 Механическая работа и мощность.
- •§3.3 Теорема о кинетической энергии.
- •§3.4 Потенциальная энергия.
- •§3.5 Закон сохранения механической энергии.
- •§3.6 Закон сохранения полной энергии.
- •§3.7 Упругий и неупругий удар тел.
- •Глава 4. Закон всемирного тяготения
- •§4.1 Закон всемирного тяготения.
- •Глава 5. Динамика вращательного движения
- •§5.5 Закон сохранения момента импульса.
- •§5.6 Вычисление момента инерции.
- •§5.7 Работа и кинетическая энергия при вращательном движении.
- •Глава 6. Основы специальной теории относительности
- •§6.1 Классический принцип относительности. Преобразования Галилея.
- •§6.2 Преобразования Лоренца. Постулаты сто.
- •§6.3 Сокращение длинны.
- •§6.4 Удлинение промежутков времени.
- •Значит наблюдатель в системе s` сначала увидит молнию передней части вагона и потом задней.
- •§8.2 Графический способ представления колебаний.
- •§9.2 Дифференциальное уравнение гармонических колебаний. Гармонический осциллятор.
- •§9.3 Кинетическая энергия гармонических колебаний.
- •§9.4 Затухающие колебания.
- •§9.5 Вынужденные колебания.
- •Гл. 10 Упругие волны
- •§10.1 Продольные и поперечные волны.
- •§10.2 Уравнение бегущей волны.
- •§10.3 Фазовая скорость. Энергия упругих волн.
- •§10.4 Сложение волн.
- •Молекулярная физика и термодинамика.
- •Глава 11. Кинетическая теория газов
- •§11.1 Основное уравнение кинетической теории газов.
- •§11.2 Кинетическая интерпретация абсолютной температуры.
- •§11.3 Закон равномерного распределения энергии по степеням свободы.
- •§11.4 Внутренняя энергия идеального газа.
- •Глава 12. Статистические распределения
- •§12.1 Распределения Максвелла молекул по скоростям.
- •§12.3 Барометрическая формула.
- •§12.4 Распределение Больцмана.
- •Глава 13. Физическая кинетика
- •13.1 Длина свободного пробега.
- •§13.2 Явление переноса в газах.
- •Диффузия
- •Теплопроводность
- •Глава 14. Физические основы термодинамики
- •§14.2 Зависимость работы от характера термодинамического процесса.
- •§14.3 Теплоемкость газов.
- •§14.4 Круговые процессы. Принцип работы тепловых машин.
- •§14.5 Идеальная тепловая машина Карно.
- •§14.6 Обратимые и необратимые процессы.
- •§14.7 Второй закон термодинамики.
- •§14.8 Энтропия.
- •§14.9 Статистическая природа энтропии.
- •Глава 15. Реальные газы
- •§15.1 Межмолекулярные силы.
- •§15.2 Уравнение Ван-дер-Ваальса.
§11.4 Внутренняя энергия идеального газа.
Внутренняя энергия идеального газа состоит из учета потенциальной энергии и кинетической энергии движения атомов или молекул, поэтому величина внутренней энергии определяются выражением:
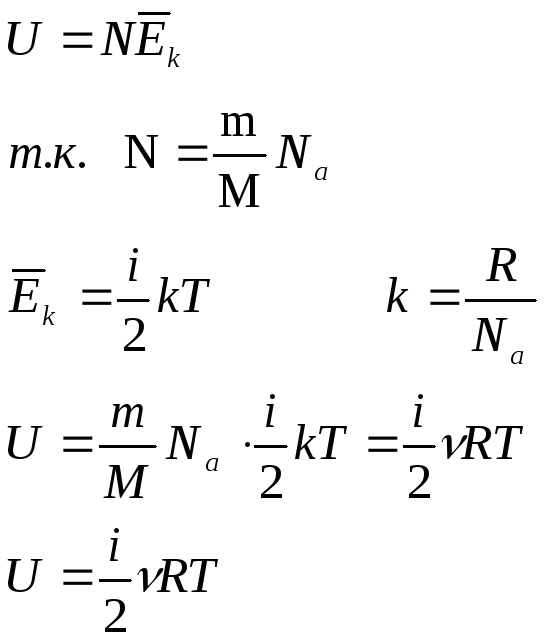
Внутренняя энергия – это функция состояние газа. Она прямо пропорциональна абсолютной температуре и характеризует энергию всех молекул газа.
Глава 12. Статистические распределения
§12.1 Распределения Максвелла молекул по скоростям.
![]()
Введенная ранее средняя квадратичная скорость характеризует среднюю интенсивность движения, ясно, что при хаотическом движении молекулы движутся с различными скоростями. Очевидно, что число молекул с очень маленькими скоростями, как и число молекул со скоростями сравнительно невелико. Основное количество молекул имеет скорости близкие к КВРаспределение по скоростям установил Максвелл. Для этого он ввел функцию распределенияf(). Физический смысл этой функции заключается в том, что она позволяет вычислить число молекулdNдвижущихся со скоростями в интервале (,+d)dN=f()d


В конечном интервале (1,2):
![]()
Графическая зависимость функции распределения от скорости имеет вид:
Аналитический вид:
![]() (N–общее число молекул)
(m0– масса одной
молекулы)
(N–общее число молекул)
(m0– масса одной
молекулы)
![]() -наиболее вероятная скорость
-наиболее вероятная скорость
![]() - средняя арифметическая скорость
- средняя арифметическая скорость
![]() - средняя квадратичная скорость.
- средняя квадратичная скорость.


При увеличении температуры интенсивность движения возрастает
§12.3 Барометрическая формула.
Распределение молекул в поле силы тяжести является неравномерным. В жидкостях давление на различных глубинах различно в следствии гидростатического давления.
![]()
![]()
Для газов это соотношение может быть записано только для малых толщин:
![]()
![]()
![]()
![]() т.о.
т.о. ![]()
![]()
![]()
![]()
т.о.
![]()
![]()
![]()
![]() - барометрическая формула. Вывод получен
при условии, что температура на всех
высотах одинакова.
- барометрическая формула. Вывод получен
при условии, что температура на всех
высотах одинакова.
§12.4 Распределение Больцмана.
Распределение Больцмана – распределение частиц в потенциальном поле. Барометрическая формула является частным случаем распределения частиц в потенциальном поле. Преобразуем его используя уравнение Менделеева-Клапейрона в виде: p=nkT
![]()
![]()
![]() -распределение
Больцмана.
-распределение
Больцмана.
Анализ:
1)T∞, следовательноWП/kT0,n=n0
2)T0, след.WП/kT∞,n0, Все молекулы падают на землю.
Глава 13. Физическая кинетика
13.1 Длина свободного пробега.
Длина свободного пробега – расстояние между двумя последовательными соударениями молекул в газе.<λ> Достаточно большой круг явлений может быть описан с помощью простейшей механической модели, согласно которой молекулы представлены в виде шариков, которые испытывают упругие соударения между собой и стенками сосуда. Минимальное расстояние, на которое могут сблизиться молекулы называется эффективным диаметром и принимается за диаметр шариков.

К руг
площадьюd2- называется эффективным сечением.
Найдем среднее число соударений которые
испытывает молекулы при хаотическом
движении <Z>; Пусть все
молекулы покоятся и движется только
одна. За 1 сек. молекула пройдет расстояние
равное <>
руг
площадьюd2- называется эффективным сечением.
Найдем среднее число соударений которые
испытывает молекулы при хаотическом
движении <Z>; Пусть все
молекулы покоятся и движется только
одна. За 1 сек. молекула пройдет расстояние
равное <>
При этом она столкнется со всеми молекулами которые находятся в пределах эффективного сечения т.е. находится в цилиндре высотой <> и площадью сечения равнойd2еслиn– концентрация молекул, то <Z>=nV=nd2<>
Учет движения всех частиц приведет к:
![]()
Средний путь за 1 сек. т.е. длина свободного пробега:

