
2. Атом водорода
Э
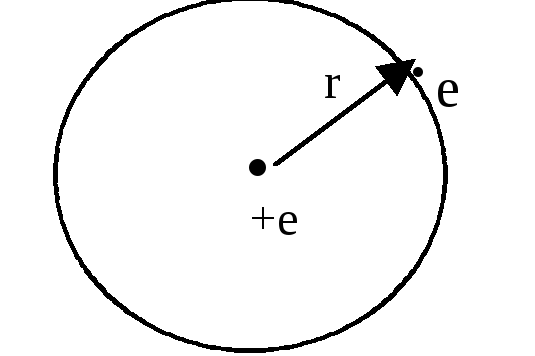
Граничные условия
имеют характер:
![]()
![]() .
.
Таким образом, имеем потенциальную яму бесконечной глубины (ящик) с радиальной симметрией, со стенками гиперболической формы (фигура вращения - типа грамофонной трубы).
Кинетическая энергия электрона Т = kqе2/2r и полная энергия Е = Т + U = - kqе2/2r = - T = |U|/2.
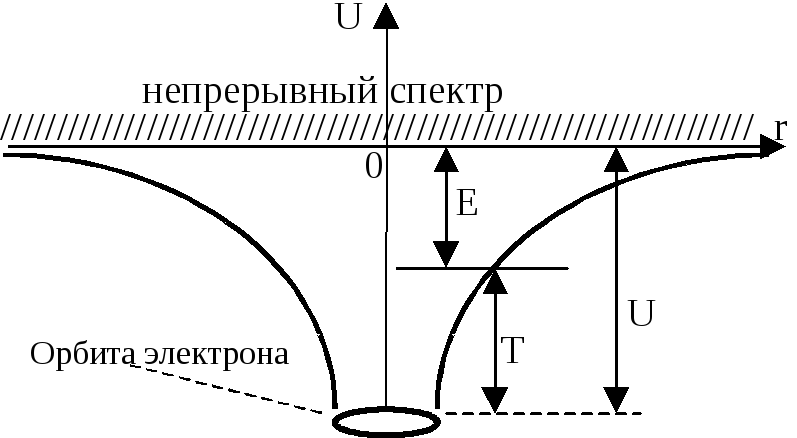
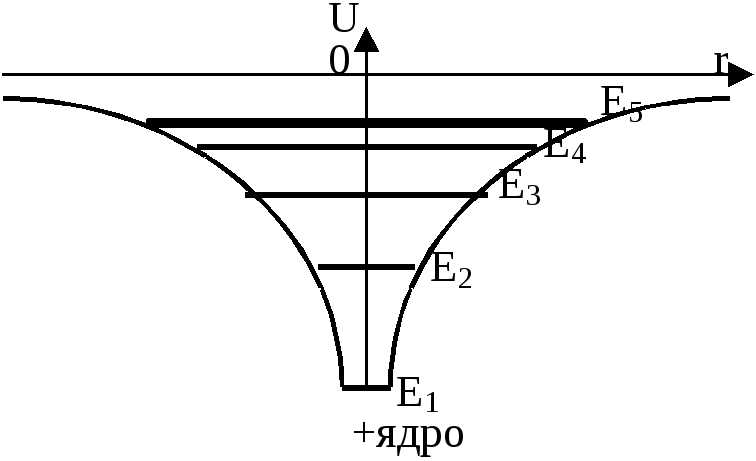
Электрон за счет туннельного эффекта может кратковременно выйти за пределы ямы, (за границы), но затем обязан вернуться в нее обратно. Поэтому в квантовой теории говорят, что электрон вращается не по орбитам, а как бы размазан в пространстве в виде облака вероятности его различных местонахождений.
Стационарное уравнение Шредингера для электрона в атоме водорода имеет вид:
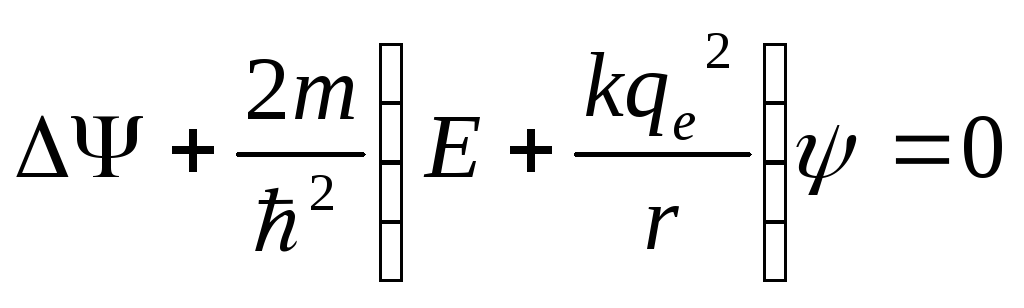
В силу наличия сферической симметрии потенциальной энергии, уравнение Шредингера целесообразно записать и решать в сферической системе координат r, , . Оператор Лапласа в сферических координатах запишется так:
= 2 /x2 + 2 /y2 + 2 /z2 = 1/r2 /r(r2 /r) + (1/r2sin ) /(sin /) + (1/r2sin2 )2 /2
И уравнение Шредингера:
[1/r2
/r(r2
/r)
+ (1/r2sin
)
/(sin
/)
+ (1/r2sin2
)2/2]
+ (2m/![]() 2)(Е
+ kqе2/r)
= 0
2)(Е
+ kqе2/r)
= 0
Представляем - функцию в виде произведения трех сомножителей с разделенными переменными r, , : ( r, , ) = R(r) () Ф(). Решаем уравнение Шредингера методом разделения переменных. Возможность такого разделения доказывается в процессе решения.
После подстановки выражений для потенциальной энергии и волновой функции электрона в атоме водорода в уравнение Шредингера, оно распадается на три уравнения, каждое из которых записано для своей сферической координаты:
1) R(r) = 1(n, l); 2) () = 2(l, m); 3) Ф() = 3(m).
В этих уравнениях появляются квантовые числа n, l, m, как параметры при решениях соответствующих уравнений.
Решив три уравнения,
получаем выражение для полной энергии
электрона в атоме водорода, которая
квантуется: Еn
= - k2mqе4/2n2![]() 2.
Это выражение совпадает с полученным
ранее в полуклассической теории Бора.
Напомним, что Бор, и позднее Зоммерфельд,
постулировали введение квантовых чисел
в теорию. Здесь же, в квантовой теории,
квантовые числа вводятся не "вручную",
а вытекают естественным образом в
результате решения уравнения Шредингера.
Четвертое квантовое число – спиновое,
в нерелятивистском уравнении Шредингера
не появляется. Оно вытекает из более
общего, релятивистского уравнения
Дирака.
2.
Это выражение совпадает с полученным
ранее в полуклассической теории Бора.
Напомним, что Бор, и позднее Зоммерфельд,
постулировали введение квантовых чисел
в теорию. Здесь же, в квантовой теории,
квантовые числа вводятся не "вручную",
а вытекают естественным образом в
результате решения уравнения Шредингера.
Четвертое квантовое число – спиновое,
в нерелятивистском уравнении Шредингера
не появляется. Оно вытекает из более
общего, релятивистского уравнения
Дирака.
Главное квантовое
число n и в
квантовой, и в классической теории
определяет полную энергию электрона в
атоме водорода: Еn
= - k2mqе4/2n2![]() 2.
2.
Орбитальное (азимутальное, побочное) квантовое число l, по Бору-Зоммерфельду, определяло форму орбиты электрона (ее отличие от круговой орбиты, ее "эллиптичность"). В квантовой же теории это число определяет форму электронного облака и численно - момент импульса электрона в нем:
![]() .
.
Число l = 0, 1, 2, … (n - 1) изменяется, начиная с нуля, а у Бора с 1. При l = 0, L = 0 - нет вращения. Электронное облако имеет конфигурацию сферы. Такое состояние, называемое S - состоянием, в классической теории невозможно. Там орбиты были плоскими, и сферически симметричный случай был невозможен. Состоянию с нулевым значением момента импульса в теории Бора соответствовало бы прямолинейное движение электрона вдоль диаметра атома.
Магнитное квантовое число m у Бора - Зоммерфельда определяло ориентацию эллиптической орбиты электрона в пространстве, а в квантовой теории - ориентацию электронного облака в пространстве и численно - проекцию L момента импульса на некоторое выделенное направление z:
Lz
= m![]() ,
где m = 0,
1,
2, …
l.
,
где m = 0,
1,
2, …
l.
Для l = 0 (S - состояние) и m = 0 - сферическая симметрия, нет никакой избранной симметрии в пространстве, то есть каких-либо выделенных в нем направлений.
Рассмотрим поподробнее 1S - состояние – простейший, сферически симметричный случай распределения плотности вероятности в пространстве. Это состояние является стационарным невозбужденным. В нем волновая функция (r, , ) = (r) - не содержит зависимости от угловых координат и , и уравнение Шредингера запишется так:
 .
.
Решение ищем в
виде
![]() - простейшей сферически симметричной
функции. Подставив
- простейшей сферически симметричной
функции. Подставив
![]() в уравнение Шредингера, получим:
в уравнение Шредингера, получим:
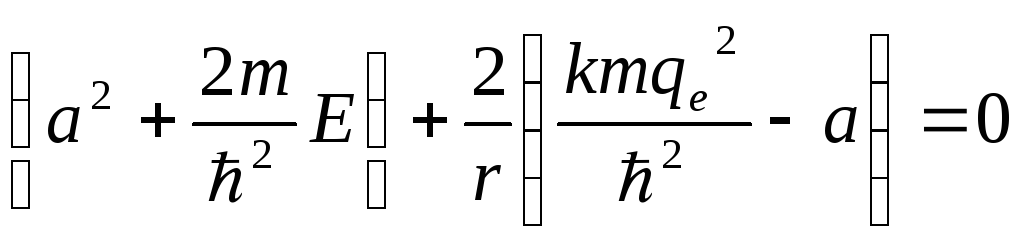
Полагаем равными нулю каждое из слагаемых по отдельности:
![]() и
и
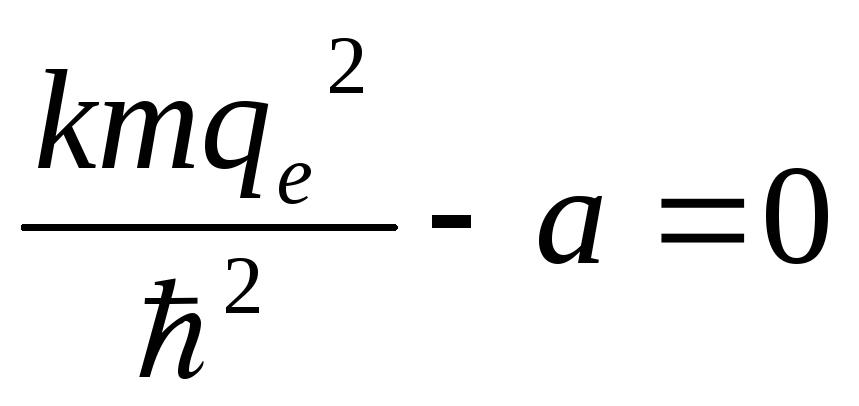 ;
;
![]() и
и
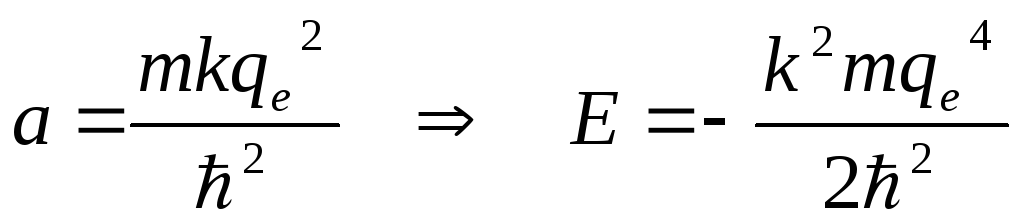 .
.
В итоге для энергии
электрона в 1S - состоянии имеем:
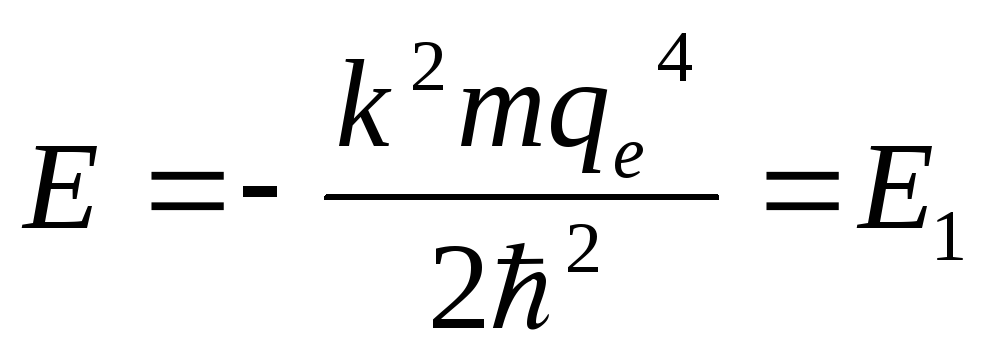 - как у Бора.
- как у Бора.
В
![]() .
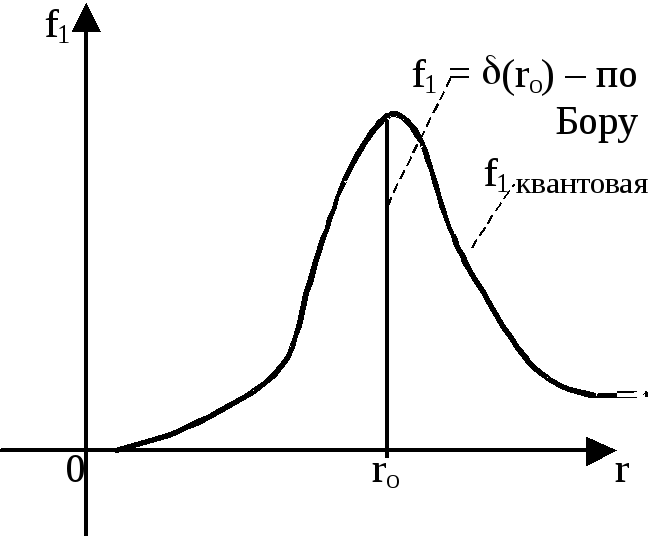
Радиальная плотность вероятности
(радиальная функция распределения):
.
Радиальная плотность вероятности
(радиальная функция распределения):
![]() - функция с максимумом. Плотность
вероятности имеет максимум, при r = rо,
который и соответствует значению радиуса
первой орбиты по теории Бора.
- функция с максимумом. Плотность
вероятности имеет максимум, при r = rо,
который и соответствует значению радиуса
первой орбиты по теории Бора.
![]() .
У Бора для радиуса
орбит было:
.
У Бора для радиуса
орбит было:
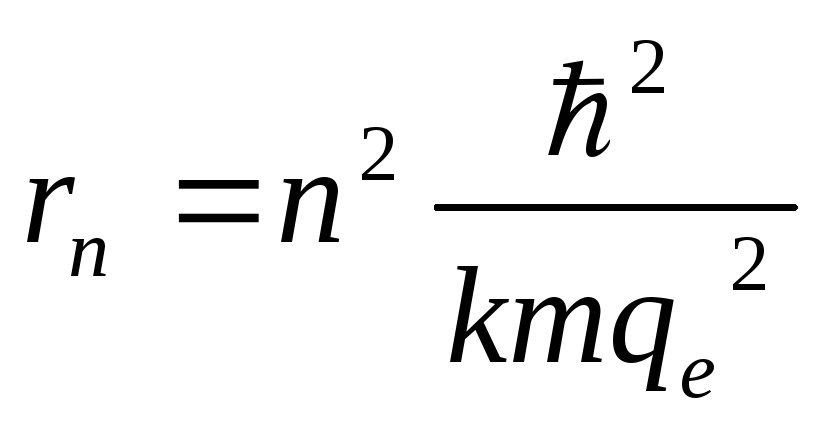 .
.
По теории Бора - Зоммерфельда электроны в атоме вращались по орбитам. В квантовой механике орбит как таковых нет, а есть целые пространственные области (облака), в которых электрон может находиться с разной вероятностью. Но у этого облака пространственного распределения вероятности местонахождения электрона есть максимумы, которые и попадают на радиусы боровских орбит. Таким образом, теория Бора есть некоторое приближение к более глубокой и полной, адекватной теории микробытия - к квантовой теории.
В невозбужденном
1S - состоянии вероятность найти электрон
в разных направлениях одна и та же,
зависящая только от радиуса. В возбужденных
состояниях (при n
1 и l
0) плотность вероятности начинает
зависеть и от углов
и .
Рассмотрим, например, состояние с
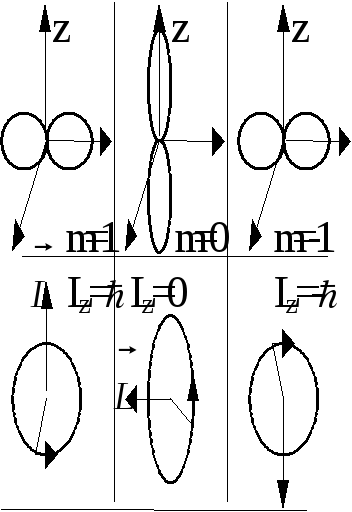
![]() = 1, называемое р - состоянием. В нем имеем
три ориентации облака вероятности с m
= 0,
1.
= 1, называемое р - состоянием. В нем имеем
три ориентации облака вероятности с m
= 0,
1.
Для l
= 1 она изображается фигурой типа гантели.
Вдоль направления
![]() вероятность найти электрон по теории
Бора, равна нулю.
вероятность найти электрон по теории
Бора, равна нулю.
Д
![]()
Для электрона в атоме водорода, как и для гармонического осциллятора, существуют определенные правила отбора, ограничивающие число возможных переходов электрона в атоме, связанных с дипольным излучением и поглощением света. Согласно этим правилам, побочное квантовое число l может изменяться на единицу, то есть l = 1, а магнитное квантовое число m – на ноль и единицу, то есть m = 0, 1. Переходы электрона с n – го на первый уровень (серия Лаймана), то есть в 1S состояние, могут осуществлять лишь из р – состояний: nр 1S. Соответственно переходы электрона на второй уровень (серия Бальмера) могут происходить по схемам: nр 2S, nS 2р, nd 2р.
