
- •Зміст лекції
- •1.Мікробіологія як наука.
- •Значення мікробіології в підготовці медичних працівників.
- •Історія розвитку мікробіології. Вітчизняні мікробіологи, їх внесок у розвиток науки. Досягнення мікробіології в боротьбі з інфекційними хворобами. Мікробіологічна служба в Україні.
- •Досягнення мікробіології в боротьбі з інфекційними хворобами. Мікробіологічна служба в Україні.
- •Поняття про класифікацію мікроорганізмів.
- •Будова бактеріальної клітини
- •Коротка морфологічна характеристика грибів, спірохет, найпростіших, рикетсій, хламідій, мікоплазм, вірусів.
- •Поняття про хімічний склад мікроорганізмів. Основні фізіологічні процеси у бактерій. Живлення, дихання, ріст і розмноження бактерій. Умови культивування бактерій.
- •6. Характеристика поживних середовищ. Поняття про культуральні і біохімічні властивості мікроорганізмів. Бактеріологічний метод дослідження, значення для діагностики.
- •Поняття про культуральні властивості мікроорганізмів. Бактеріологічний метод дослідження, значення його для діагностики
- •Лекція № 2
- •Зміст лекції
- •1.Поширення мікробів у природі. Мікрофлора організму людини, її значення. Гнотобіологія. Циркуляція патогенних мікроорганізмів у довкіллі. Мікроекологія. Поширення мікробів у природі
- •Мікрофлора організму людини, її значення
- •Циркуляція патогенних мікроорганізмів у довкіллі. Мікроекологія
- •Вплив фізичних, хімічних і біологічних факторів на мікроби
- •Транскрипція Транскрипція Трансляція
- •5.Бактеріофаг, його природа і практичне застосування. Вплив бактеріофага на мінливість мікроорганізмів.
- •7.Вплив антибіотиків на мінливість мікроорганізмів. Побічна дія антибіотиків і методи її подолання. Антибіотикограма, її практичне застосування. Противірусні хіміотерапевтичні препарати. Антисептики.
- •Антибіотикограма.
- •Хіміотерапевтичні препарати
- •Лекція № 3
- •Зміст лекції Визначення понять "інфекція", "інфекційний процес", "інфекційна хвороба". Основні ознаки інфекційних хвороб
- •Характеристика мікроорганізмів — збудників інфекційних хвороб
- •Форми інфекційного процесу
- •Динаміка інфекційної хвороби
- •Резервуари та джерела інфекції. Механізми і шляхи проникнення мікробів у макроорганізм. Фактори інфекційного процесу
- •Форми поширення інфекцій
- •Поняття про внутрішньолікарняну інфекцію
- •Принципи діагностики інфекційних хвороб. Експериментальний метод дослідження
- •Принципи профілактики та лікування інфекційних хвороб
- •Лекція № 4
- •Зміст лекції Визначення поняття "імунітет". Види імунітету
- •Фактори природної неспецифічної резистентності
- •Види імунітету
- •Імунна система. Центральні та периферичні органи імунної системи
- •Антигени, їх властивості
- •Специфічні фактори імунітету
- •Вікові особливості імунітету
- •Реакції імунітету, їх практичне застосування
- •Лекція № 5
- •Зміст лекції
- •Класифікація вакцин. Принципи виготовлення вакцин та анатоксинів
- •Методи вакцинації. Ревакцинація
- •Сироватки. Правила введення. Серопрофілактика і серотерапія
- •Поняття про моноклональні антитіла
- •Поняття про алергію, її основні форми
- •Лекція № 6
- •Зміст лекції Загальна характеристика гноєтворних коків
- •Грампозитивні коки стафілококи
- •Стрептококи
- •Пневмококи
- •Грамнегативні коки
- •Менінгококи
- •Гонококи
- •Лекція № 7
- •Зміст лекції
- •Ешерихії
- •Сальмонели
- •Черевний тиф та паратифи аів
- •Збудники харчових токсикоінфекцій
- •Короткі дані про умовно-патогенні мікроорганізми
- •Клебсієли
- •Ієрсиніі
- •Синьогнійна паличка
- •Короткі дані про кампілобактерії і гелікобактерії
- •Лекція № 8
- •Зміст лекції Загальна характеристика збудників холери, чуми, туляремії, бруцельозу, сибірки і захворювань групи особливо небезпечних інфекцій
- •Збудник туляремії
- •Мал. 25. Збудник туляремії в чистій культурі
- •Збудники бруцельозу
- •Збудник сибірки
- •Лекція № 9
- •Зміст лекції коринебактерії дифтерії
- •Бордетели
- •Мікобактерії туберкульозу
- •Лекція № 10
- •Зміст лекції Патогенні клостридії. Неклостридіальні анаероби Конкретні цілі:
- •Збудник правця
- •Збудник ботулізму
- •Збудники газової гангрени
- •Патогенні спірохети
- •Трепонеми
- •Борелії
- •Лептоспіри
- •Лекція № 11
- •Зміст лекції рикетсії
- •Збудник ендемічного висипного тифу (тифу щурів)
- •Мікоплазми
- •Патогенні гриби
- •1 Для самостійного опрацювання
- •Збудники поверхневих мікозів
- •Збудники кандидозів (кандидамікозів)
- •Лекція № 12 Тема лекції: Віруси. Рнк-геномні віруси
- •Зміст лекції
- •Ортоміксовіруси
- •Параміксовіруси
- •Вірус епідемічного паротиту
- •Вірус кору
- •Вірус сказу
- •Пікорнавіруси
- •Віруси Коксакі
- •Віруси echo
- •Віруси гепатиту
- •Вірус гепатиту а
- •Вірус гепатиту с
- •Ретровіруси
- •Вірус імунодефіциту людини
- •Лекція № 13
- •Зміст лекції Вірус гепатиту в
- •Поксвіруси. Вірус натуральної віспи
- •Онковіруси
- •Герпесвіруси
- •Віруси простого герпесу
- •Вірус вітряної віспи
- •Цитомегаловірус
- •Вірус Епстейна—Барр
Будова бактеріальної клітини
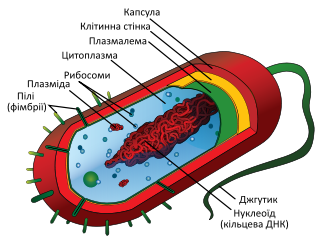
Бактерії — прокаріоти (від лат. pro — замість, грец. karyon — ядро). Клітини бактерій здатні існувати автономно, як складний організм. Структура їх клітин відрізняється від структури клітин рослин і тварин — еукаріотів (від грец. еи — повністю, karyon — ядро). Прокаріоти не мають ядерної оболонки, мітохондрій, апарату Голь-джі, ендоплазматичного ретикулуму, хлоропластів. Генетична інформація міститься в 1 молекулі ДНК, статевий шлях розмноження відсутній.
Еукаріоти можуть бути одноклітинними або багатоклітинними. У багатоклітинних всі клітини фізіологічно пов'язані і окремо існувати не можуть. Тому структура прокаріотної клітини суттєво відрізняється від клітин еукаріотів. Але загальний план будови у них подібний (мал. 2).
У будові бактеріальної клітини розрізняють три основні частини: поверхневі структури, клітинну оболонку та цитоплазму. Деякі бактерії утворюють спору, містять включення, плазміди та інші елементи.
Поверхневі структури. До них відносять капсулу, джгутики, мі-кровійки. Наявність або відсутність їх є постійною ознакою для даного виду бактерій. Це враховується під час їх ідентифікації.
Капсула (від лат. Capsula — ящик, футляр). Розрізняють мікро-капсулу, макрокапсулу, слизовий шар.
Мікрокапсулу виявляють за допомогою електронної мікроскопії. Вона представлена мукополісахаридними фібрилами.
Макрокапсула товстіша за мікрокапсулу, зберігає зв'язок з клітинною стінкою. Вона містить 98 % води, 2 % полісахаридів (Streptococcus pneumoniae), поліпептиди (Bacillus anthracis) або амі-новуглеводи (Streptococcus pyogenes) і має гелеподібну консистенцію. Через велику кількість води вона не затримує барвників, тому у разі фарбування за Буррі—Гінсом залишається безбарвною на фоні забарвленого препарату. У деяких бактерій капсули утворюються в організмі людини або тварини (збудники пневмонії, сибірки та ін.), а в деяких — як у макроорганізмі, так і на штучних поживних середовищах (Staphylococcus aureus, Streptococcus pyogenes, Klebsiella pneumoniae тощо). У патогенних мікроорганізмів капсула може оточувати одну (збудник чуми — Yersinia pestis) або дві клітини (збудник пневмонії — S. pneumoniae), навіть цілий ланцюжок клітин (збудник сибірки — В. anthracis).
Макро- і мікрокапсули захищають клітину від бактеріофагів, фагоцитів, антибіотиків та антитіл. Вони також є факторами патогенності (пневмококи, що втратили капсулу, втрачають патогенність). Капсула зумовлює антигенні властивості бактерій — містить K-антиген (капсульний антиген).
Слизовий шар. Бактерії часто виділяють велику кількість слизу, який утворює навколо них пухкий шар, здатний відділятися від клітини (збудник гонореї).
Джгутики забезпечують рухливість бактерій. Це довгі ниткоподібні структури діаметром 12—13 нм і завдовжки 6—80 мкм. Джгутики
утворені білковими часточками, які спірально чи вздовж укладені навколо пустої серцевини у вигляді циліндра. Білок, з якого складається джгутик, називається флагеліном, він відрізняється від інших білків бактеріальної клітини тим, що має здатність скорочуватись. Джгутик прикріпляється до базального тільця, яке розміщується в оболонці бактеріальної клітини (клітинній стінці і цитоплазматичній мембрані). Джгутики мають здатність обертатися навколо своєї осі за і проти годинникової стрілки.
Завдяки джгутикам відбувається хемотаксис бактерій.
Рухливі бактерії швидше наближаються до чутливих клітин макроорганізму, тому джгутики впливають на патогенність бактерій. Джгутики визначають антигенну структуру бактерій (містять Н-антиген).
Утворення джгутиків кодується генами і є постійною ознакою певного виду бактерій. Тому виявлення рухливості враховується під час їх ідентифікації. За кількістю та розміщенням джгутиків бактерії поділяють на групи (мал. 3):
монотрихи (від грец. monos — один, thrix — волосся) — один джгутик розміщується на полюсі клітини (холерний вібріон);
лофотрихи (від грец. lophos — пучок, thrix — волосся) — пучок джгутиків розміщується на одному кінці (синьогнійна паличка);
амфітрихи (від грец. amphi — з обох боків, thrix — волосся) — один або пучок джгутиків розміщується на обох кінцях (спірили);
перитрихи (від грец. peri — навколо, біля, thrix — волосся) — джгутики розміщуються на всій поверхні клітини (сальмонели, ешерихії та ін.).
Рухливість бактерій визначають за допомогою мікроскопічного методу — фазово-контрастна або темнопольна мікроскопія "роздавленої" або "висячої" краплі; та бактеріологічного методу — посів штриком у стовпчик напівщільного агару: для рухливих бактерій характерний дифузний ріст, середовище стає мутним, а нерухливі ростуть тільки вздовж уколу, середовище залишається прозорим.
Мікровійки. Окрім джгутиків поверхню бактерій вкривають мі-кровійки. Вони набагато, майже в 10 разів, коротші за джгутики, на рухливість бактерій не впливають. Розрізняють два типи мікро-нійок: 1) фімбрії, або війки; 2) кон'югативні, або донорські (F-пілі).
Фімбрії(від, англ. fimbria — бахрома) — це короткі тонкі волоски, яких може бути від 10 штук до декількох тисяч. Вони є фактором патогенності. За допомогою фімбрій бактерії прикріплюються до чутливих клітин (адгезія), де потім розмножуються (колонізація).
F-пілі (від англ. pile — волосок) — довгі тонкі ниткоподібні структури. На одній клітині їх може бути 1—2. Вони є апаратом кон'югації у бактерій. F-пілі забезпечують контакт між клітиною-донором і клітиною-реципієнтом, а також передачу спадкової інформації, що міститься в плазмідах.
Мікровійки — це білкові структури. Білки джгутиків, фімбрій і пілей різні за складом і властивостями.
Клітинна оболонка складається з клітинної стінки і цитоплазматичної мембрани.
Клітинна стінка має два шари: внутрішній (ригідний) та поверхневий (пластичний). Ригідний шар складається з пептидоглі-кану, пластичний — з ліпополісахаридопротеїнового комплексу. Крістіан Грам запропонував метод фарбування мікроорганізмів генціановим фіолетовим і розчином йоду, при цьому всі бактерії забарвлювались у фіолетовий колір. Після оброблення спиртом і промивання водою одні з них втрачали попереднє забарвлення і забарвлювалися фуксином Пфейфера в червоний колір. їх назвали грамнегативними. Мікроорганізми, які не втрачали фіолетового забарвлення, назвали грампозитивними. Ця відмінність зумовлена різним складом клітинної стінки.
У грампозитивних бактерій більш виражений ригідний шар, він складається з пептидоглікану, який є тільки у прокаріотів. Пеп-тидоглікан має структуру молекулярної сітки. У клітинній стінці грампозитивних бактерій його міститься 5—6 шарів. Пептидоглі-кан пронизаний тейхоєвими (від грец. teichos — стінка) кислотами. Вони є головними поверхневими антигенами грампозитивних бактерій. Клітинна стінка більшості грампозитивних бактерій не містить ліпідів, але деякі (збудник туберкульозу) мають їх багато — понад 40 % . Ці ліпіди токсичні для макроорганізму. Вміст білка дуже різний. Білки зумовлюють антигенні властивості, а також є факторами патогенності.
У грамнегативних бактерій виражені пластичний і ригідний шари. Ригідний шар тонкий, складається з одного, рідко з двох шарів пептидоглікану, що становить 5—10 % маси всієї клітинної стінки. До складу пластичного шару входять ліпополісахарид, ліпопротеїди, поверхнева мембрана, які мозаїчно переплітаються між собою. Ліпополісахарид запускає синтез близько 20 сполук, що виявляють хвороботворну дію на макроорганізм. Він спричинює ознаки загальної інтоксикації: підвищення температури тіла, зниження артеріального тиску, загальну слабкість, головний біль, втрату апетиту тощо. Ліпополісахарид ще називають ендотоксином, він розміщений у клітинній стінці і не виділяється назовні із живої клітини. Він є чужорідним для макроорганізму (О-антиген), тому спричинює утворення антитіл.
Поверхнева мембрана входить до складу клітинної стінки грамнегативних бактерій. Вона має, як будь-яка біологічна мембрана, два шари фосфоліпідів. У зовнішньому її шарі частина фосфоліпідів заміщена молекулами ліпополісахариду та білків (їх понад 10 видів). Білки є рецепторами для фагів, коліцинів, донорських мікровійок. Поверхнева мембрана — бар'єр, через який не можуть проникати великі молекули речовин, а це забезпечує один з механізмів стійкості грамнегативних бактерій до антибіотиків.
Патогенних бактерій більше серед грамнегативних.
Відмінності між грамнегативними та грампозитивними бактеріями
Грамнегативні бактерії |
Грампозитивні бактерії |
Клітинна стінка чітко розділяється на два шари |
Клітинна стінка має однорідну структуру |
Забарвлюються за Грамом у червоний колір |
Забарвлюються за Грамом у фіолетовий колір |
Клітинна стінка тонша, складніша за структурою |
Клітинна стінка товща, простіша за структурою |
Вміст петидоглікану — 5—10 % маси клітинної стінки |
Вміст пептидоглікану — до 90 % маси клітинної стінки |
Малочутливі до йоду, пеніциліну, лізоциму |
Чутливі до йоду, лізоциму, пеніциліну (мішенню є пептидоглікан) |
Клітинна стінка містить ліпополісахарид (ендотоксин) |
Більшість мікроорганізмів утворюють екзотоксин. Не містять ліпополісахарид |
Не містять тейхоєвих кислот |
Містять тейхоєві кислоти |
Роль клітинної стінки:
зберігає форму клітини (у разі втрати клітинної стінки паличкоподібні бактерії набувають форми кульки);
бере участь у рості та поділі клітини;
захищає від дії факторів навколишнього середовища та макрофагів (знижує фагоцитарну активність макрофагів, гальмує їх міграцію);
є фактором патогенності;
визначає антигенну структуру бактерій (ліпополісахарид, тейхоєві кислоти);
врівноважує осмотичний тиск.
Клітинну стінку можна зруйнувати. Лізоцим руйнує лише пеп-тидоглікан клітинної стінки, а пеніцилін перешкоджає його утворенню. При цьому у грамнегативних мікроорганізмів поверхнева мембрана (або її частина) і ліпополісахарид залишаються неушко-дженими. Бактерії, клітинна стінка у яких частково зруйнована, називаються сферопластами. Після оброблення грампозитивних бактерій ферментами, які руйнують пептидоглікан, утворюються протопласти — структури, у яких повністю зруйнована клітинна стінка. Протопласти і сферопласти інакше називаються L-формами бактерій, оскільки вперше були виявлені в інституті ім. Лістера (L — перша літера назви інституту). Цю мінливість бактерій назвали L-трансформацією. L-форми мають схожі властивості незалежно від виду бактерій, з яких вони утворилися. Вони подібні за морфологічними (мають форму кульки, нитки, волокна тощо), тинкторі-альними (всі грамнегативні), культуральними властивостями (мають дрібні колонії типу виливної яєчні), за антигенною структурою (втрачають О- і К-антигени); мають знижену вірулентність (втрачають фактори адгезії, інвазії, токсини), нечутливі до хіміотерапевтичних препаратів і антитіл.
L-трансформація буває зворотною та незворотною. При зворотній зберігається генетичний контроль за синтезом клітинної стінки, тому за сприятливих умов відбувається реверсія (від лат. reuersio — повернення) L-форм — відновлення клітинної стінки і основних біологічних властивостей, у тому числі і патогенності. При незворотній L-трансформації втрачається генетичний контроль за синтезом клітинної стінки, утворюються стабільні L-форми бактерій, які дуже схожі на мікоплазми.
L-трансформація бактерій може відбуватися як in vitro (поза макроорганізмом), так і in vivo (в організмі людей і тварин) під впливом антибіотиків (препарати пеніцилінового ряду, цефалоспорини, ван-коміцин), ферментів (лізоцим), антибактеріальних антитіл тощо.
Перетворення патогенних бактерій на L-форму в організмі людини призводить до тривалої персистенції, переходу гострої форми інфекції в хронічну, що супроводжується рецидивами хвороби (відновленням симптомів).
Цитоплазматична мембрана покриває цитоплазму. Вона напівпроникна (одні речовини пропускає, інші — ні) і є осмотичним бар'єром. На ній виявлені системи, які беруть участь у синтезі різних сполук, у тому числі ферментів і токсинів (від грец. toxikon — яд). Через цитоплазматичну мембрану здійснюється транспорт речовин у клітину та із клітини. Унаслідок інвагінації (вдавлювання) цитоплазматичної мембрани утворюютьсяТйгезосоми, які беруть участь у синтезі клітинної стінки, поділі клітини і спороутворенні. Між клітинною стінкою та цитоплазматичною мембраною у грам-негативних бактерій периплазматичний простір. Він заповнений ферментами (фосфатази, рибонуклеази та ін.), які зумовлюють взаємодію цитоплазматичної мембрани і клітинної стінки.
Цитоплазма — складна колоїдна система, яка містить нуклеоїд, плазміди, рибосоми та інші включення.
Нуклеоїд (хромосома, геном) є еквівалентом ядра еукаріот, але не має власної мембрани. Це двониткова ДНК, замкнута в кільце. За аналогією з еукаріотами її називають хромосомою (вона одна). Кількість закодованої інформації різна у різних видів бактерій (2500— 3000 генів). Перед поділом нитки ДНК розходяться і кожна добудовується другою ниткою за законом комплементарності. Дочірні клітини успадковують ознаки материнської.
ßL Плазміди — додаткова позахромосомна кільцева молекула ДНК. Нині плазміди розглядають як найпростіші організми, що не мають власної системи синтезу білка та систем іммобілізаціїтзнергії. Вони паразитують на бактеріях, наділяючи їх певними властивостями (стійкість до антибіотиків, вірулентність тощо). Плазміди передаються під час кон'югації та поділу бактеріальних клітин.
Рибосоми. На рибосомах відбувається синтез білка. Вони складаються з двох субодиниць (одиниць Свеберга): 50S і 30S, які об'єднуються в рибосому 70S. Бактерицидні антибіотики (левоміцетин, тетрациклін, стрептоміцин) пригнічують синтез білка тільки на рибосомах 70S і не порушують його синтез на рибосомах людей і тварин — 80S.
Запасні речовини (включення). До них відносять крохмаль, глікоген у грибів роду Candida, воски — у мікобактерій. Вони мають діагностичне значення (наприклад, у коринебактерій дифтерії — волютин, який вперше був виявлений у Sarcina volutans — звідси його назва).
Спора — стійка форма бактерій Утворюється переважно паличкоподібними бактеріями, дуже рідко — коками та звивистими. Вона є ущільненою ділянкою цитоплазми з нуклеоїдом, яка містить ліпіди, мінімальну кількість води(40). Велику кількість кальцію та інші сполуки, яких немає у вегетативних клітинах (наприклад, дипіколінову кислоту, завдяки якій спора термостійка). Спора вкрита щільною багатошаровою оболонкою.
Утворюються спори протягом 18—20 год, проростають протягом 4—5 год.
Спори ніколи не утворюються в тканинах живого макроорганізму.Убактеріальній клітині спора може розміщуватися:
центрально, наприклад у збудника сибірки;
термінально (від лат. terminalis — кінцевий), яку збудника правцю; субтермінально (від лат. sub — під, біля, terminalis кінцевий;ближче до одного кінця), як у збудника ботулізму.
Спори стійкі до дії високих температур (спори збудника ботулізму витримують кип'ятіння протягом 1—6 год), висушування, зміни рН, впливу дезінфекційних розчинів. Упродовж десятків і навіть сотень років спори можуть зберігатися в несприятливих умовах навколишнього середовища. Це слід враховувати під час вибору методів знезараження. Матеріал, що містить спори, знезаражують в автоклаві за температури 127—132 °С або в сухожаровій шафі за температури 160—180 °С.
Спороутворення кодується генами, тому є постійною ознакою певного виду бактерій. Це слід враховувати під час ідентифікації бактерій.
Форми бактерій, що не культивуються (ФБН). У грамнегатив-них бактерій, що не утворюють спор, існує особливий пристосувальний стан, який фізіологічно аналогічний до такого у цист (від грец. kystis — міхур). Цей стан характеризується тим, що такі форми бактерій не здатні розмножуватись на поживному середовищі, але зберігають власну життєздатність. У разі потрапляння в макроорганізм вони відновлюють здатність швидко рости і розмножуватись. В навколишньому середовищі їхні метаболічні процеси пригнічені, тому вони можуть тривалий час зберігатися в несприятливих умовах. Так, збудник холери в стані ФБН у забруднених відкритих водоймах зберігається роками, підтримуючи несприятливу епідемічну ситуацію в регіоні.
У формі ФБН збудників хвороб неможливо виявити традиційними методами, що утруднює ліквідацію спалаху інфекції. Виявляють ці форми бактерій за допомогою молекулярно-генетичних методів (ланцюгової полімеразної реакції — ЛПР).
Вивчення морфології мікроорганізмів лежить в основі мікроскопічного методу діагностики інфекційних хвороб, який ґрунтується на виявленні бактерій у патологічному матеріалі за допомогою мікроскопа. При цьому можна визначити морфологічні та тинкторі-альні ознаки. Цей метод застосовують для підтвердження клінічного діагнозу сифілісу, гонореї, туберкульозу тощо або постановки орієнтовного діагнозу у разі захворюваності на дифтерію, правець, анаеробну газову інфекцію.
