
- •Э.Х. Процессами называются процессы взаимного превращения электрической и химической энергий.
- •Водородный электрод
- •Кислородный электрод
- •Форма записи гэ: ZnZnSo4 CuSo4 Cu
- •Изотерма Вант-Гоффа
- •Уравнение Нернста:
- •Изучает скорость и механизм протекания электродных процессов
- •Еконц Еэл/х
- •I пред – предельная плотность тока
Особенность:
влияние потенциала на скоростьИзучает скорость и механизм протекания электродных процессов






отклонение
потенциала от равновесного под действием
электрического тока
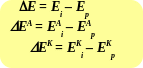
Согласно закону Фарадея, ток (I) пропорционален количеству вещества, прореагировавшему на электродах в единицу времени, т.е. скорости электрохимической реакции:
![]() значение
I
для
оценки скорости
значение
I
для
оценки скорости
При одном и том же потенциале в зависимости от площади электрода могут быть разные токи:
i = I/S - плотность тока
Строят график зависимости Е =f(i) –
поляризационные кривые



В гальваническом элементе при прохождении электрического тока
Е анода становится более положительным
Е катода – более отрицательным
U - уменьшается
![]()
U – напряжение ГЭ;
I(r1 + r2) - омическое падение напряжения;
r1- сопротивление в проводниках с электронной
проводимостью (проводники 1-го рода);
r2 - сопротивление в электролит (проводник 2-го рода);





возникает за счет изменения концентрации
реагентов в приэлектродном слое при
прохождении тока
обусловлена замедленностью собственно
электрохимической реакции
Еконц Еэл/х
По уравнению Нернста Е пропорционален логарифму активности (концентрации) ионов
![]()
аs,v – активности ионов в приэлектродном слое(S)
или в объеме раствора (V)
С увеличением i возрастает концентрационная поляризация
Диффузным
называется
тонкий слой около поверхности электрода,
в котором не
происходит
перемешивания
жидкости
![]()
![]()
I пред – предельная плотность тока
D – коэффициент диффузии
реагента
- толщина диффузного сло
Для
уменьшения Еконц
следует:
↑ D;
↑ Сv;
↓
; перемешивать
Зависимость между перенапряжением и плотностью тока:

Еэл/х
= а
+ в • lgi
Коэффициенты а, в – зависят от природы реакции,
температуры, рН, Sэлектродов
и определяются из графиков
зависимости Еэл/х = f(lgi)
Для
уменьшения Еэл/х
следует:
↑ Т; ↑
Sэлектродов
; ↓ Среагента
;
использовать
электроды-катализаторы
Поляризация приводит к бесполезной трате электрохимической энергии, т.к. снижает полезное напряжение химического источника тока
С целью увеличения напряжения необходимо:
Э ДС ГЭ;
п оляризацию;
о мические потери, для чего:
- уменьшить ток,
- уменьшить r1 и r2
(за счет расстояния между электродами, использовать добавки увеличивающие электропроводность электролита)
В некоторых случаях, благодаря поляризации, исключается возможность протекания нежелательных побочных процессов.
