
- •Рахмонов джамахон ахмадович объективизация диагностики и контроля лечения пареза желудочо-кишечного тракта при разлитом
- •Оглавление
- •Глава il материалы и методы исследования 37
- •Глава IV. Результаты лечения iiape3a желудочно-кишечного тракта при разлитом перитоните с использованием традиционных методов
- •Глава V. Результаты лечения пареза желудочно-кишечного тракта при разлитом перитоните с применением низкоамплитудной
- •Введение
- •Глава I.
- •13. Принципы лечения пареза желудочно-кишечного трактапри разлитом перитоните.
- •2.2. Традиционные методы лечения пареза желудочно-кишечного тракта при разлитом перитоните (группа сравнения).
- •Статистическая'обработка результатов исследования
- •Расчет погрешностей результатов измерения*
- •Из 3 основных частей.
- •Глава ul диагностика пареза желудочно-кишечного тракта при различных фазах разлитого перитонита
- •107 Выводы
2.2. Традиционные методы лечения пареза желудочно-кишечного тракта при разлитом перитоните (группа сравнения).
Всем больным группы сравнения (33 пациента) проводилось комплексное лечение включающее в себя: обезболивание, санацию и дренирование брюшной полости, интубацию кишечника, антибактериальную и деток-сикационную терапию, коррекцию гемодинамики, (форсированный диурез и плазмаферез), введение препаратов улучшающих перистальтику кишечника, антихолинэстеразных препаратов, новокаиновые блокады.
Методы оперативного лечения заключались в выполнении-диагностической лапароскопии, лапароскопической аппендэкгомии, ушивании перфо-ративных язв желудка и 12п кишки, ликвидации повреждений кишечника, санации и дренировании брюшной полости. В зависимости от фазы перитонита, характера и распространенности экссудата произведено: ланаротомия, аппендэктомия, ушивание перфоративных язв, устранение кишечной непроходимости, интубация кишечника, вскрытие и дренирование сальниковой сумкиг санация и дренирования брюшной полости. При наличии желчека-
F
менной болезни - холецистэктомия.
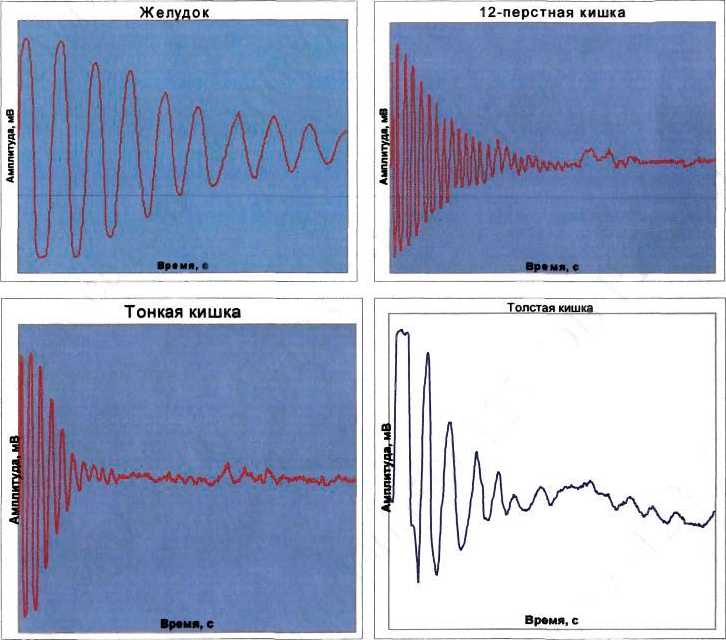
С момента поступле!тия больных в стационар производилось снятие энтерограмм с помощью селективного электрогастроэнтероколонографа (СЭГЭКГ) до операции, а также в раннем послеоперационном периоде на 1, 3-5 и 6-8 сутки. Кроме этого снимали энтерограммы у 20 здоровых лиц3 с це
Значения
параметров:
Таблица 4,
Показатели га-строэнтерокол оно-грамм в мкВ |
Желудок |
12-перстная кишка |
Тонкая кишка |
Толстая кишка |
Максимальная амплитуда Uo, мкВ |
|
49,6±3,2 |
52Д)±4,2 |
58,8±4,8 |
Период сокращенияHfy секунд |
0,81*0,06 |
1 J3±0,14 |
1,76*0,16 |
0,62*0,28 |
Уменьшение до ЭдБ Q,секунд |
77,3±2,17 |
94519±6,48 |
Э4,5б±1,47 |
109,39±6,7 |

 ью
получения нормальных показателей и
сравнения их с показателями больных
пациентов.
ью
получения нормальных показателей и
сравнения их с показателями больных
пациентов.
4" . <F ^
Всего было произведено снятие энтерограмм и перевод в цифровое значение у 69 пациентов; 33- контрольной группы! 36 - основной группы.
2.3,
Лечение
пареза желудочно-кишечного тракта у
больных разлитым
перитонитом с применением низкоамплитудной
электростимуляцни, мониторного
толстокнщечного сорбцнонного диализа
и парентеральное питание препаратом
дипептивен (основная группа)*
В
основную группу вошли 36 пациентов.
ДаЗшя группа разделена на*">>
две
подгруппы: первая - из 20 пациентов,
которым наряду традиционными
методами
лечения производилась низкоамплитудная
электростимуляция и монйторный толстокип
1©чный
сорбционный диализ: вторая - из 16
пациентов, которым данные лечебные
мероприятия дополнялись парентеральным
питанием с использованием препарата
дипептивен.
Все
операции, как и в контрольной группе,
выполнялись под эндотра-хеальным
наркозом- Все дальнейшие этапы операции
полностью соответствовали методике
изложенной в контрольной группе.
*s
Монйторный
толстокишечный сорбционный диализ
проводился с ПОМОЩЬЮ аппарата
AMQK-2
(Кулик Я:П., авторское свидетельство
№3621665/28-14, 1985, патент 4А 61 м 9/00), с
использованием лигносорба -энтеросорбента,
созданного и выпускаемого в центре
сорбционных технологий СПб МАЛО.
Лигносорб - препарат, разработанный на
основе полифепа-
.
на, выпускается в виде пасты и при
растворении легко превращается в сус-
,
пензию.
Л.
43 ' '•^у При относительно небольшой удельной площади (15-20 м 2/л) лигао-сорб, как и все лигшшовые сорбенты, имеет на своей пористой поверхности значительное количество функциональных групп, участвующих в процессе сорбции. Частицы сорбента имеют размеры 30-70 мкм, что позволяет им долго удерживаться во взвешенном состоянии в жидких средах и свободно проходить по зонду, не засоряя его отверстия.
Аппарат предназначен для проведения мониторной очистки толстой кишки путем нагнетания в нее через специальный 4-х канальный зонд> жид-
кости и одновременного удаления содержимого кишечника с поддержанием заданной температуры нагнетаемой жидкости, а так же контроля внутрики-шечного давления. Зонд длиной 60-70см; из полихлорвинила, вводится в ректосигмоидный отдел толстой кишки через анальное отверстие. Зонд состоит из 4-каналов; для подачи жидкости в толстую кишку, для се удаления, для введения сорбента или других лекарственных растворов и контроля внутрикишечного давления.
Весь сеанс проведения МТКСД состоит из 2 этапов - подготовительного и основного. Подготовительный этап обеспечивается продвижением no-прямой'кишке зонда, дистальный конец которого поворачивают направо, со— ответственно направлению дистальной части сигмовидной кишки, после чего зонд проводится через изгиб сигмовидной кишки.
В качестве раствора промывающего кишку использовали кипяченую воду нагнетаемую в кишечник через подающий канал под контролем1 внутрикишечного давления. Управляемость процессами подачи, жидкости и отсоса создает условия для образования пульсирующего потока жидкости, что улучшает качество выведения токсических метаболитов из толстой кишки, образования гидромеханического раздражения стенки кишечника, улучшая в ней процессы кровообращения и лимфообращения и, тем самым, стимулируя кишечную перистальтику.
Второй этап МТКСД осуществляется с использованием в качестве промывной жидкости взвеси мелкодисперсного сорбента, обладающего спо
собностью связывать значительный спектр веществ с различной молекулярной массой. В подготовленную и очищенную от токсических метаболитов слизистую оболочку стенки толстой кишки через ирригационный канал зонда подается взвесь лигносорба, приготовленная перед процедурой. Взвесь готовится из 15% пасты препарата (из расчета 1-2 г/кг массы тела больного) путем взбивания миксером или механическим перемешиванием в 5л раствора Рингера. Процесс МТКСД осуществляется в режиме подачи раствора со ско-фостьгаЛ50г250_мл_/ мин-.при_внутрикишечном давление 8 - 10мм. рт. ст. Общее время процедуры составляет 30-35 мин.
Количество используемой жидкости достигает в среднем Юл. В режиме введения и выведения жидкости и взвеси сорбента в растворе Рингера на этапах проведения МТКСД необходимо стремиться к тому, чтобы количество выведенного из кишки содержимого было больше или равно количеству введенной жидкости и взвеси.
При большой экспозиции взаимодействия со слизистой оболочкой толстой кишки, создается активный транспорт токсических метаболитов из крови в просвет кишечника с последующей их эвакуацией с удаляемой жидкостью (Мирошниченко А.Г., Кацадзе М,А., Изотова О.Г., 1988-1996).
На 1-е, 3-й, 5-е сутки после операции для улучшения моторики желудочно-кишечного тракта нами был использован комбинированный метод, включающий в себя мониторный толстокишечный диализ, низкоамплитудная
+
электростимуляция кишечника и парентеральное питание препаратом^ ди-пептивен.
В 100 мл дипептивена содержится^ 20 г К(2)-Е-аланил-Ь-глутамина, что соответствует 13,46 г L-глутамина и 8,20 г L-аланина. Теоретическая ос-молярноеть составляет 921 мосмоль/л- L-алаиин и L-глутамин ковалентно связаны пептидной связью, аналогичной существующей в природных белках. После внутривенного введения дипептид подвергается эндогенному гидролизу с образованием свободных аминокислот, которые поступают в пул аминокислот организма и используются в качестве энергетических и пластических
субстратов. Препарат можно добавлять к растворам аминокислоты или глюкозы либо вводить параллельно этим растворам. Суточная доза составляет 1,5-2 мл на 1 кг массы тела. Форма выпуска - флаконы по 50 мл и 100 мл. Средняя суточная доза составляет 1,5—2,0 мл дипептивена на 1 кг массы тела, что примерно равно 0,3-0,4 г дипсптида или 0,2-0,3 г глутамина на 1 кг массы тела. Эта доза соответствует 100-150 мл дипептивена в день для больного с массой тела 70 кг.
~ 2.4..Методь1_исследодадия. ____
Помимо изучения сравнительных клинических данных, оценка течения заболевания проводилась с использованием лабораторных исследовании состава периферической крови. Все показатели в группах больных оценивались до операции, а также в раннем послеоперационном периоде на 1,3-5 и 6-8 сутки.
Прежде всего, оценивались данные общепринятого клинического обследования (жалобы, данные анамнеза, общее состояние больного, температура тела, пульс, артериальное давление, объем живота, перкуторные данные, наличие перистальтики и шума плеска при аускультации, симптомы раздражения брюшины, состояние мотор&ки желудочно-кишечного тракта).
Все клинические и биохимические анализы крови и мочи проводили по общепринятым унифицированным методикам. Для определения содержания в плазме крови ВНиСММ была использована спектрометрическая методика (Габрислян Н.Н. и соавт., 1981) в модификации М-Я.Малаховой и соавт., 1989;
Перед процедурой пробирки маркировались и добавлялся- гепарин из расчета 0,05 мл (при концентрации гепарина 5000 БД в 1 мл) на 5 мл крови.
Методика заключается в осаждении крупномолекулярных частиц плазмы крови и эритроцитов раствором трихлоруксусной кислоты (ТХУ) 150г/л и регистрации спектральной характеристики водного раствора супернатанта в зоне длин волн от 238 до 310 нм. Для определения находящихся в и на эритроцитах ВНиСММ эритроцитарную массу доводили до исходного объема
крови изотоническим натрия хлорида, перемешивали, отбирали 1 мл и производили осаждение ТХУ в концентрации 150 г/л, как и при исследовании плазмы крови. Через 5 минут центрифугировали при 3000 об/мин в течение 30 мин. Супернатант разводили дистиллированной водой в соотношении 1:9 и фотометрировали против контроля. Для определения ВНСММ в моче, последнюю разводили в 10 раз, осаждали в растворе ТХУ 150г/л в тек же соотношениях, что и плазме, затем фотометрировали. Разведение супернатанта мочи такое же, как плазмы или эритроцитов. Полученные значения выражались в условных единицах (усл. ед.) по формуле:
-ш
J
BI 1иСММ11л = (Егзк+ Е242+ E2j6+- ■ .+ l^a) х 4 усл.ед.
ВНиСММ^- (Разе* Е242+ Еш+.. .+ E2gg) х 4 усл.ед.
ВНиСММчочи= (Е^в-Ь Fan* ЕМб+...+ E29s) х 4 усл.ед. Для оценки степени токсемии наряду с другими показателями использовали лейкоцитарный индекс интоксикации (ЛИИ), который нашел широкое применение в качестве показателя интоксикации у больных с различными воспалительными заболеваниями (Карабанов Г.Н., 1989). Метод основан, на изменениях в качественном составе клеточных-элементов гемограммы и вычисляется по ►формуле (Кальф-Калиф Я.Я., 1941):
(4хМИ + ЗхЮ + 2хП + С)х(Г1л+П (Мо + Л)х(Э+1)
где: Ми - миелоциты, Ю - юные, П - палочкоядерные, С - сегментоя-дерные, Пл - плазматические клетки Тюрка, Мо - моноциты, Л - лимфоциты, Э - эозинофилы.
Полученные значения выражались в условных единицах.
Повышение ЛИИ связано с исчезновением эозинофилов, увеличением количества сегментоядерных, палочкоядерных, плазматических клеток и снижением количества лимфоцитов и моноцитов.
