
- •Изложите товарные и определяющие технологию свойства формальдегида, область применения.
- •Укажите сырьевые источники для получения формальдегида.
- •Кратко охарактеризуйте современные промышленные способы получения формальдегида.
- •Опишите физико-химические закономерности процесса получения формальдегида путем каталитического окисления метанола кислородом воздуха. Определите тип процесса.
- •Изобразите и опишите аппаратурно-технологическую схему.
- •Рассчитайте и составьте материальный баланс процесса получения choh.
- •Работа над ошибками.
- •Литература
Работа над ошибками.
Рассчитаем часовую производительность СНОН:
![]() кг/час,
– производительность по формальдегиду,
кг/час,
– производительность по формальдегиду,
где (365-30)24=8040 ч – количество рабочих часов в год, т.к. 365 дней в году, 30 дней ремонт установки.
Рассчитаем массу СН3ОН, расходуемую на получение целевого продукта, реакции (1,2):
,
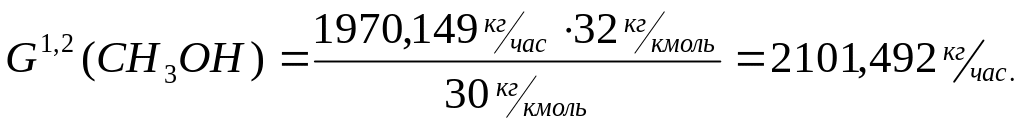
где М(HCOH)-молярная масса формалина,
где М(CН3OH)-молярная масса метанола.
![]()
![]()
На (1) реакцию расходуется 64,88% - 1363,448 кг/час,
На (2) реакцию расходуется 35,12% - 738,044 кг/час.
Рассчитаем массу СН3ОН, подаваемую в контактный аппарат:
2101,492 кг/час СН3ОН расходуется на получение целевого продукта, а
т.к. реакции 1,2, а конверсия по условию Кпол=89,71%, тогда
![]() -
количество метанола идущего на реакции
(1,2), с учетом
Кпол.
-
количество метанола идущего на реакции
(1,2), с учетом
Кпол.
Т.к. 2342,539 – расходуется на получение целевых , а конверсия условию Кобщ=92,51%, тогда
![]() -
количество метанола подаваемое в
контактный аппарат, с учетом Кобщ,
идущего на реакции (1-4)
-
количество метанола подаваемое в
контактный аппарат, с учетом Кобщ,
идущего на реакции (1-4)
0,9251 – общая конверсия на загрузку метанола,
0,8971 – полезная конверсия на загрузку метанола
Рассчитаем расход СН3ОН на побочные реакции (3,4) и «проскок» метанола:
![]() -
количество метанола расходуемого на
побочные реакции (3,4).
-
количество метанола расходуемого на
побочные реакции (3,4).
![]() -
количество метанола которое
не вступило в реакцию (1-4) – «проскок».
-
количество метанола которое
не вступило в реакцию (1-4) – «проскок».
Доля участия СН3ОН на реакции(3,4):
По соотношению СО2:СН4 как 6,7:1, рассчитаем количество метанола расходуемого на реакцию (3) и реакцию (4)

![]() -
расход СН3ОН4
идущий на реакцию (4), тогда расход СН3ОН3
идущий на реакцию (3) равен
-
расход СН3ОН4
идущий на реакцию (4), тогда расход СН3ОН3
идущий на реакцию (3) равен
![]()
Определим расход остальных компонентов исходя из уравнений реакций:
Расход технического воздуха на реакцию:
.


![]() .
.
Количество образовавшейся воды:



Т.к. метанол подается в контактный аппарат в разбавленном состоянии Н2О, то:
![]() -
количество воды в метаноле по условию.
-
количество воды в метаноле по условию.
![]() .
.
Количество образовавшегося водорода:
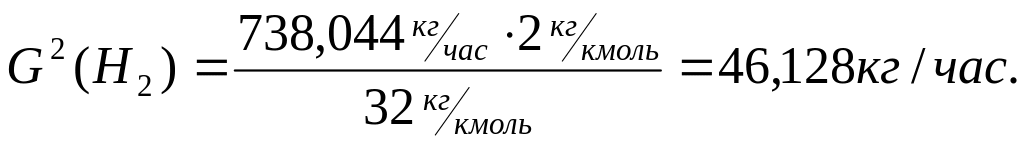
Количество затраченного водорода:

Количество образовавшегося углекислого газа:

Количество образовавшегося метана:

Полученные расчеты сведем в таблицу материального баланса:
Приход |
расход |
||||
вещество |
% масс |
кг/час |
вещество |
% масс |
кг/час |
СН3ОН |
70,71 |
2532,201 |
HCOH |
55,01 |
1970,149 |
H2O |
1,41 |
50,644 |
СО 2 |
8,05 |
288,395 |
О2 |
28,82 |
996,337 |
СН4 |
0,44 |
15,653 |
H2 |
0,06 |
1,956 |
H2 |
1,29 |
46,128 |
|
|
|
H2O |
29,91 |
1071,151 |
|
|
|
проскок |
5,30 |
189,662 |
ИТОГО: |
100 |
3581,138 |
|
100 |
3581,138 |
Рассчитаем технологические показатели:
Конверсия - технологический показатель, отражающий степень использования (долю) исходного реагента на химические превращения, который может быть выражен:
![]()
где
![]() -
количество сырья вошедшего в реактор
-
количество сырья вошедшего в реактор
![]() -
количество непрореагировавшего сырья
в реакционной смеси
-
количество непрореагировавшего сырья
в реакционной смеси
![]()
![]()
Селективность – это отношение количества исходного реагента, расходуемого на целевую реакцию, к общему количеству исходного реагента, пошедшего на все реакции (целевые и побочные):
![]()
где
![]() -
количества исходного реагента,
расходуемого на целевую реакцию
-
количества исходного реагента,
расходуемого на целевую реакцию
![]() -
общему количеству исходного реагента,
пошедшего на все реакции (целевые и
побочные).
-
общему количеству исходного реагента,
пошедшего на все реакции (целевые и
побочные).
![]()
![]()
Выход целевого продукта (НСОН) - отношение реально полученного количества продукта к максимально возможному выходу.
![]()
где
![]() - выход продукта;
- выход продукта;
![]() -
зависит от типа химической реакции.
-
зависит от типа химической реакции.
![]() (для необратимых
химических реакций).
(для необратимых
химических реакций).
![]() или
или

где
![]() -
количества реально полученного продукта
-
количества реально полученного продукта
![]()
Расходные коэффициенты на получение 1 тонны продукта:
Различают теоретические и практические расходные коэффициенты.
Теоретические рассчитывают по уравнению реакции:
основные
CH3OH+0,5O2→HCOH+H2O +Q;
CH3OH→HCOH+H2-Q;
побочные
CH3OH+1,5O2=CO2+2H2O+Q;
CH3OH+H2=CH4+H2O+Q.
Тогда
![]()
![]()
где
![]() -
молекулярная масса метанола;
-
молекулярная масса метанола;
![]() -
молекулярная масса кислорода;
-
молекулярная масса кислорода;
![]() -
молекулярная масса формальдегида;
-
молекулярная масса формальдегида;
а,в,с – стехиометрические коэффициенты.
Практические расходные коэффициенты рассчитываются из данных материального баланса как отношение массы затраченного сырья (А или В) к массе полученного целевого продукта (С):
По метанолу расходный коэффициент:
![]()
где
![]() -
масса метанола 100%;
-
масса метанола 100%;
![]() -
масса воды в метаноле;
-
масса воды в метаноле;
![]() -
масса формальдегида.
-
масса формальдегида.
По кислороду расходный коэффициент:
![]()
