
БИЛЕТ 11
1. Фосфопротеины – это белки, в которых присутствует фосфатная группа, она связывает-
ся с пептидной цепью через остатки тирозина, серина, треонина (т.е. тех аминокислот, которые содержат ОН-группу).
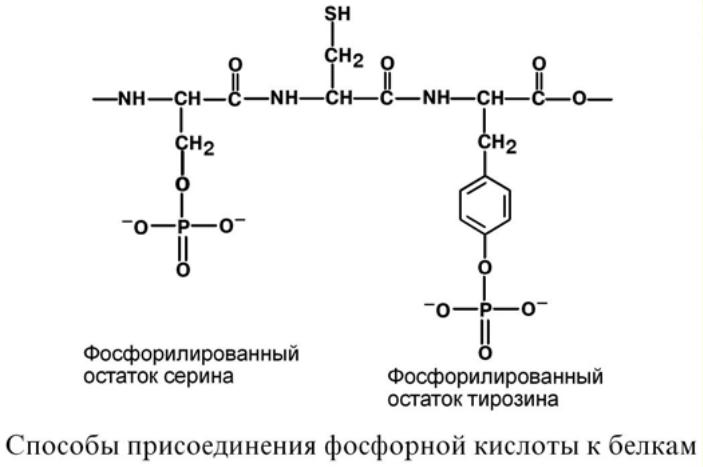
Фосфорная кислота может выполнять:
1. Структурную роль, придавая заряд, растворимость и изменяя свойства белка, например, в казеине молока, яичном альбумине.
2. Функциональную роль. В клетке присутствует много белков, которые связаны с фосфатом не постоянно, а в зависимости от активности метаболизма. Белок может многократно переходить в фосфорилированную или в дефосфорилированную форму, что играет регулирующую роль в его работе. Например, 1) ферменты гликогенсинтаза и гликогенфосфорилаза 2) гистоны в фосфорилированном состоянии менее прочно связываются с ДНК и активность генома возрастает.
Металлопротеины
Металлопротеины, кроме белка, содержат ионы одного или нескольких металлов. Ме-
таллопротеины часто являются ферментами. Ионы металлов соединены координационными связями с функциональными группами белка и выполняют следующие функции:
o участвуют в ориентации субстрата в активном центре фермента,
o входят в состав активного центра фермента и участвуют в катализе, например, служат
акцепторами электронов на определенной стадии ферментативной реакции.
К металлопротеинам, например, относятся белки, содержащие:
o медь – цитохромоксидаза, в комплексе с другими ферментами дыхательной цепи
митохондрий участвует в синтезе АТФ,
o железо – ферритин, депонирующий железо в клетке, трансферрин, переносящий
железо в крови,
o цинк – алкогольдегидрогеназа, обеспечивающая метаболизм этанола и других спир-
тов, лактатдегидрогеназа, участвующая в метаболизме молочной кислоты, карбоан-
гидраза, образующая уголюную кислоту из CO2 и H2O, щелочная фосфатаза, гидро-
лизующая фосфорные эфиры различных соединений.
o селен – тиреопероксидаза, участвующая в синтезе гормонов щитовидной железы,
антиоксидантный фермент глутатионпероксидаза,
o кальций – α-амилаза слюны и панкреатического сока, гидролизующая крахмал. Примерами металлоферментов являются селензависимая монодейодиназа, карбоангидраза.
2. Оксидоредуктазы, Трансферазы, Гидролазы, Лиазы, Изомеразы, Лигазы.
Шифр КФ (Классификация ферментов) или код фермента — это классификационный номер фермента по международной иерархической классификации.
IV К Л А С С . Л И А З Ы
Лиазы – ферменты, катализирующие разрыв С-О, С-С, C-N и других связей, а также
обратимые реакции отщепления различных групп негидролитическим путем. Выделяют 7
подклассов. Эти реакции сопровождаются образованием двойной связи или присоединением
групп к месту двойной связи. Лиазы являются сложными ферментами. Коферментами слу-
жат пиридоксальфосфат, тиаминдифосфат, участвует магний, кобальт.
Примером подклассов являются ферменты, действующие на углерод-углеродные связи,
углерод-кислородные связи, углерод-азотные связи.
Систематическое название образуется:
Расщепляемый субстрат : отделяемая группа – лиаза
Пример:
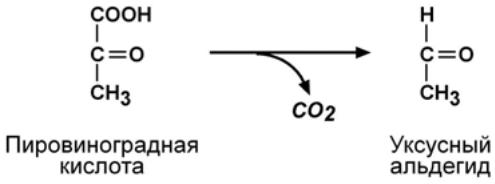
Характеристика фермента
Систематическое название 2-оксокислота:карбокси-лиаза
Рабочее название Пируватдекарбоксилаза
Класс 4. Лиазы
Подкласс 4.1. Углерод-углерод-лиазы
Подподкласс 4.1.1.Карбокси-лиазы
Классификационный номер КФ 4.1.1.1.
Кофермент Тиаминдифосфат
3. В И Т А М И Н В 2 ( Р И Б О Ф Л А В И Н , В И Т А М И Н Р О С Т А )
Источники
Достаточное количество содержат мясные продукты, печень, почки, молочные продук-
ты, дрожжи. Также витамин образуется кишечными бактериями.
Суточная потребность
2,0-2,5 мг.
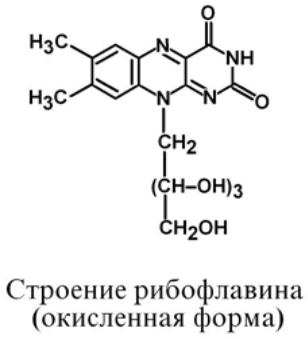
Строение
В состав рибофлавина входит флавин – изоаллоксази-
новое кольцо с заместителями (азотистое основание) и спирт
рибитол.
Коферментные формы витамина дополнительно содер-
жат либо только фосфорную кислоту – флавинмононуклео-
тид (ФМН), либо фосфорную кислоту, дополнительно свя-
занную с АМФ – флавинадениндинуклеотид
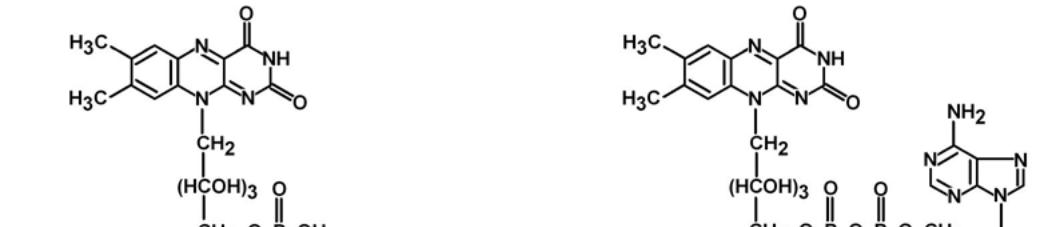

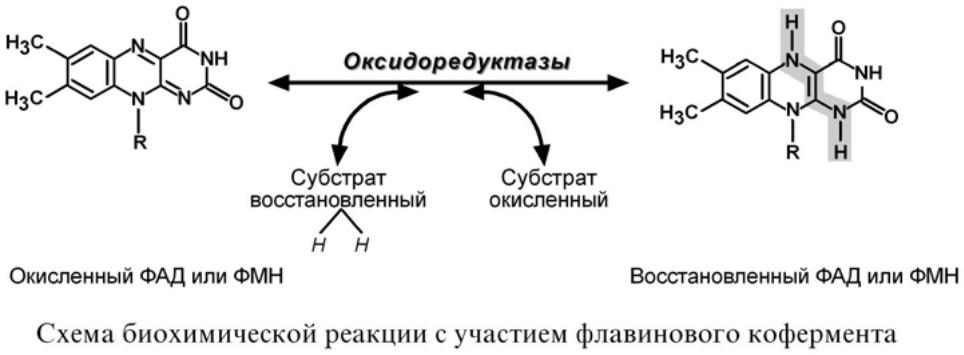
Биохимические функции
Кофермент оксидоредуктаз – обеспечивает перенос 2 атомов водорода в окислитель-
но-восстановительных
реакциях.
 Витамин
содержат:
Витамин
содержат:
1. Дегидрогеназы энергетического обмена – пируватдегидрогеназа, α-кетоглутаратде-
гидрогеназа, сукцинатдегидрогеназа, ацил-КоА-дегидрогеназа, митохондриальная
α-глицеролфосфатдегидрогеназа.
2.
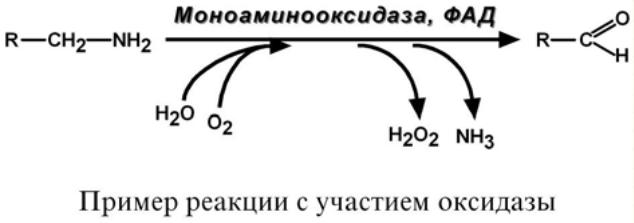
Оксидазы,
окисляющие субстраты с участием
молекулярного кислорода.
 Гиповитаминоз
Гиповитаминоз
Причина. Пищевая недостаточность, хранение пищевых продуктов на свету, фототе-
рапия, алкоголизм и нарушения ЖКТ.
Клиническая картина. В первую очередь страдают высокоаэробные ткани – эпителий
кожи и слизистых. Проявляется как сухость ротовой полости, губ и роговицы; хейлоз, т.е.
трещины в уголках рта и на губах ("заеды"), глоссит (фуксиновый язык), шелушение кожи в
районе носогубного треугольника, мошонки, ушей и шеи, конъюнктивит и блефарит.
Сухость конъюнктивы и ее воспаление ведут к компенсаторному увеличению кровото-
ка в этой зоне и улучшению снабжения ее кислородом, что проявляется как васкуляризация
роговицы.
Билет 12
