
- •Руды и минералы Au, Ag. Формы нахождения Au, Ag в рудах
- •Iтонкое измель флотация, обжиг
- •II. Плавка золотой головки
- •III. Гидрометаллургичесие методы
- •III. Влияние температуры
- •IV. Вязкость пульп
- •I. Метод перколяции
- •II. Метод кучного выщелачивания
- •III. Цианирование перемешиван
- •Au содовый раствор
- •Сжатый |оздах
- •1 Раствор
- •Сдира,н
- •Цианирование
- •Поведение примесей Au
- •III. Цианирование перемешиван
Рис.
36.Сдира,н
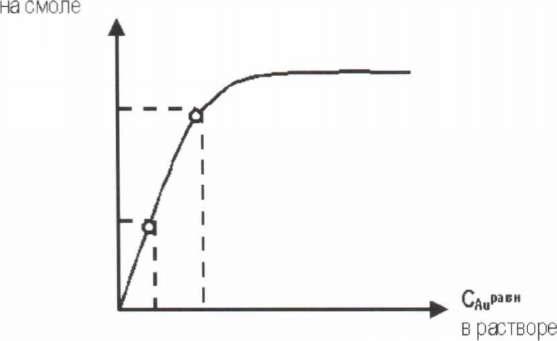
Чем больше вогнутость изотермы, тем селективнее смола. Из изотермы видно, что содержание Аи в смоле находится в зависимости от содержания Аи в растворе. Поэтому на практике для повышения ОЕ по Аи процесс ведут противотоком.
Предвари тельное цианирование руды, т.е. цианирования без смолы, когда в раствор переходит 70 + 80% Аи. Применяют для всех типов руд кроме углистых. Этот богатый раствор контактирует с выходящей из процесса смолой, обеспечивая высокую ее емкость. Рисунок 37
.
Рис.
37.
Обменная
емкость смолы по Аи сильно зависит от
наличия примесей. Рисунок 38.
Цианирование
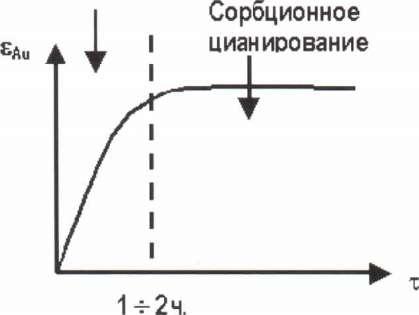

0Ед„

Рис. 3
8
На практике сорбционного цианирования ведут при минимальной возможной концентрации CN" и защитной щелочи :
CCN =0.01-0.02%;
ССаО=0.001 -0.01%.
>
[Au(CN)2]- > [Zn(CN)4r > [Ni(CN)4f > [Ag(CN)2] [Cu(CN)3]2"> [Fe(CN)6]4~>CNS~,CN
Кинетика и механизм сорбции
Исследованиями установлено, что процесс сорбции лимитируется либо пленочной, т.е. диффузией CN" - через пленку раствора прилегающей к зерну смолы , либо гелевой диффузией, т.е. диффузией CN" внутри зерна смолы
.
Поэтому для увеличения скорости процесса сорбции желательно применение макро пористых ионитов и меньших размеров зерен.
Практика сорбционного выщелачивания
Сорбционное
цианирование применяют для руды,
измельченной до состояния илов,
крупностью 0,150 мм или 0,074мм. Пески
недопустимы. Процесс ведут непрерывно
в серии 8 + 11 последовательно установленных
аппаратов. Рисунок 39.
Раствор NaCN Раствор СаО
Пачуки
сорбционного
Пульпа
Свежая или
регенерируемая
смол
а
Пачуки предварит, выщелачивания
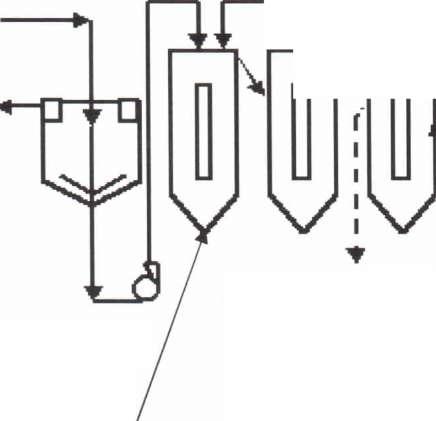
Слив
Сгущенный
продукт Ж : Т= 1 : 1
Насыщенная
смола
На
регенерацию
га
is
V
I
С)|ола
В оборот
Отвлеченная пульпа
I
На
обезвоживани
е
Рис. 39
Параметры сорбционного выщелачивания
1.Число аппаратов в каскаде сорбционного выщелачивания. Обычно оно составляет не менее 10+12. Число аппаратов устанавливают теоретически по изотерме сорбции (графически). Рисунок 40
.Г
Р
Аи
на
смоле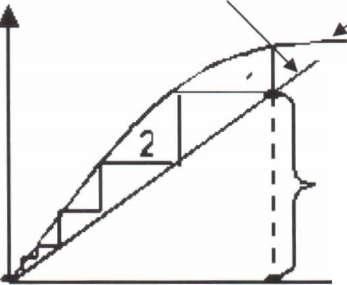
Рабочая
линия
70-90
% степень использования емкости смолы
кон
Рис.
40.
Изотерма
С
р
Аи
в
растворе
САи
САи
нач
С
=
Саируд =10 г/л Ж : Т= 1:1 £Au = 98%. 1 m - 1 mj 100 - 9,8г nT=4
п.
КПД
Nannap. зависит от КПД аппарата, т.е. от степени проскока.
Поэтому:
Для пачуков КПД « 30-35%. Значит:
^=- = 1,3
Для пульсационных колонн КПД = 90%. Значи
тДля аналитического метода используют формулу:
где т - коэффициент снижения концентрации Аи в растворе за счет
|^Аи-в-растворе j ^-jAu-в-растворе^
N = -
lg т
сорбции в одном аппарате (в одной ступени). Для пачуков т = 1.5-2. Для пульсационных колонн т=3-4. 2. Продолжительность сорбционного выщелачивания, т.е. время нахождения пульпы в аппаратах тг„=6-12-20 часов.
3. Поток пульпы (м3/час)-0
апп
Yv =От
/ j апп сл
4. Продолжительность сорбции- это время нахождения смолы в аппаратах от загрузки до насыщения ее и выгрузки тСорб.=Ю0 + 300 часов (до 400 ч.).
5. Поток смолы (литр смолы/час, или м7час)
В =
^ сорб
6. Величина единовременной загрузки смолы Р (л, м3) Р = 1.5-2% от XVpa6ann; Потери смолы, или расход свежей смолы составляет 10-20 г/т руды.Аппаратура сорбционного цианирования
Предварительное цианирование ведется в обычных пачуках.
Сорбционное цианирование ведется в пачуках сорбционного выщелачивания. Рисунок 41. Они отличаются от пачуков цианирования и наличием дренажных устройств и дополнительного аэролифта для транспортировки смолы и пульпы на дренажное устройство (аэролифт).
Рис.
41.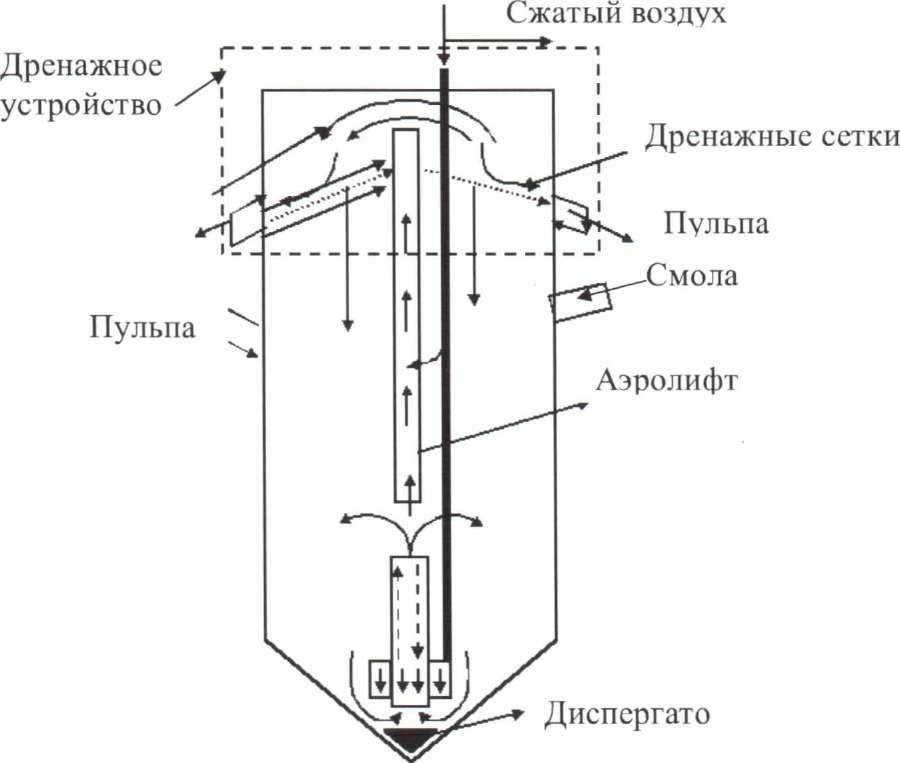
Недостаток: возможность проскока, поэтому на некоторых фабриках испытывают пульсационные колонны, к которым дополнительно устраивают аэролифт и дренажное устройство.
Смола 1-гЗ мм.
Руда 0.074 -г- 0.015 мм. Дренажные сетки: d = 0.4 мм.
S =1-5-15 м2. V = 500 м3.
Продукты сорбционного выщелачивания
Поступает: Руда:
CAu=5+ 10 г/т; Ж:Т=1:1 (2:1);
крупность -0,150 мм;-0,074 мм. Выходит:
Обеззолоченная пульпа: -твердая фаза 0.1+0.2 (0.3) г/т; -жидкая фаза 0.01 + 0.02мг/л (г/м3);
Насыщенная смола: -5 + 15 (20) мгАи/гСМ0Лы;
-60 + 80 (100) мгпримесей/г смолы"
Обеззолоченная пульпа поступает на контрольное грохочение для улавливания случайно проскочившей смолы, далее на обезвреживание и в отвал. Насыщенная смола поступает на регенерацию.
Регенерация смолы
Цель данной операции:
Выделить со смолы Аи в богатый раствор;
Удалить из смолы примеси, восстановив ее сорбционные свойства. Регенерированная смола:
САи< 0.1+0.3 мг/г; ХСприм.< 1+3 мг/г.
Десорбция смолы ведется методом элюирования, т.е. вымыванием ионов Аи и примесей со смолы различными растворами.
Для десорбции Аи используют раствор тиомочевины в H2SO4 (или
НС1).
Стъю= 60-80 г/л; CH2so4= 30 г/л; Thio= CS(NH2)2.
При этом протекают следующие реакции:
R[Au(CNJzJ + Thio + H2S04 = [Au(Thi0)i]2+S04 +t?//CW +R2S04;
Процесс ускоряется при Tt, поэтому ведут при t=50+60°C.
Данный метод не избирателен. Кроме Аи десорбируются Ag и Си. Поэтому Си должна быть удалена ранее.
Для удаления Си и Fe используют крепкие цианистые растворы: раствор: NaCN + NaOH.
50 г/л
R2[Cu(CN) 3] + 2NaCN + NaOH = Na2[Cu(CN)3J + 2RCN;
R4[Fe(CN)6] + 4 NaCN = Na4[Fe(CN)6] + 4RCN. Для десорбции Ni, Zn - смолу обрабатывают раствором H2SO4.
R\Zn(CN\\ + 2H2SOA = ZnSO, + R2S04 + 4HCN T fl2[M(CW)4J + 2H2S04 = NiS04 + R2SOA + 4 HCN T
Для более полного удаления из смолы Zn, Si02, АЬОз, а также CN, CNS", S03\ SO4-", S203z" смолу обрабатывают растворами щелочи. При этом смола переходит в ROH форму и используется снова в цикле сорбции.
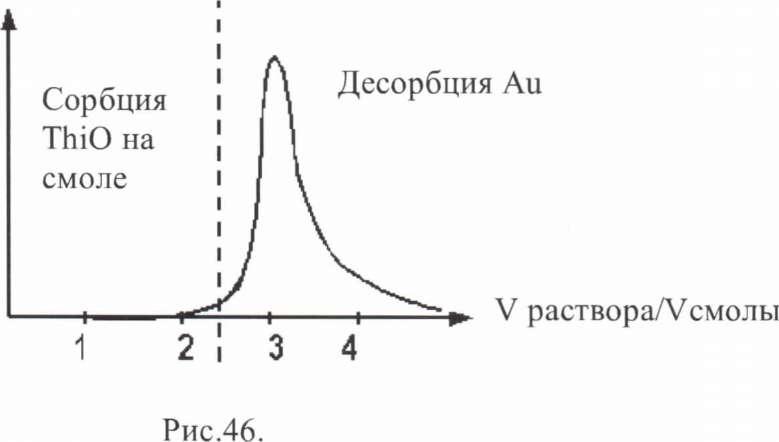
Схема регенерации смолы. Рисунок 45.
Отмывка от ионов, песков ведется на отсадочной машине, все остальные операции в регенерационных колоннах. Отходящие газы улавливаются для регенерации NaCN. Первые порции раствора не содержат золота,т.е. десорбция золота не идет. Лишь по истечении некоторого времени обработки появляется золото. Процесс десорбции описывается кривой элюирования. Рисунок 46.
На большинстве фабрик регенерация смолы ведется в регенерационных колоннах типа КДС ("колонна движущегося слоя"). Для промывки и десорбции ионов используется один тип колонн, различающийся только наличием подогревающего устройства к теплоизоляции. Для кислых сред колонна выполняется изТк
Для цианистых , щелочных, водных сред - из стали (ст. 3).
Д = 100- 1000 мм ;
Н = 1 - 6(10)м ;
Н : Д = 10(20): 1 ;
^раствора = 0.5 - 1 м/час (3-4 м/ч) - линейная скорость движения раствора
.
Длительность регенерации смолы около 200 часов, на десорбцию Аи расходуется 70+80 часов.
Аппаратура для регенерации. Рисунок 47.
Смола Смола
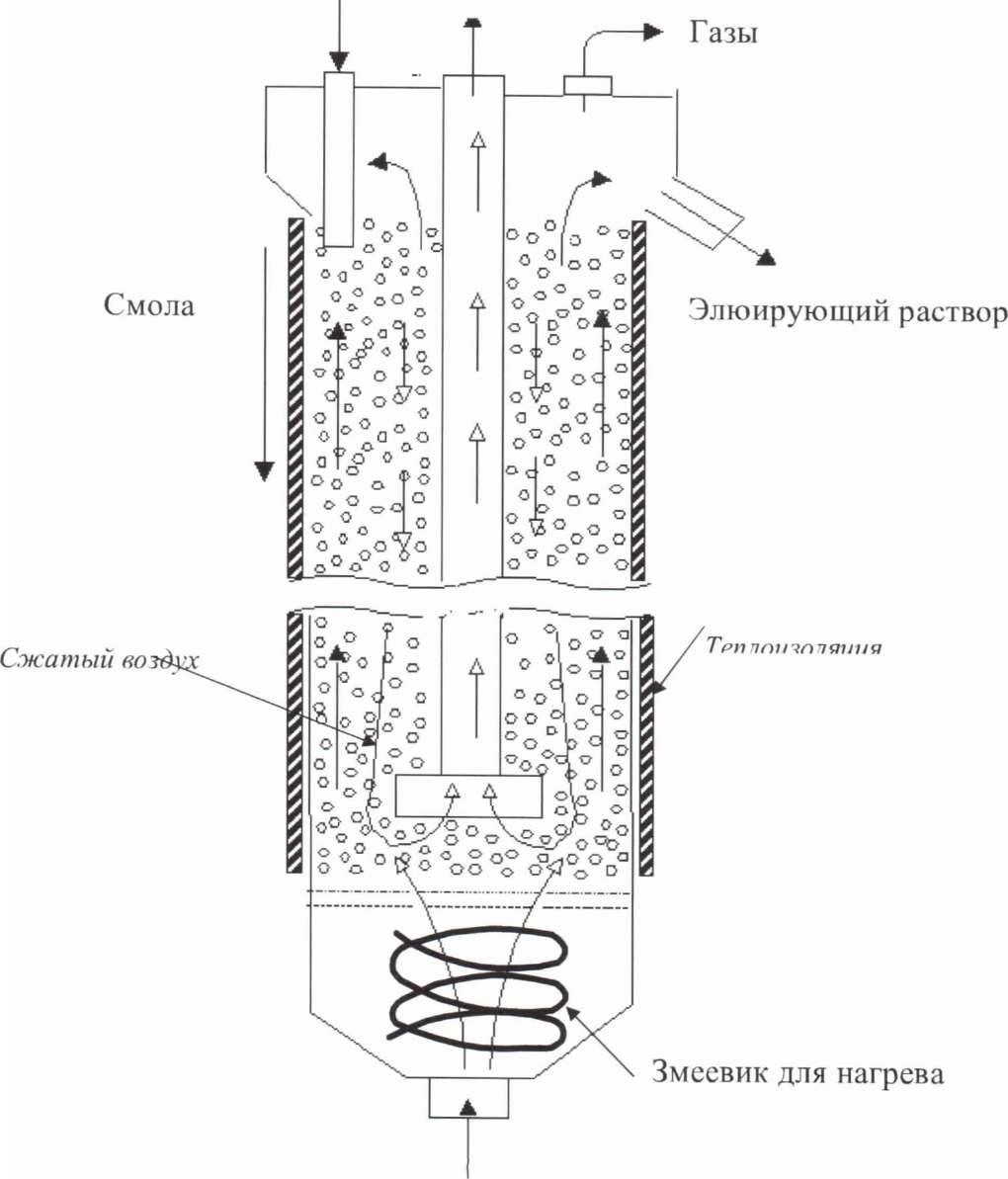
Элюирующий раствор Рис.47.Полунепрерывный режим
Периодически по спец. графику включается аэролифт. Время пребывания смолы в 1 колонне около 15 ч. На некоторых фабриках применяются другие типы колонн, типа пульсационных. Рисунок 48.
Раствор Смола
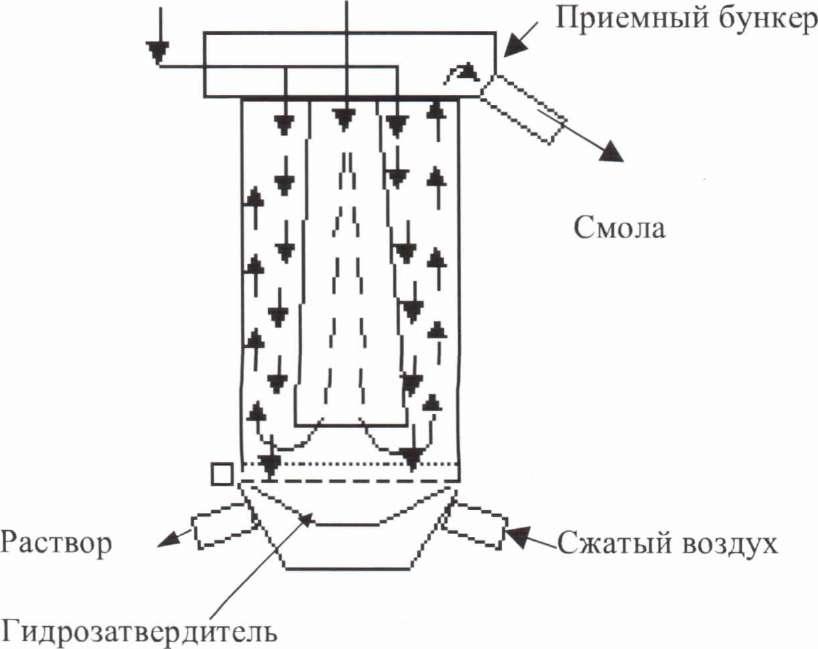
Схема цепи аппаратов. Рис.48.
Каждая операция ведется в специальной колонне. Например, для цианистой обработки устанавливается - 3 колонны; Для отмывки -2; Для кислотной обработки -3; Для сорбции Thio -2; Для десорбции Аи - 5 и т.д. На каждой операции движение смолы и раствора противоточное. Смола передвигается от первой колонны к последней с помощью промежуточных аэролифта, а растворы перекачиваются из колонны в колонну с помощью промежуточных аэролифтов вместо центробежных насосов.
Например, для десорбции Аи схема цепи аппаратов выглядит так. Рисунок 49
.Thio, H2SO4
Смопа
4
с
СХ-![]()
Раствор
Рис.
49.
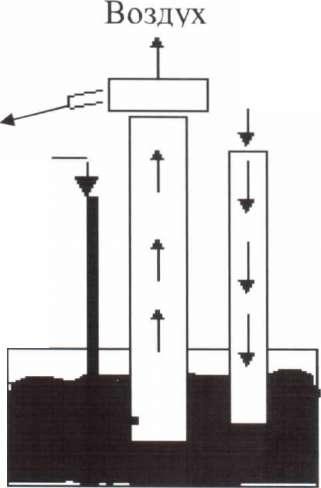
Раствор в
рсгенерационную
колонну
Сжатый воздух
Раствор
Рис.50. Промежуточный аэролиф.
Выделение золота из тиомочевинного элюата
Thio (элюат), или товарный регенерат содержит Аи в форме: [Au(Thio)2]2S04; CAu=0.5-2 г/л. В такой же форме Ag: [Ag(Thio)2]2S04.
В качестве примесей: [Cu(Thio)3]S04; [Zn(Thio)4]S04; [Fe(Thio)4]S04.;
Кроме того, свободную Thio, H2S04, Н20. Для выделения Аи могут быть использованы разные методы: 1. Цементация Zn, Pb, А1;
Сейчас не находит применение, т.к. низкое качество получаемых осадков.
2. Гидролитическое осаждение Аи. Характеризуется низким качеством осадка и невысоким извлечением Аи. 3. Электролитическое извлечение Аи из раствора. Проба Аи 980-990; ЕАи= 98% и более.
Электролитическое выделение Аи из тиомочевинного элюата
Электрохимическую
ячейку для выделения Аи можно представить:
K(Ti,C)
[Ag(Thio)2]4
A(Pt)
На аноде - окисление наиболее электроотрицательных элементов . На катоде - наиболее электроположительных. Рассмотрим электродные потенциалы наших элементов :
Ф Au/Au(Thio)2+ = +0,38 (В); ФJ Ag/Ag(Thio)2+ = +0,023 (В);
ф° cu/cu(Thio)43+ = -0,12 (В); ф° zn/zn(Thio)2-+ =-0,78 (В).
Отсюда видно, что на катоде протекают следующие процессы
:
[Au(Thio)2]+ + e ->Au + 2Thio; [Ag(Thio)2]+ + e->Ag + 2Thio.
2H + 2e —» H2 - степень развития реакции высока из-за высокой концентрации H2S04.
Поэтому г|к= 10-20%.
На аноде возможно протекание 2-х реакций:
2Н20 = 4Н+ + 02 + 4е;
Окисление Thio:
2CS(NH2)2- 2е CS2(NH2)2(NH)2 + 2Н+
формамидиндисульфид / \
s cnnh2
Цианамид
Этот процесс происходит при повышенной плотности тока и является вредным, так как:
Происходит потери Thio ;
Образуется элементарная сера, загрязняющая катодное Аи;
Возможно обратное растворение золота с катода.
Поэтому на практике принимают все меры для предотвращения на аноде окисления Thio. Это достигается разделением катодного и анодного пространства с помощью ионитовой мембраны.
Использование в качестве анолита просто раствора h2S04, в качестве католита- золото содержащий элюат (Au(Thio)2 ).
Могут использоваться либо катионитовые, либо анионитовые мембраны (пластины из ионообменных смол). Рисунок. 51.
Анионитовая
мембрана
1>ис.51.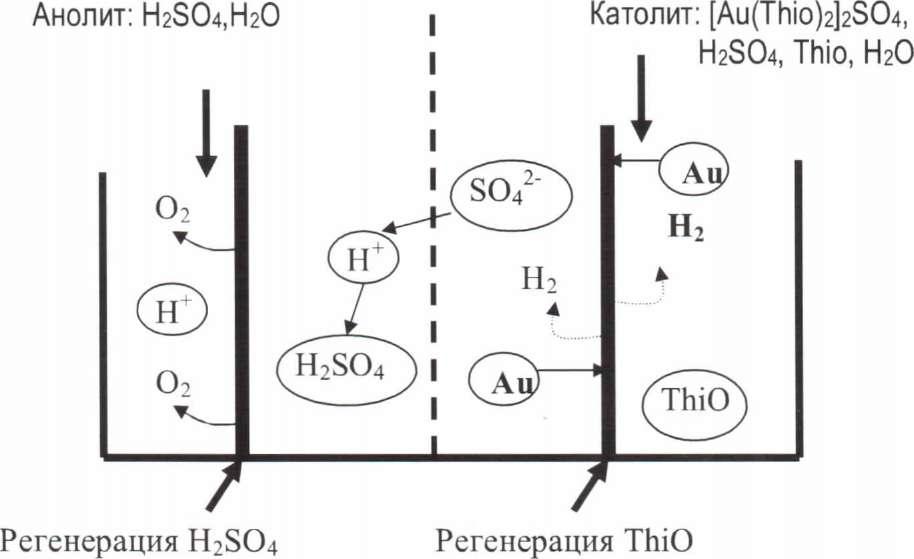
Исследованиями установлено, что выделение Аи лимитируется величиной предельного тока, т.е. процесс ограничивается диффузией [Au(Thio)2]+ к поверхности катода. Рисунок 52.
Катионитовая
мембрана Анолит:
НгЭОд.НгО | Католит: [Au(Thio)2]2S04,
Рис.
52.
Пути интенсификации :
Увеличение интенсивности перемешивания;
Повышение температуры ;
Увеличение катодной поверхности.
Перемешивание осуществляется: 1-Н2;
2. Принудительным движением элемента по катодной камере. Температура: Т до 40+50°С. Увеличение катодной поверхности достигается двумя путями:
Использование пластинчатых электродов, выполненных из Ti ;
Использование волокнистых углеграфитовых материалов (углеродистый ватин);
- толщина нитей 5 н-10мкм;
2 2
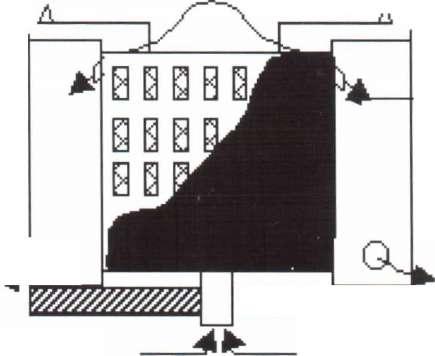
Вывод
католита -LP
Анолит
У//////////////М
Rhianr)
пнппнтл
Подача
анолита
Подача
католита
Токоподвод
/
Устройство электролизной ванны
Электролизер представляет собой Ti -ящик размерами: 935 х 1220 х 805 мм .Рисунок 53.
В электролизер помещено 10 катодных и 11 анодных камер. Размеры катодов: 254 х 374 х 2 мм. Бэф = 30 + 40 м2.
Рис.
53. Катионитовая мембрана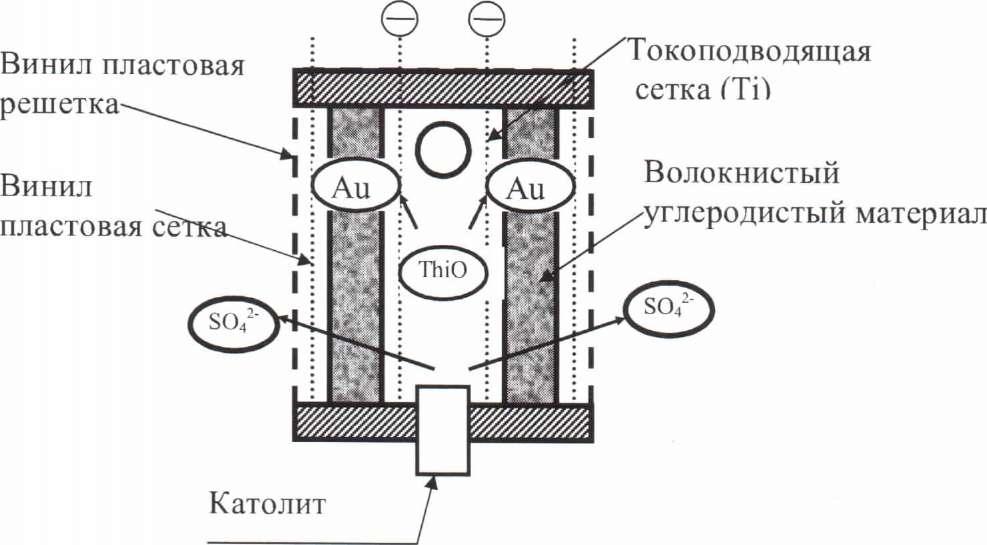
Ф)
Pt-
сетка
Рис.
54. Анионитовая мембрана
Раствор
H2SO4
Рис.55.
Анодная камера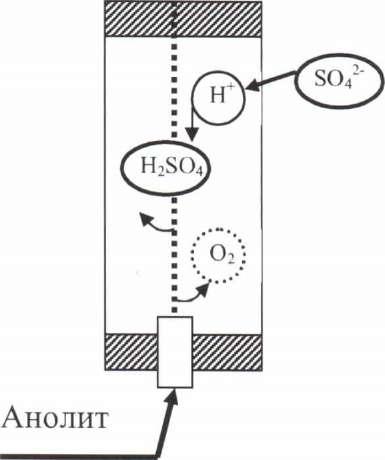
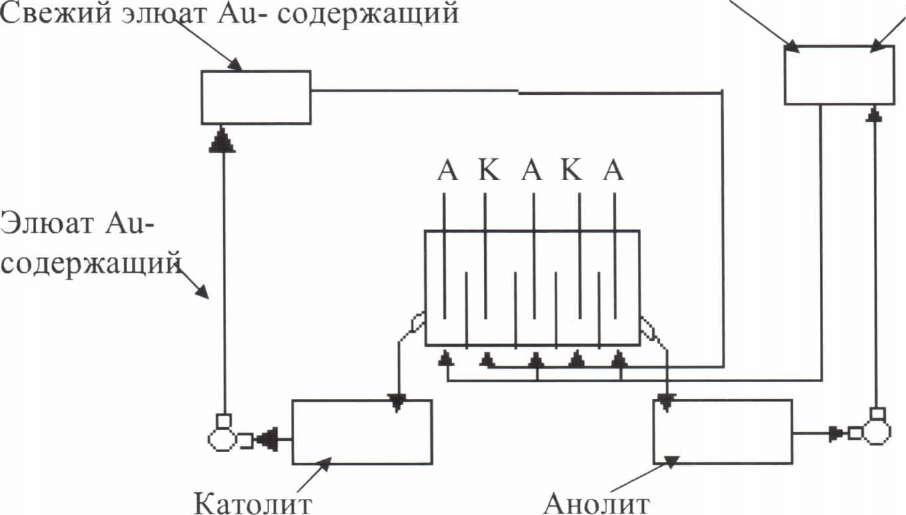
Катоды перед выпуском промывают в электролизере водой, пропускают снизу сжатый воздух (для просушивания) и затем только вынимают.
Разгрузка золото содержащих катодов осуществляется периодически по мере накопления золота на углеродистом ватине.
Катоды вынимают из ванны, ставят на Ti - поддон, открывают крышки, стряхивают углеграфитный ватин, ставят новый ватин и устанавливают в электролизную ванну. В полученном осадке содержится 2-4% углерода. 1 кг углерода может осадить 50 кг золота. Для удаления углерода полученный катодный осадок прокаливают при t = 60СН-850 °С в электрической печи. Получают катодное золота пробы 990-^998. Это конечная операция технологии сорбционного выщелачивания таких руд.
Технология сорбционного выщелачивания кроме исключения операции фильтрации, кроме повышения извлечения золота позволяет получать металл высокого качества.
Данная технология имеет и ряд недостатков:
Длительность процесса (большая величина незавершенного производства);
Сложность, громоздкость схемы;
Высокая стоимость смол.
Поэтому данную технологию применяют только для отдельных видов
руд
.
Сорбция на активированных углях
Сорбентом служит активированный уголь:
сферической формы 0.3 ч- 4 мм;
цилиндрической формы.
Активированный уголь получают из древесины, бурого угля, каменного угля из скорлупы орехов (кокосовых). У нас в стране до последнего времени не было налажено производства прочных активированных углей.
Их
получают термической обработкой без
доступа воздуха для удаления воды,
смол. Затем проводят активацию, которая
достигается обработкой сырца либо ССЬ
либо водяным паром FbO.
50%
С
выгорает: I-
Нг
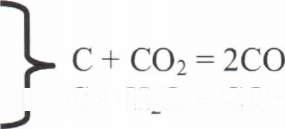
Образуются зерна угля с сильно развитой поверхностью. Может вестись термохимическая обработка солями:СаСОз,№2СОз, FeCh и др. Природа сорбции до сих пор не установлена.
Особенности углеродистых сорбентов
Углеродистый сорбент отличается:
Высокой избирательностью сорбции по отношению к золоту и серебру.
Практически не сорбирует цветные металлы (значит не нужна смежная схема регенерации);
Низкая емкость по отношению к золоту :
ОЕ = l-f-5 мг/г (шах 2 ч- 8 мг/г);
углей по Au
3. Низкая механическая прочность, следовательно высокие потери;
Расход углей 100 -ь 200 г/т руды;
Более низкая стоимость по сравнению со смолами.
Области применения активированных углей
1. Извлечение золота из растворов кучного выщелачивания. Растворы бедны по золоту, содержат много примесей. Уголь, как правило, сжигается, получается золотой осадок. Рисунок 56
.
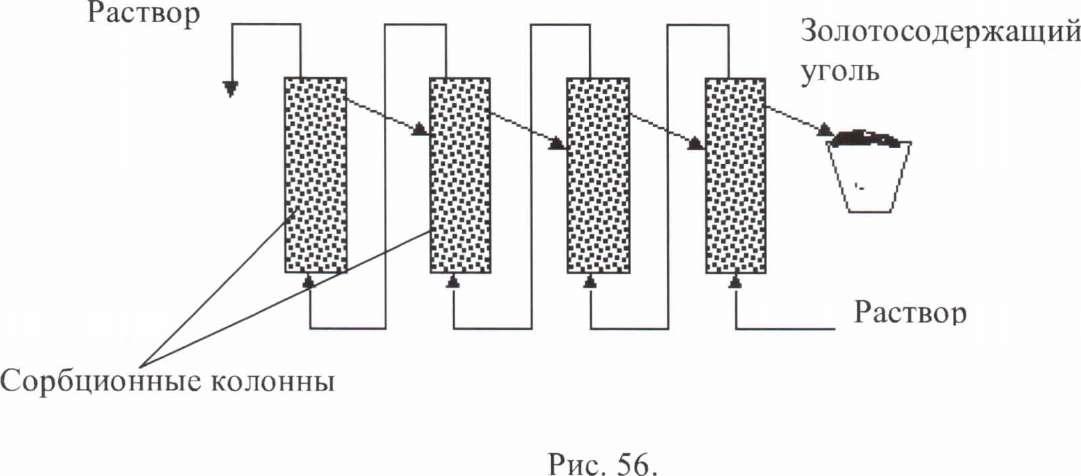
Извлечение золота и серебра из растворов по переработке Pb-Zn руд обогатительных фабрик;
Извлечение золота, серебра из растворов хвостахранилищ ЗИФ;
Использование активированных углей для извлечения золота и серебра из технологии сорбционного выщелачивания "уголь в пульпе".
Для шламистых руд используют с осторожностью из-за возможности забивания пор сорбента .
Технология анологична технологии сорбционного выщелачивания с использованием ионитов:
-предварительное выщелачивание;
-сорбционное выщелачивание (4-5 колонн);
регенерация.
Регенерация насыщенных углей ведется по схеме, включающей:
обработку раствором :
0,1-0,2% NaCN и 1-2% NaOH
t=20°C Т= 5 - 3 суток;
t=l30°С (в автоклаве) Т=10 -ь 12 ч.
[Au(CN)2]~ на выделение золота
рециркуляция угля.
СаСОз, смоляные вещества, масла, примеси удаляют раствором НС1 и прокалкой без доступа воздуха в трубчатой вращающейся печи. Получают регенерированный уголь. Из цианистого раствора золото выделяют электролизом. Применяют электролизеры цилиндрической формы с катодом из стальной ваты. Рисунок 57.

Полученный катодный осадок Fe-Au(Ag) подвергается переплавке с добавкой окислителя (селитра) и образованием шлака (сода и бура). Получают сплав золота пробы 900 и выше.
Недостаток технологии: высокие потери угля.
Обезвреживание сточных вод ЗИФ
Для переработки 1 т руды на фабриках расходуется: -0,2-1,5 кг/т NaCN; -0,5-1,3 кг/т каустической соды; -0,3-0,9 кг/т H2S04; -0,2-0,5 кг/т Thio;
-3,0-9,0 кг/т извести, ртути и другие реагенты.
Поэтому сточные воды фабрик содержат токсичные элементы, основным из которых является CN-, а также CNS^, Hg, As и
некоторые др. Поэтому продукты обработки, выбрасываемых в отвал (хвосты сорбционного выщелачивания, обеззолоченные растворы после цементации золота, кеки фильтрации пульп цианирования и др.) должны быть обезврежены до ПДК.
Содержание токсичных веществ в продуктах и ПДК на них могут колебаться в следующих пределах. В таблице 3 приведены содержания токсичных веществ в продуктах и ПДК на них
.
|
Таблица
3. Для
рыбно - хозяйственных нужд
ж |
С ж.ф , мг/л |
ПДК, мг/л |
|
CN" |
32-570 |
0,1-0,05 |
|
CNS- |
13-420 |
0,1-0 |
|
С1~ (акт.) |
100-500 |
0-0 |
|
As |
0,1-4,0 |
0,05-0,01 |
|
Pb |
0,5-200 |
0,1-0,1 |
|
Fe |
0,01-6,0 |
0,5-0,25 |
|
Си |
0,1-6,0 |
1,0-0,1 |
|
Thio |
|
0,03-0 |
|
Hg |
0,1-0,5 |
0,015-0,001 |
Цианид, может находится в следующих соединениях:
Простые, растворимые, токсичные соединения NaCN, KCN,
HCN
Комплексные растворимые, токсичные соединения: [Cu(CN)3]2-,[Zn(CN)4]2-
Растворимые нетоксичные соединения: [Fe(CN)6]4-H [Fe(CN)6]3~
Эти соединения в кислой среде, например под действием желудочного сока разлагается на: FeCl3, NaCN, HCN- токсичные соединения.
нерастворимые, нетоксичные простые цианиды Cu(CN)2 и Fe(CN)2
в кислой среде также разлагаются с образованием токсичных соединений.
5. комплексное нерастворимое соединение Fe4[Fe(CN)6]3- Ион [Fe(CN)6]4" под действием О2 в водной среде переходит в [Fe(CN)6]3" + ОН". Далее ион гидрализует :
[Fe(CN)6]3" + Н20 >Fe(OH)3 + HCN
Роданиды могут находиться в форме:
NaCNS;
Для
хозяйственных нужд
.
Методы обезвреживания
1. Нейтрализация цианистых растворов с отгонкой образующихся HCN и последующим улавливанием ее щелочным раствором.
Исходная пульпа (рН=10 ч- 11) подкисляется H2SO4 до рН=2,5 -s- 2,8. При этом под действием H2SO4:
NaCN + H2S04 = HCN t + Na2S04
происходит разложение простых и некоторых комплексных соединений:
[Zn(CN)4]2' + H2SO4 > HCNt +ZnS04
HCN удаляется в газовую фазу, улавливается NaOH , происходит регенерация NaCN (достоинство метода).
Недостатки: не регенерируется значительная часть комплексных соединений, поэтому очистки до ПДК не происходит.
Обработка цианистой пульпы сульфатом Fe(II) (солью Мора). Преследуется цель: связать простые, растворимые токсичные
соединения в нетоксичные растворимые или нерастворимые соединения: Fe(CN)6]3", [Fe(CN)6]4-, Fe(CN)2. Недостатки:
очистки до ПДК нет ;
не разрушаются CNS" ;
возможен переход нетоксичных соединений снова в токсичные.
Окислительные методы;
Суть их основана на обработке цианистой пульпы окислителями, которые окисляют все группы цианистых соединений и роданидов, разрушают при этом CNT , переводя его в безвредные СО32", NH/ или N2. Очистка этими методами ведется до ПДК. Действующим методом в этой группе является: а) Хлорный метод;
В качестве окислителя используют NaCIO, Са(СЮ)2, СаОС12 или С12. CN +Cio: = CNO" + СГ :
хлорат- ион цианат- ион
CNO +2Н20 = С032' + NH4+;
CNS~ +4CIO + 2 ОН = CNO + 4СГ + SO/' + H20;
[Cu(CN)3]2~ + 7 СЮ' + 20H~ + Н20 = 2Си(ОН)2 + 6CNO~ + 7СГ
.
Обезвреживание с помощью жидкого хлора ведется по следующей схеме: Рисунок 58.
Достоинства:
очистка до ПДК. Недостатки:
использование токсичного хлор-газа;
дорогой метод ;

Рис.57.
СаОС12
б) Метод озонирования Считается перспективным.
В качестве окислителя используется озон : 0з=02 + О Он образуется при воздействии электрического разряда на воздух (или кислород):
САГ + О = CNO' CNO' + Н20 = СО32~ + NH/ и т.д.
образующийся СГ , что приводит к "засаливанию" воды.
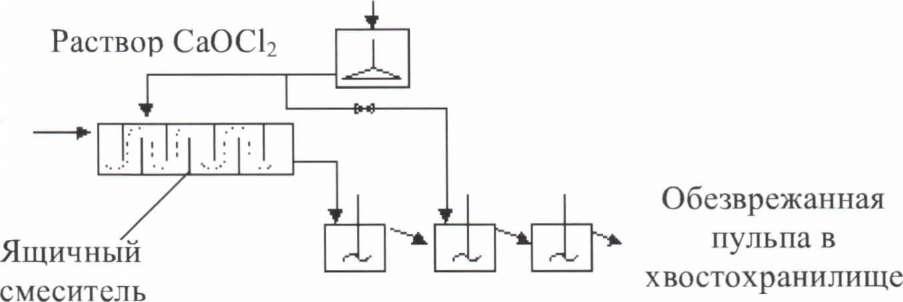
п = 2 -г 3; т = 15 + 20 мин
.
Очистка ведется до ПДК, но не нужны ни какие дополнительные реагенты и не образуется побочных продуктов.
Недостаток: высокая стоимость электроэнергии необходимой для получения озона.
в) Анодное окисление
Заключается в пропускании раствора через электролизер с нерастворимыми анодами и катодами. Метод применяют для пульп с высокой концентрацией CN".
На аноде:
CN~ + 20НГ = CNO+ 2Н20 +2е; [Cu(CN)s]2~ + 80Н~ = Си (ОН) 2 + 3CNO" + ЗН20~+7е; CNS~ + ЮОН~ = CNO~ + SOt + 5Н20 +8е 2CNO~ + 40Н~ = 2СО: + N2 + 2Н20 +6е
Недостатки: высокий расход электроэнергии.
Известны и другие методы (сорбции на анионитах, экстракция ), не вышедшие из стадии лабораторных исследований.
Очистка от As
Используют метод очистки, основанный на высокой сорбционной способности гидроксидов Fe(OH)3 по отношению ко многим соединениям As, Se,Te. Если на фабрике используют хлорный метод очистки, то в хвостах содержится некоторое количество СЮ~ в виде гиппохлорита. Для его нейтрализации вводят FeS04, который является эффективным сорбентомАз.
C10" + FeS04 > Fe2(S04)3 гидролиз Fe(OH)34,
Очистка идет до ПДК.
Очистка от Hg
Метод основан на малой растворимости в водных средах сульфида Hg (HgS44). Для образования этого соединения вводят сульфид Na: Na2S + HgCl2 = HgS + 2NaCl (Пр=10"50) Очистка идет до ПДК.
!!! Обезвреживание сточных вод является обязательным, но неокончательным решением вопросов охраны окружающей среды.
С целью обеспечения более экологически чистой обстановки на фабриках рекомендуют использовать оборотное водоснабжение.
Особенности переработки упорных руд
По технологическим свойствам руды делят на простые и упорные. К категории простых руд относят такие, которые удовлетворяют следующим требованиям:
Измельчение руды 80-90% класса - 0,074 мм.
Извлечения золота при цианировании более 90%.
Время цианирования менее 24 часов.
При последующей цементации золота из цианистых растворов извлечения золота 95-99%.
Расход NaCN при цианировании составляет 0,5 -§- 1,0 кг/т.
Пульпы легко сгущаются и хорошо фильтруются. Большинство руд относят к категории упорных.
В зависимости от признака упорности руды их разделяют в отдельные виды:
Кварцевые с тонковкрапленным золотом;
Кварцево-сульфидные (мышьяковистые или арсенопиритные) с тонковкрапленным золотом;
Медистые руды;
Углистые руды.
Глинистые руды;
Ферро-золотые;
Сурьмянистые;
Марганцовистые и т.д.
Кварцевые руды с тонковкрапленным золотом
Размер золота 0,005-0,001 мм. Упорность руды связанна с трудностью вскрытия золотин для доступа NaCN.
Методы вскрытия:
1. Проводят тонкое (четырех стадийное) измельчение руды до класса -0,040 мм и последующее цианирования руды по схеме сорбционного цманирования. Метод применим, если не содержится сверхтонкодисперсного золота.
Недостатки:
- Высокий расход электроэнергии на измельчение. 60-80% от общих затрат на переработку 1т руды. (Обычно - 30-40%).
- Большое количество образующихся шламов, что затрудняет операцию сгущения и фильтрации. Поэтому процесс проводят не в шаровых мельницах, а применяют рудное самоизмельчения.
2. Отправка кварцевой золото содержащей руды на медеплавильный или свинцово-цинковые заводы, для использования этой кварцевой руды в качестве флюса.
При медной плавке золото переходит в медный штейн, при конвертировании - в черновую медь, при огневом рафинировании - в красную медь, при электролитическом рафинировании - в электролитный шлам. Шламы перерабатывают до получения сплава Доре (сплав золота с серебром), который отправляют на аффинаж.
Недостатки:
недостаточно высокое извлечение золота (90- 93%);
высокие транспортные расходы.
Если кварцевый флюс отправляют на свинцово цинковый завод, то свинцовый концентрат агломерируют с кварцевой рудой и отправляют на шахтную плавку. Получают черновой свинец, содержащий золото, на стадии рафинирования золото и серебро переводят в серебристую пену.
(Au - Ag)Zn и перерабатывают с получением сплава Доре. Недостатки
те же.
Кварцево - сульфидные руды с тонковкрапленным золотом
В таких рудах сульфиды чаще всего содержатся в виде пирита FeS2 или арсенопирита FeAsS. В таких рудах может быть крупное золото, которое
удаляют гравитацией.
При переработке таких руд в технологическую схему включают операцию флотации для разделения сульфидов и оксидов.
Особенности флотационного режима
При флотации во флотоконцентрат извлекается золото свободное и золото ассоциированное с сульфидами. В качестве собирателя используют ксантогенаты - бутиловый, амиловый или пропиловый.
Расход их 80-150 г/т руды. В качестве вспенивателя - Т-80 или сосновое масло, расход которых 80+150 г/т.
Для
лучшей флотации золота рН должно быть
« 7,5. Для регулирования среды используют
Са(ОН)2,
NaOH,
№2СОз.
Рисунок 59.£au
a
![]()
В
пульпе CuS04,
NaCN и
6,0
7,5
9,0
Рис.59
Сульфат меди - активатор окисленных соединений, содержащих золото.
Для подавления флотации пустой породы вводят жидкое стекло.
Схемы флотации разнообразны, отличаются числом стадий флотации, числом перечистных и контрольных флотаций.
Особенность схем: число перечистных флотаций должно быть минимальным, контрольных - два или три для более полного извлечения золота из хвостов. Рисунок 60
.Примерная схема флотации
Хвосты
I
Контрольная ^флотация.
Руда
I
Измельчение
-0,300мм Стадия флотации в
об
^
_1
Флотоганцентрат
Хвосты- Доизмельчение -0,150 мм II
Стадия флотации
Хвосты
i
На
контрольную концентрацию
Промпродукт
в оборот
Хвосты
т
в отвал
Рис. 60.
Получают флотоконцентрат с содержанием :
Аисвоб и AuMeS -20 н- 120 г/т ;
FeS2, FeAsS и другие сульфиды до 20 %.
Методы переработки флотоконцентратов
Непосредственное цианирование руды в специальном режиме.
Вскрытие золота термохимическими методами:
Окислительный обжиг;
Окислительно-хлорирующий обжиг и последующее цианирование огарков.
Гидрометаллургические методы вскрытия золота из сульфидов:
Автоклавное выщелачивание в кислых или щелочных средах;
Биохимическое (бактериальное выщелачивание сульфидов) и последующее цианирование остатков;
4. Хлоридовозгонка. Рассмотрим эти методы
:
Применяется только для флотоконцентрата с невысоким содержанием пирита и арсенопирита. Флотоконцентрат доизмельчают до крупности -0,074 мм и цианируют в специальном режиме. Для исключения вредного влияния As, FeS, FeS2 в раствор вводят соли свинца и поддерживают пониженное значение рН .
Наиболее распространенный метод переработки данных руд.
2.1. Окислительный обжиг
Цель окислительного обжига :
Перевести плотные золото- содержащие сульфиды в пористые соединения (гематит Ре20з).
- Удалить из флотоконцентрата мышьяк, который мешает при цианировании, в газовую фазу в виде As203 .
Обжиг проводят при t=500-700°C т.к. окисление FeS2, FeAsS начинается при t=450 °С. При более высокой температуре (выше 700 НС) происходит частичное оплавление материала, за счет образования легкоплавких эвтектик.
Протекают следующие реакции:
FeS 2 + О 2= FeS + S02; FeS + 02 = Fe304+ S02;
Fe304 + 02= Fe2Os;
FeAsS + О2= FeS + As203 T ;
FeS + О 2= Fe304+ S02; Fe304+02= Fe203
Если есть избыток кислорода,то: As203 + 02= As^snI - вредно!
Практика процесса
При обжиге необходимо отогнать мышьяк в газовую фазу в виде А820з, серу - в виде S02. Для этого нужны разные условия.
Процесс обжига проводят либо в две стадии (в двух печах "КС" с разным расходом воздуха), либо в одну стадию, но противотоком (в одноподовых печах или трубчатых вращающихся печах).
а) Печи "КС" применяют при высокой производительности, но! для них характерен очень большой пелевынос, поэтому необходима установка громоздкой системы пелеулавливания. Потери золота достигают 2-3%.
б) Применяют одноподовые печи типа Эдвардса.
Они представляют собой камеру с площадью пода - от 10 до 20м2.
Сверху печь покрыта железным кожухом. Рисунок 61.
Печь установлена под углом 2 + 12 .Воздух
t
л
Флотоконцентрат
FnrtPT!
Огарок![]()
KJ KJ KJ KJ
Л-Ж.А-Л--Л...А-
S
= 12-16%
, As
до
16%
Au
30-
ЗООг/м
|
1 |
|
|
У |
г |
j |
|
|
X |
ж |
д |
ж |
|
Флотоконцентрат
Огарок
Рис.61
Хотя печь имеет меньшую производительность, но при этом резко снижается пылеунос, а значит меньше потери золота.
S в концентрате должно быть 16- 20 %. Если S < , то подается
топливо.
В результате окислительного обжига получают огарок, содержащий: S =1-2% ;
As=l-2% ; Au= 50-500 г/т.
Этот огарок после доизмельчения направляется на цианирование.
Анализ метода
Достоинства:
- Достаточно полное удаления серы и мышьяка. -Получение пористого огарка (РегОз)
;
Извлечения золота при цианировании 90-93%.
Недостатки:
Происходит частичное оплавления материала и его спекание, что может привести к резкому снижению извлечения Аи;
Получение при обжиге пылей (возгонов), содержащих токсичные
As203;
Значительные потери золота с пылями.
2.2 Окислительно - хлорирующий обжиг;
Цель обжига: та же самая.
Суть метода: Флотоконцентрат с содржанием серы 5 % смешивают с NaCl (в количестве 20% от массы флотоконцентрата) и подвергают Окислительному обжигу при t= 500-700°С.
Если серы больше 5% то сначала проводят просто окислительный обжиг (без NaCl). При этом сера переходит в S02, As - в As203.
Далее проводят окислительно-хлорирующий обжиг.
При этом:
FeS 2 = FeS + S2;
FeS2 + О 2 = FeS + S02;
NaCl + S + О 2 = Na2S04+ Cl2;
NaCl + SO 2 + О 2 = Na2S04+ Cl2:
FeS + Cl2 + 02= FeCU (FeCl2) + S02;
FeCl2+ О 2= Fe203+ Cl2;
FeCU + 02= Fe203+ Cl2;
Таким образом, образуется очень пористый материал - гематит, что улучшает доступ NaCN при цианировании золота и повышает его извлечение.
3. Гидрометаллургические методы предусматривают разложения сульфидов, содержащих золото и вскрытие золотин, заключенных в них.
Автоклавное выщелачивание сульфидных
золотосодержащих концентратов в кислых и щелочных
средах
Процесс ведется при t= 120-180°С, т.е. в автоклавах, при давлении кислорода Р02=0,5-1,0 мПа в течении 2-4 часов. При выщелачивании в кислой среде происходит окисление FeS:
(A) FeS + О2 +Н2О = FeSOs+FUSQj;
(Б) FeAsS + О2+ Н20 = FeSOj + H3As04;
FeS О 4 +02 + H2SO 4 = Fe?(SOd)i + Н20;
FeS + Fe2(S04)3 + H20 = FeS04 + H2S04; FeAsS + Fe2(S04)3 + H20 = FeSQ4 + H2S04 + H3As04.
Железо переходит в раствор.
H3ASO4 с соединением железа образует FeAs04 - арсенат железа переходит в нерастворимый осадок (н.о.).
Fe2(S04)3 +H?0=Fe1Q1nH1Q +H2S04
н.о.
Золото переходит в н.о.
Нерастворимый остаток (пустая порода + FeAsC>4 + Fe203-nH20 + Au, Ag) отделяют , промывают от серной кислоты и направляют на цианирование.
При цианировании извлечение золота достигает 95-97%.
При выщелачивании в щелочной среде железо в раствор не переходит, а в окисленной форме остается в н.о. Мышьяк переходит в раствор, сера переходит в раствор:
2FeS2 + HNaOI! +7,502 = FezOj + Na2S04 + 4Н20;
н.о.
2 FeAsS +10 NaOff +702 = Fe203+2NgjAs04 + 2Na2S04 + 5H20;
h..o.
Fe203-H.o.
Au —н.о.
пустая порода - н.о.
NaiS04 и Na3AsC>4- раствор, то есть обеспечивается еще более полное вскрытие золота.
При цианировании н.о. извлечение золота составляет 97-99%.
Но! этот метод более дорогой, чем кислотный.
4. Хлоридовозгонка
- это самостоятельный метод переработки руд данного типа.
Суть метода: сульфидный флотоконцентрат с содержанием серы менее 5%, смешивают с NaCl (10-15% от массы флотоконцентрата) и подвергают обработке в окислительной атмосфере при t = 900-1100 °С.
Процесс осуществляется в шахтной печи или в трубчатой печи. Процесс ведут без расплавления материала.
Реакции, протекающие в процессе, аналогичны записанным выше.
Образуются хлориды металлов:
FeCl3, FeCl2; CuCl, CuCl2; ZnCl2; AuCljAgCl.
Хлориды цветных и благородных металлов летучи.
Степень возгонки:
AuCl-99%; AgCl-98%;
ZnCl2-90%; CuC12-96%.
Возгоны улавливаются водой.
CuCl2, CuCl, ZnCl2 - переходят в раствор.
Золото и серебро образуют нерастворимый осадок:
AuCl + Н20 = Аи н.о.
AgCl + Н20 = н.о.
Остается нерастворимый остаток в котором содержится 80% золота и серебра.
Широкого применения метод не находит, что обусловлено сложным аппаратурным оформлением процесса и частичным оплавлением огарка.
Бактериальное выщелачивание
Этот один из наиболее перспективных методов переработки кварцево- сульфидных руд с тонковкрапленным золотом. В основе метода лежит окисления сульфидов кислородом воздуха в растворе. В роли катализаторов выступают бактерии особого типа - тионовые бактерии, которые способны окислять сульфиды металлов и переводить их в MeS04, S02, S042-.
Бактерии выращивают в специальных прудах. Условия их выращивания такие:
1=28-35 °С; рН=1,7-2,4.
Далее их добавляют в водную пульпу, содержащую руду. В течении 90 н- 120 часов проводят выщелачивание( t=28-35 °С; рН=1,7-2,4) . При этом протекают процессы как при автоклавном выщелачивании в кислой среде.
Последующее цианирование обеспечивает извлечение золота 95-97%.
Переработка пирротиновых руд
К этой категории относятся руды, содержащие более 1-5% FeS . Упорность этой руды связана с активной растворимостью пирротина в цианистых средах и это вызывает большой расход NaCN (более 6-12 кг/т) и низкое извлечение золота (до 50-60%). Поэтому при переработке таких руд применяют специальную подготовку. Данную руду можно перерабатывать по схеме 1, но с некоторыми изменениями (подготовка):
1.Для некоторых типов руд является достаточной термическая прокалка при
t = 300 °С. При этом происходит пассивация поверхности пирротина. При последующем цианировании пирротин (FeS) не растворяется.
Если пирротина много, то применяют окислительный обжиг (либо всей руды, либо флотоконцентрата) FeS=Fe203 + S02;
Если пирротин не содержит в себе золото, то его можно удалить методом
магнитной сепарации после измельчения руды. Затем цианирование по схеме 1.
Если содержание пирротина не велико то его можно перерабатывать по схеме 1, но цианирование вести в специальном режиме:
введение солей свинца, чтобы связать серу;
держать пониженную концентрацию щелочи (СаО);
интенсивная аэрация пульпы, при этом пирротин переходит в Fe203.
Переработка феррозолотых руд
Это руды верхнего слоя месторождения, образованные за счет выветривания сульфидных руд. Они содержат плотные оксиды железа (FeOOH, FeO, Рез04, FeAs04 и др.). С ними ассоциировано "ржавое" золото и тонковкрапленное. Упорность руды связана с трудностью вскрытия золотин.
Методы переработки
Если золото тонковкрапленное или находится в "рубашке" ("ржавое"), то переработка ведется по схеме 1, но с дополнительным доизмельчением руды в цианистой среде;
Возможна термическая прокалка руды при t =300-400 °С (происходит разложение и дополнительное окисление);
Если золото связано в основном с FeAs04, то можно его вскрыть выщелачиванием руды 5-10% раствором NaOH.
Медистые руды
На ряду с золотом присутствуют минералы меди: CuFeS2, Cu3FeS4, Cu2S, CuS, CuC03, Cu(OH)2, СиСОэ*2Си(ОН), CuSi03, СиО.
Вредным является содержание меди более 0,1%.
Упорность руды связана с тем, что все соединения меди переходят в цианистый раствор, резко увеличивая расход NaCN и 02. Кроме того, образуются поверхностные пленки на золотинах. Все это приводит к резкому понижению извлечения золота.
Методы переработки
Зависят от содержания меди, вещественного состава руды, форм нахождения меди (сульфидные или окисленные):
I. Если руда содержит много меди (более 0,1%), необходимо извлечь
не только золото но и медь.
В схемы переработки таких руд включается операция флотации (схема №3).
Вся медь в виде сульфидов;
Если медь в виде сульфидов и оксидов, то применяют флотацию в специальном режиме. Для улучшения флотации окисленных форм применяют активаторы или применяют метод Мостовича, который заключается в следующем:
Выщелачивание руды в растворе H2SO4 (окисленная форма меди переходит в раствор);
Не проводя фильтрации добавляют губчатое железо, оно цементирует
медь;
При последующей флотации CuS, Си, Аи переходит во флотоконцентрат.
Флотоконцентрат и хвосты перерабатываются аналогично пункту 1.
Если медь находится в виде сульфидов и оксидов, то применяют
выщелачивание соединений меди в растворе аммиака или серной
кислоты. Оставшийся, нерастворимый остаток цианируют.
II. Если меди менее 0,1%
Необходимо уменьшить вредное воздействие меди, чтобы полнее извлечь золото.
1. Цианирование в специальном режиме (при низкой концентрации NaCN, менее либо равное 0,01%). Золото растворяется, а медь - нет.
Ферритизирующий обжиг преследует цель обжечь руду с переводом меди в ферриты, практически нерастворимые в NaCN (Cu0*Fe203).
Снижение вредного воздействия меди достигается путем регенерации NaCN обработкой обеззолоченных цианистых растворов серной кислотой в присутствии хлорида железа (III):
Na2[Cu(CN)3] + H2S04 + FeCl3 = HCNtt + CuS04 + FeCl2 + Na2S()4
на улавливание
Переработка сурьмянистых руд
В них присутствуют окисленные и сульфидные соединения Sb.
Упорность руды связана с вредным влиянием сурьмы при цианировании.
В щелочных цианистых растворах на поверхности Аи они образуют пленки, что приводит к резкому снижению извлечения Аи.
Методы переработки зависят от содержания Sb, соотношения сульфидной и окисленной форм, формы нахождения Аи в руде и распределением его между минералами.
1. При невысоком (Csb <0,5%) содержании в руде и отсутствии тонковкрапленного золота данную руду можно перерабатывать по схеме №1, но цианирование вести в специальном режиме с добавкой солей Sb и поддержанием пониженного значения рН;
Если сурьмы много (0,5% н- 20%), то в схему включают операцию флотации (схема №3) Флотоконцентрат (Sb2S3, MeS, Au в MeS) отправляют на медепла- вильный или сурьмянистый заводы для извлечения золота.
Хвосты (в зависимости от содержания золота) либо в отвал, либо на цианирование в специальном режиме.
Если сурьмы более 5-20%, ее стоимость соизмерима с ценной золота. Нужно извлечь и сурьму, и золото.
Выщелачивание руды горячими щелочными растворами Na2S:
Sb2S3 + Na2S = Na3SbS3
Sb2S3 + Na2S = Na3SbS3 + Na3Sb03
Золото переходит в нерастворимый остаток. Из этих растворов сурьму извлекают электролизом, золото из н.о., цианированием в специальном режиме.
Sb2S3 + Na2S = Na3SbS3;
Sb2S3 + Na2S = Na3SbS3 + Na3Sb03.
Применяют сложную схему флотации, которая позволяет сначала получить сурьмянистый концентрат, а потом золотосуль -фидный концентрат и хвосты.
Сурьмянистый концентрат отправляют на сурьмянистый завод.
Золотосульфидный концентрат:
-Если есть мышьяк - производят обжиг и цианирование огарка.
- Если мышьяка нет - отправляют на медеплавильный либо сурьмянистый заводы для извлечения золота.
Углистые руды
Это руды, которые содержат углистые сланцы (1-10%), которые в свою очередь обладают высокой сорбционной способностью к цианистому комплексу золота. Это приводит к резкому уменьшению извлечения золота и увеличению концентрации золота в отвальных хвостах. Рисунок 62.
Сорбция
Аи
Рис.
62
Методы переработки
Методы переработки зависят от вещественного состава руды (есть сульфиды или нет); от формы нахождения золота и распределения его между породообразующими соединениями; от сорбционной активности углистых сланцев.
При не высоком содержании углистых сланцев и невысокой их активности можно непосредственно цианировать руду в специальном режиме: цианирование в несколько стадий; с малой длительностью цианирования 2-3 часа; обновление раствора на каждой стадии.
Проводят пассивацию углистых сланцев, если они не содержат золота, введением при сгущении (перед цианированием) керосина или масел. При этом происходит пассивация углистых частиц и Аи не сорбируется.
золото в сульфидах) отправляют на медеплавильный завод ( !!! нужны новые методы переработки на месте).
Хвосты - либо в отвал, либо на цианирование.
Шламистые (глинистые) руды
Это руды которые содержат более 3% тонких шламистых частиц
(крупностью менее 0,043%). Илы состоят в основном из Fe203, А1203.
Переработка таких руд методом обычного цианирования по схеме 1 связана с затруднениями на операциях сгущения и фильтрации пульп.
Глинистые руды при переработке склонны к структурированию, то есть образованию пульп с ячеистой структурой, что приводит к низкому извлечению золота, за счет ухудшения отмывки при фильтрации.
Лучшим методом переработки глинистых руд является технология сорбционного выщелачивания (схема 2). Если шламы не содержат золота, то для исключения их вредного воздействия наиболее просто выделить шламы из руды гидроциклонированием (после измельчения) и направить их в отвал.
Остающуюся руду перерабатывают как по схеме 1, так и по схеме 2.
Аффинаж золота и серебра
Разделение Аи и Ag и получение их в чистом виде осуществляют приемами аффинажа.
Известно несколько методов аффинажа Аи и Ag.
Наиболее распространены:
Хлорный процесс;
Электролитическое рафинирование.
Сырье, поступающее на аффинажные заводы различают по составу.
Аи поступает в виде:
сплавов, получаемых в результате плавки Au- Zn осадков;
черного золота после отпарки альмагамы;
шлихового золота(после обогащения россыпей и руд);
катодного чернового из тиомочевинных регенератов.
Кроме Аи и Ag материалы содержат примеси: Си, Pb, Hg, As, Sb, Sn,
Bi и др.
Содержание примесей достигает более 200 проб.
Ag поступает в виде серебряно-золотых сплавов(сплавов Доре), получаемых при рафинировании чернового РЬ и переработки медеэлектролитных шламов.
Сплав содержит 97-98% Аи и Ag.
Кроме названных видов сырья поступают различные сплавы; бытовой и технический лом; монеты и прочие.
Поступающие на аффинажный завод сплавы подвергают приемной плавке для усреднения и опробования отдельных видов сырья. Плавку ведут в графитовых тиглях в индукционных печах. Вместимость тиглей до 280 кг Аи.
Для предотвращения улетучивания БМ плавку ведут под слоем шлака (1.5 -н 3% от массы металла). Добавляют флюсы (сода и бура).
tnpw плавке Au —' 1 1 50 — 1 200 С ,
tAg= 1040 - Ю60°С. Высокопробное Ag может разбрызгиваться (при застывании вследствие выделения поглощенного 02). Поэтому плавку ведут под слоем древесного угля (создается восстановленная атмосфера).
Хлорный процесс
Хлорный процесс основан на различном сродстве металлов к хлору. Неблагородные Me и Ag окисляются хлором быстрее, чем золото.
Сущность процесса: СЬ продувается через расплавленное Аи (черновое). Хлор взаимодействует сначала с ЦМ и Ag, затем с металлами платиновой группы. Хлориды металлов не растворяются в Аи и всплывают на поверхность. Некоторые хлориды неблагородных металлов улетучиваются.
Порядок образования хлоридов следующий:
—► Zn —+Fe2+—*-Pb —► Си —► Fe3+ -> Ag.
Хлорный процесс применяют в ЮАР.
На аффинаж поступает металл, который содержит: 88- 90% Аи, 7- 11 %Ag.
Основные примеси: Си, Pb, Fe, Zn.
Процесс ведут в графитовых тиглях(тАи = 500кг).
Черновой металл после приемной плавки, в виде слитков, загружают в тигли. Для образования шлака загружают флюсы(смесь буры, кварца и хлорида натрия). Тонкий слой шлака на поверхности снижает улетучивание Me и предохраняет стенки тигля от разъедания.
После расплавления металла в расплав вводят одну или две фарфоровые трубки и подают газообразных хлор (t =1150°С).
Низкокипящие хлориды Fe и Zn - в газовую фазу (г.ф.).
РЬ - частично в г.ф. , частично в шлак. Улетучивание хлоридов приводит к бурлению, поэтому С12 в этот момент подают медленно. Аи и Ag начинают взаимодейст- вовать с С12 после того, как прореагируют Fe, Zn,Pb.
AgCl и CuCl остаются в шлаке (tKim > tpacraiaBa )• Подачу хлора в этот момент увеличивают, так как нет разбрызгивания. Образующийся шлак по мере накопления снимают, добавляют новую порцию флюсов.
Окончание процесса определяют по желтому налету Аи или красного АиСЬ на трубках. С поверхности расплава снимают остатки шлака, золото сливают в миксер и разливают в слитки. Шлаки и хлориды содержат запутавшиеся корольки Аи, поэтому их плавят при t=1100°C. Расплав расслаивается: внизу хлориды, сверху- шлак.
На поверхность шлака небольшими порциями загружают соду, часть Ag восстанавливается по реакции:
4AgCl + 2Na2CO} = 4Ag+4NaCl+2C02+02;
Ag опускается на дно тигля, увлекая большую часть Аи из хлоридов
.
Вводят 4% №2СОз от массы хлоридов, при этом восстанавливается 20% Ag, что обеспечивает высокое извлечение Аи.
Полученный Au- Ag сплав направляют на хлорирование. Из обеззолоченных хлоридов выделяют Ag (в хлоридах содержится: 70% AgCI, остальное Си, Na, Pb).
Ag выделяют двумя способами:
1. Хлориды дробят до крупности - 25мм и многократно обрабатывают во вращающихся бочках 5% раствором NaCl,
подкисленным НС1.
Хлориды Na и РЬ переходят в раствор.
Малорастворимый хлорид меди (CuCl) в присутствии СГ переходит в раствор: CuCl + СГ * СиСЬ".
2. Хлориды гранулируют, выливая их в воду. Гранулы (-2мм) обрабатывают хлоратом натрия (NaClCb) в присутствии НС1. Си переходит в раствор.
2 CuCl + СЮз + СН+ = 6Си + + 7СГ + ЗН20.
Очищенный хлорид Ag восстанавливают Zn. Губчатое Ag промывают, сушат и переплавляют в аноды. Чистота металла 998 - 999 пробы. Аи получают 995 - 996 пробы.
Метод хлорирования проще и дешевле электролитического, но не позволяет получать Аи высокой пробы (! Недостаток).
Недостаток: кроме 1 в том, что высокие потери Ag и Pt металлов. Все Pt металлы остаются в Аи.
Электролитическое рафинирование Ag
Анод - растворимый (серебряный сплав).
Катод - Ag (чистое).
Электролит
- водный раствор (AgN03
+
HNO3)
10-
20 г/л .
Ag
AgN03,
HNO3, Н20,
примеси
Ag
(катод)
)
На A: Ag — Ag++ е; <p Ag/Ag+ = + 0,799 В.
Au, Pt, Pd переходят в шлам, так как более электроположительны
.о .
ф Н20/02 > ф Ag,
!!!2Н20 4Н++02+4е, ф 0 = +1,23 В - реакция невозможна !!!
На А : Си, Pt, Bi, Zn, Fe и другие, более электроотрицательные , чем Ag
переходят в раствор . На К : основной процесс Ag+ + е —> Ag.
Выделение Н по реакции: 2Н +2е * Н2; ф0 = 0 ; невозможно,
так как ф 0 Ag> Ф ш •
Возможно восстановление: ЫОз"+2Н+ +е * N02 + H20;
NOf + 4Н+ + Зе N0 + 2НЮ; 2NOi + 10Н+ + 8е N20+ 5Н20.
Эти реакции возможны при повышенной кислотности раствора (HNO3 необходима для повышения электропроводности электролита).
Чрезмерное повышение рН приводит к уменьшению выхода по току Ag. Кроме того, увеличивается растворимость Pt и Pd на аноде. Иногда для повышения электропроводности вводят FINO3 (до 15 г/л).
