
- •Пищевые белки как источник аминокислот. Качественный состав и биологическая ценность пищевых белков.
- •Динамическое состояние белков в организме. Нормы белка в питании. Азотистый баланс.
- •П ереваривание белков
- •Протеиназы пищеварительного тракта (общая характеристика и классификация)
- •Минеральный состав желудочного сока. Роль соляной кислоты в процессах пищеварения.
- •Виды кислотности желудочного сока, определение и расчет всех видов кислотности по михаэлису.
- •Проферменты пищеварительных протеиназ, механизм превращения в ферменты. Субстратная специфичность протеиназ.
- •Желудочные протеиназы: пепсин, гастриксин, их роль в переваривании белков.
- •Методы количественного определения пепсина.
- •Химический состав панкреатического и кишечного соков. Роль панкреатических и кишечных протеиназ в переваривании белков.
- •Б иохимические механизмы регуляции пищеварения, гормоны желудочно-кишечного тракта. Всасывание аминокислот.
- •Общая схема источников и путей расходования аминокислот в тканях. Экзогенный и эндогенный пул аминокислот
- •Трансаминирование, химизм. Трансаминазы, их специфичность. Роль витамина в6 в трансаминировании.
- •Биологическая роль реакций трансаминирования
- •Определение трансаминаз в сыворотке крови.
- •Д езаминирование аминокислот
- •Окислительное дезаминирование химизм. Роль глутаматдегидрогеназы. Биологическая роль окислительного дезаминирования аминокислоты.
- •Непрямое дезаминирование аминокислот, понятие, стадии, биологическое значение.
- •Декарбоксилирование аминокислот, химизм, ферменты, субстратная специфичность декарбоксилаз.
- •Биогенные амины, механизм образования, влияние на процессы метаболизма и физиологические функции. Окисление биогенных аминов.
- •Образование катехоламинов и гамк, функции аминов.
- •Понятие о свободном амином азоте. Принцип метода определения, диагностическое значение.
- •Трансметилирование. Метионин и s-аденозилметионин. Роль метионина в биосинтезе биологически важных соединений, в реакциях обезвреживания.
- •Тетрагидрофолиевая кислота и ее роль в синтезе и переносе одноуглеродных радикалов.
- •Обмен фенилаланина и тирозина. Пути превращения в норме.
- •Врожденные нарушения обмена ароматических аминокислот. Методы предупреждения, диагностики и лечения врожденных нарушений обмена фенилаланина и тирозина.
- •Наследственные нарушения обмена других аминокислот.
- •Понятие о скрининг-тестах.
- •Качественное открытие фенилпировиноградной и гомогентезиновой кислот.
- •Конечные продукты азотистого обмена. Основные источники аммиака в организме.
- •О безвреживание аммиака в месте образования в организме.
- •Транспортные формы обезвреженного аммиака
- •Г люкозо-аланиновый цикл
- •Синтез мочевины как путь окончательного обезвреживания аммиака. Химизм, ферменты, энергетика. Биологический смысл цикла мочевинообразования, связь с цтк.
- •Нарушения синтеза и выведения аммиака. Причины уремии.
- •Патология азотистого обмена.
- •Определение мочевины в сыворотке крови. Диагностическое значение.
- •Креатин и креатинин. Количественное определение креатинина, роль, диагностическое значение.
- •Образования аммонийных солей
Понятие о свободном амином азоте. Принцип метода определения, диагностическое значение.
Свободный аминный азот сыворотки крови - азот свободных аминокислот, содержащихся в сыворотке крови (в основном глу и асп)
Принцип метода количественного определения основан на способности нингидрина взаимодействовать с продуктами деградации аминокислот и давать сложный комплекс сине-фиолетового цвета. Интенсивность развивающегося окрашивания пропорциональна количеству свободных аминокислот. Определение проводятся в 3 этапа:
1. Осаждение белков, при этом сыворотка освобождается от α-аминного азота белковых молекул.
2. Реакция свободных аминокислот с нингидрином.
3. Электрофотоколориметрия и расчет.
Увеличение содержания свободных аминокислот в крови имеет ме-сто при деструктивных состояниях: печеночной коме, острой желтой атрофии печени, при отравлениях (фосфором, фенилгидразином, СС14, хлороформом), при квашиоркоре, тяжелых ожогах, шоке, истощающих поносах, после кровотечений. Уменьшение уровня аминокислот характерно для почечных поражений, для гиперпродукции инсулина, гормона роста, андрогенов
Трансметилирование. Метионин и s-аденозилметионин. Роль метионина в биосинтезе биологически важных соединений, в реакциях обезвреживания.
Трансметилирование (син. переметилирование)– реакции переноса метильной группы от донора к акцептору
М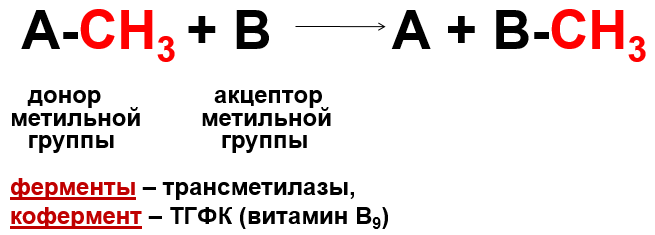 етионин -
незаменимая аминокислота, участвует в
реакциях дезаминирования, является
источником атома серы для синтеза
цистеина. Метионил-тРНК участвует в
инициации процесса трансляции. Метальная
группа метионина - мобильный одноуглеродный
фрагмент, используемый для синтеза ряда
соединений. Перенос метильной группы
метионина на соответствующий акцептор
называют реакцией трансметилирования.
Метальная группа в молекуле метионина
прочно связана с атомом серы, поэтому
непосредственным донором этого
одноутлеродного фрагмента служит
активная форма аминокислоты.
етионин -
незаменимая аминокислота, участвует в
реакциях дезаминирования, является
источником атома серы для синтеза
цистеина. Метионил-тРНК участвует в
инициации процесса трансляции. Метальная
группа метионина - мобильный одноуглеродный
фрагмент, используемый для синтеза ряда
соединений. Перенос метильной группы
метионина на соответствующий акцептор
называют реакцией трансметилирования.
Метальная группа в молекуле метионина
прочно связана с атомом серы, поэтому
непосредственным донором этого
одноутлеродного фрагмента служит
активная форма аминокислоты.
Реакция активация метионина Активной формой метионина является S-аденозилметионин (SAM) - сульфониевая форма аминокислоты, образующаяся в результате присоединения метионина к молекуле аденозина. Аденозин образуется при гидролизе АТФ. Эту реакцию катализирует фермент метионин аденозилтрансфераза, присутствующий во всех типах клеток. Структура (-S+-CH3) в SAM - нестабильная группировка, определяющая высокую активность метильной группы (отсюда термин "активный метионин"). Эта реакция уникальна для биологических систем, так как, по-видимому, является единственной известной реакцией, в результате которой освобождаются все три фосфатных остатка АТФ. Отщепление метильной группы от SAM и перенос её на соединение-акцептор катализируют ферменты метилтрансферазы. SAM в ходе реакции превращается в S-аденозилгомоцистеин (SAT)
Синтез фосфатидилхолина из фосфатидилэтиноламина
Ф осфатидилхолины
(лецитины) - наиболее распространённая
группа глицерофосфолипидов, участвующих
в образовании мембран клеток и
липопротеинов, в составе которых
осуществляется транспорт липидов
осфатидилхолины
(лецитины) - наиболее распространённая
группа глицерофосфолипидов, участвующих
в образовании мембран клеток и
липопротеинов, в составе которых
осуществляется транспорт липидов
С интез
креатина.Креатин
необходим для образования в мышцах
высокоэнергетического соединения -
кре-атинфосфата. Синтез креатина идёт
в 2 стадии с участием 3 аминокислот:
аргинина, глицина и метионина. В
почках образуется
гуанидинацетат при действии
глицинамидинотрансферазы
интез
креатина.Креатин
необходим для образования в мышцах
высокоэнергетического соединения -
кре-атинфосфата. Синтез креатина идёт
в 2 стадии с участием 3 аминокислот:
аргинина, глицина и метионина. В
почках образуется
гуанидинацетат при действии
глицинамидинотрансферазы
З атем
гуанидинацетат транспортируется в
печень, где
происходит реакция его метилирования
атем
гуанидинацетат транспортируется в
печень, где
происходит реакция его метилирования
Креатин с кровотоком переносится в мышцы и клетки мозга, где из него образуется высокоэнергетическое соединение - креатинфосфат. Определение содержания креатина и креати-нина в крови и моче используется для характеристики интенсивности работы мышц в спортивной медицине и при некоторых патологических состояниях. Определение активности фермента креатинкиназы и его изоферментных форм в крови используется в медицине для диагностики таких заболеваний, как инфаркт миокарда, миопатии, мышечные дистрофии и др.
Р еакции
трансметилирования используются также
для:
еакции
трансметилирования используются также
для:
синтеза адреналина из норадреналина;
синтеза анзерина из карнозина;
метилирования азотистых оснований в нук-леотидах и др.;
инактивации метаболитов (гормонов, медиаторов и др.) и обезвреживания чужеродных соединений, включая и лекарственные препараты.
В организме метилированию могут подвергаться амины, фенолы и тиолы. В результате метилирования образуются соответствующие N-, О- и S-метильные конъюгаты. При метилировании чужеродных соединений и некоторых метаболитов переносчиком метильных групп является кофермент S-аденозилметионин. С участием метильных групп этого кофермента происходит метилирование перечисленных выше соединений. Реакции метилирования происходят под влиянием ферментных систем (метилтрансфераз)
