
- •1. Химическая природа и строение ферментов
- •1.1. Химическая природа ферментов
- •1.2. Активный центр ферментов
- •1.3. Изоферменты
- •2. Основные свойства ферментов
- •2.1.Отличие от неорганических катализаторов
- •2.2 Субстратная специфичность действия ферментов
- •Термолабильность ферментов
- •Зависимость активности ферментов от рН-среды
- •2.5. Активность ферментов
- •3. Механизм действия ферментов.
- •4. Основы кинетики ферментативного катализа
- •5. Факторы, определяющие активность ферментов. Активаторы и ингибиторы ферментов.
- •6. Классификация и номенклатура ферментов
- •Примеры реакций катализируемых ферментами различных классов:
- •Количественная оценка активности ферментов
5. Факторы, определяющие активность ферментов. Активаторы и ингибиторы ферментов.
Существенное влияние на активность ферментов оказывает наличие в среде определенных химических веществ – эффекторов. Эффекторы могут повышать активность ферментов (активаторы) и подавлять ее (ингибиторы). В качестве ингибиторов или активаторов часто могут выступать ионы металлов. Иногда ион металла является постоянным, прочно связанным компонентом активного центра фермента, т.е. фермент относится к металлосодержащим сложным белкам, или металлопротеидам.
Активация некоторых ферментов может происходить с использованием другого механизма, предусматривающего протеолитическое расщепление неактивных предшественников ферментов (проферментов или зимогенов) с образованием активных ферментов (например, трипсина).
Различают обратимое и необратимое ингибирование. Необратимое ингибирование приводит к формированию стабильного комплекса ингибитора с ферментом, ведущее к его необратимой инактивации. Чаще происходит обратимое ингибирование, которое разделяют на конкурентное, неконкурентное и бесконкурентное.
При конкурентном ингибировании ингибитор (I) связывается с активным центром фермента и конкурирует за него с субстратом. Конкурентный ингибитор обычно структурно похож на субстрат, однако фермент не способен катализировать реакцию в присутствии ингибитора из-за отсутствия у последнего необходимых функциональных групп.
Схема конкурентного ингибирования выглядят следующим образом:
|
|
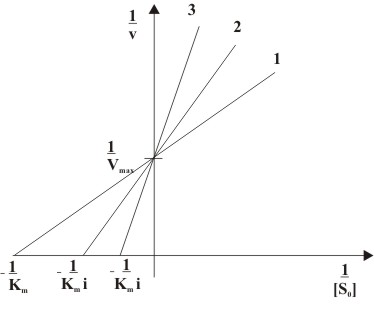
Рис. 2: Конкурентное ингибирование при различных концентрациях ингибитора в двойных обратных координатах
На графике Лайнуивера-Берка в двойных обратных координатах (зависимость 1/v0 от 1/[S]) видно, что при конкурентном ингибировании максимальная скорость реакции Vmax не меняется, а константа Михаэлиса увеличивается . Поэтому при разных концентрациях ингибитора получают семейство прямых с различным наклоном, пересекающихся в одной точке на оси ординат.
Неконкурентный ингибитор не имеет структурного сходства с субстратом и поэтому не мешает связыванию субстрата с ферментом. Он способен присоединяться как к свободному ферменту, так и к фермент-субстратному комплексу с одинаковой эффективностью. Ингибитор вызывает такие конформационные изменения, которые не позволяют ферменту превращать субстрат в продукт, но не влияют на сродство фермента к субстрату.
Схема неконкурентного ингибирования выглядят следующим образом:
|
|
![]()
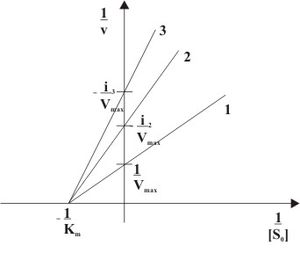
Рис. 3: Неконкурентное ингибирование в двойных обратных координатах при различных концентрациях ингибитора
При неконкурентном ингибировании константа Михаэлиса не изменяется, а максимальная скорость реакции уменьшается. Поэтому в двойных обратных координатах семейство прямых, отвечающих разным концентрациям ингибитора, пересекается в одной точке на оси абсцисс (Рис.3).
При бесконкурентном ингибировании ингибитор связывается только с фермент-субстратным комплексом, но не со свободным ферментом. Субстрат, связываясь с ферментом, изменяет его конформацию, что делает возможным связывание с ингибитором. Ингибитор, в свою очередь, так меняет конформацию фермента, что катализ становится невозможным.
Схема и уравнение Михаэлиса-Ментен в случае бесконкурентного ингибирования:
|
|
Максимальная скорость реакции и кажущаяся константа Михаэлиса уменьшаются в одинаковое число раз. Поэтому в двойных обратных координатах для разных концентраций ингибитора получаем семейство параллельных прямых.
Аллостерические ингибиторы связываются с отдельными участками фермента вне активного центра. Такое связывание влечет за собой конформационные изменения в молекуле фермента, которые приводят к уменьшению его активности. Аллостерические эффекты встречаются практически только в случае олигомерных ферментов. Кинетику таких систем нельзя описать с помощью простой модели Михаэлиса-Ментен.
