
- •Раздел 1. Оптические методы анализа
- •1.1.2. Аппаратура и принадлежности для фотометрического анализа Колориметр фотоэлектрический концентрационный кфк-2
- •1. Описание прибора
- •2. Подготовка к работе
- •3. Порядок работы
- •3. 1. Измерение коэффициента пропускания
- •3. 2. Определение концентрации вещества в растворе
- •3.2.1. Выбор светофильтра.
- •3.2.2. Выбор кюветы.
- •3.2.3. Построение градуировочного графика для данного вещества.
- •3.2.4. Определение концентрации вещества в растворе.
- •Фотометр фотоэлектрический кфк-3-01
- •1. Описание прибора
- •1. Подготовка к работе
- •3. Порядок работы.
- •3. 1. Измерение коэффициента пропускания или оптической плотности
- •3. 2. Измерение концентрации вещества в растворе
- •3.2.1. Выбор длины волны.
- •3.2.2. Выбор кюветы.
- •3.2.3. Построение градуировочного графика и определение коэффициента факторизации.
- •3.2.4. Введение коэффициента факторизации f в память вычислительного блока.
- •3.2.5. Измерение концентрации вещества в растворе.
- •Спектрофотометр сф-26
- •1. Описание прибора
- •2. Подготовка к работе
- •3. Порядок работы
- •3. 1. Подготовка к измерению
- •3. 2. Измерение коэффициента пропускания
- •3. 3. Измерение коэффициента пропускания светофильтров и образцов в кюветах.
- •3. 4. Измерение в диапазоне показаний 0 — 10%
- •Лабораторная работа № 1. Тема: «Определение железа (III) в питьевой воде».
- •Ход определения
- •Дополнительные задания:
- •Определите концентрацию железа методом добавок, для чего постройте на миллиметровой бумаге калибровочный график как на рисунке 8.
- •1.1.3.Определение концентрации вещества методом добавок
- •Расчёт неизвестной концентрации по методу сравнения
- •Определение неизвестной концентрации графическим способом
- •Контрольные вопросы и задания
- •Лабораторная работа №2
- •Ход определении.
- •Нефелометрия и турбидиметрия.
- •1.2.1.Аналитические возможности и метрологические характеристики нефелометрии и турбидиметрии Аналитические возможности.
- •Метрологические характеристики.
- •1.2.2. Взаимодействие света со взвешенными частицами
- •1.2.3.Закон Рэлея
- •1.2.4. Приёмы нахождения неизвестной концентрации в нефелометрии и турбидиметрии
- •1.2.5. Приборы для нефелометрических и турбидиметрических измерений
- •Лабораторная работа №3 Тема: «Фототурбидиметрическое определение кальция».
- •Ход определения
- •Лабораторная работа № 4. Тема: «Определение сульфатов в питьевой воде».
- •Ход определения
- •Лабораторная работа № 5. Тема: «Определение хлоридов в питьевой воде»
- •Ход определения
- •Лабораторная работа работа №6 Тема: «Определение хлоридов в питьевой воде».
- •Ход определения.
- •1.3. Рефрактометрический метод анализа
- •1.3.1. Теоретические основы рефрактометрии
- •1.3.2 Аппаратура и принадлежности для рефрактометрии Рефрактометр Аббе nar-1t
- •1. Описание прибора
- •1. Окуляр.
- •12. Измерительная ручка
- •2. Калибровка прибора с дистиллированной водой
- •3.Измерение коэффициента преломления
- •Лабораторная работа №7 Тема: «Определение сахара в виноградном соке и сусле».
- •Ход определения.
- •Лабораторная работа №8 Тема: «Определение сахарозы в сладких творожных продукта»
- •Ход определения.
- •Лабораторная работа №9. Определение концентрации хлорида натрия в водном растворе
- •Ход определения
- •Лабораторная работа №10 Тема: «Определение лактозы в молоке и кисломолочных продуктах».
- •Ход определения
- •Объяснить относительно невысокую селективность рефрактометрического метода анализа.
- •Раздел 2. Электрохимические методы анализа
- •2.1.Потенциометрия
- •2.1.1.Теоретические основы потенциометрии
- •2.1.2. Электроды
- •2.1.3 Виды потенциометрического метода анализа
- •Раствора FeCl3 раствором SnCl2
- •Аппаратура и принадлежности для потенциометрического анализа Настольный рН-метр - рН 211
- •Описание прибора.
- •Калибровка прибора по одной точке.
- •Калибровка по двум точкам.
- •Порядок работы.
- •Анализатор жидкости многопараметрический экотест − 2000
- •Описание прибора.
- •Порядок работы.
- •2.1 Измерение рХ (рН) в режиме “рН-метр-иономер”
- •2.1.1 Ионометрические измерения без термокомпенсации
- •2.1.1.1 Выбор ионометрического канала
- •2.1.1.2 Градуировка ионометрического канала
- •Выбор режима
- •2.1.1.3 Просмотр предыдущих градуировок
- •Сl Заряд -
- •Выбор режима
- •2.1.1.4 Проведение измерений
- •Сl Заряд -
- •2.1.2 Ионометрические измерения с термокомпенсацией
- •2.1.2.1 Ввод координат изопотенциальной точки
- •2.1.2.2 Ввод значения температуры раствора
- •2.1.2.3 Проведение измерений
- •Лабораторная работа №11
- •Ход работы.
- •Лабораторная работа №12
- •Ход работы.
- •Лабораторная работа №13
- •1. Назначение.
- •2. Метод анализа.
- •3. Подготовка к выполнению измерений
- •4. Выполнение измерений.
- •5. Обработка результатов измерения.
- •6. Оформление результатов измерений.
- •2.2. Кондуктометрия
- •2.2.1. Теоретические основы кондуктометрии
- •2.2.2. Прямая кондуктометрия
- •2.2.3.Кондуктометрическое титрование
- •2.2.4. Аппаратура и принадлежности для кондуктометрического анализа Настольный кондуктометр hi 2300
- •Описание прибора
- •Калибровка электропроводности/общей минерализации
- •Порядок работы
- •Лабораторная работа №14 Тема: «Определение лимонной кислоты в плодово-ягодном сырье».
- •Ход определения
- •Лабораторная работа № 15. Тема: «Определение аминокислот (глицина, аланина, валина, лейцина, серина) в растворе».
- •Ход определения
- •Лабораторная работа № 16. Тема: «Определение общей жесткости воды».
- •Ход определения
- •Раздел 1. Оптические методы анализа…………………………………………….
- •1.1.Фотометрические методы анализа……………………………………………
- •Раздел 1. Электрохимические методы анализа……………………………………..
- •Мальевская Елена Владимировна Кудырко Татьяна Геннадьевна Лабораторный практикум по физико-химическим методам анализа
- •230028, Г. Гродно, ул. Терешковой, 28
- •230028, Г. Гродно, ул. Терешковой, 28
Лабораторная работа работа №6 Тема: «Определение хлоридов в питьевой воде».
Сущность работы. Определение основано на фототурбидиметрическом титровании хлоридов, образующих при добавлении нитрата серебра коллоидно-дисперсный осадок AgCl. Помутнение (оптическая плотность) раствора возрастает при добавлении стандартного раствора титранта. После достижения точки стехиометричности оптическая плотность остается постоянной при введении новых порций титранта. На кривой титрования появляется точка перегиба, соответствующая объему титранта, израсходованному на реакцию с хлорид-ионами.
Реактивы и посуда:
1. Нитрат серебра 0,005-0,01 моль/л стандартный раствор.
2. Азотная кислота 0,1 моль/л раствор.
3. Бюретка
4. Пипетки
5. Химический стакан вместимостью 100 мл.
6. Кюветы с толщиной слоя 1см.
Ход определения.
В химический стакан помещают 25 или 50 мл анализируемой питьевой воды, подкисляют 2-3 мл азотной кислоты и титруют стандартным раствором AgNO3.После введения каждой порции титранта раствор перемешивают, часть оттитрованного раствора помещают в кювету и измеряют оптическую плотность (контроль – дистиллированная вода).
Раствор из кюветы присоединяют ко всей пробе анализируемой воды, добавляют очередную порцию титранта и т.д. По полученным данным строят кривую титрования – график зависимости оптической плотности от объема введенного титранта—и фиксируют положение точки стехиометричности.
Содержание хлоридов в питьевой воде (Q, мг Cl-/л) вычисляют по формуле:
![]() Q=
Q=![]() (16)
(16)
Где С—молярная концентрация стандартного раствора AgNO3.
Vt—израсходованный на титрование объем стандартного раствора AgNO3,
V0—взятый для титрования объем питьевой воды ,мл;
М—молярная масса хлора, г/моль.
Контрольные вопросы и задания.
1.Перечислить анионы, которые могут содержаться в питьевой воде, и указать методы их определения.
2. Как проводят фототурбидиметрическое титрование хлоридов и какие требования предъявляют при этом?
3. Обосновать характер кривой фототурбидиметрического титрования при определении хлоридов.
1.3. Рефрактометрический метод анализа
1.3.1. Теоретические основы рефрактометрии
Метод основан на зависимости показателя преломления n от концентрации двухкомпонентных растворов или смесей двух жидкостей.
Рефрактометрический метод анализа характеризуется относительной простотой аппаратуры и техники выполнения при высокой точности измерения показателя преломления. Прибор (рефрактометр) позволяет измерять показатель преломления с точностью до 1 · 10-4, т.е. до 10-2 %.
Рефрактометрия – пример оптического экспрессного микрометода: для измерения показателя преломления в течение нескольких минут достаточно 1 – 2 капель анализируемой жидкости. Метод основан на преломлении луча света при переходе из одной среды в другую. Если луч света проходит перпендикулярно поверхности раздела сред, то его направление при этом не изменяется (рис. 13, а, б; луч A – A`).
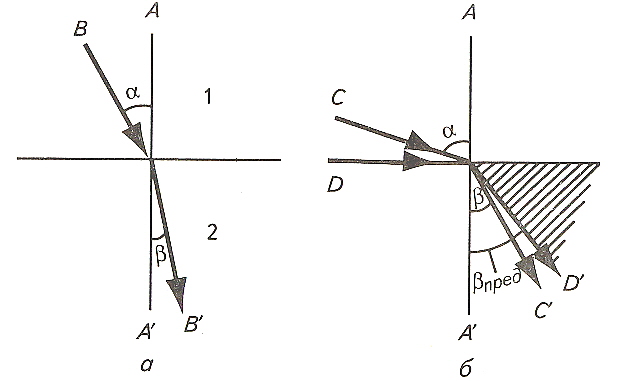
Рис. 13 Преломление луча света при переходе из одной среды в другую:
а – преломление луча света при прохождении из менее плотной среды 1 в более плотную среду 2;
б – преломление луча света при углах падения, приближающихся к 90º; предельный луч D- D` (полное внутреннее отражение)
Когда угол падения меньше 90º, направление луча света при переходе из одной среды в другую изменяется, луч преломляется (луч B – B`).
Различают угол падения α (между направлением падающего луча В и перпендикуляром к поверхности раздела сред А) и угол преломления β (между направлением преломлённого луча и перпендикуляром А). Отношение синусов этих углов представляет собой показатель преломления среды, в которую луч света входит из другой среды:
![]() (17)
(17)
При прохождении луча света из среды с меньшим значением n в среду с большим показателем преломления (рис. 22, а) β < α. Если угол падения α луча С (рис. 13, б) приближается к 90º, β < 90º. При дальнейшем увеличении угла падения (луч D) падающий свет полностью отражается от границы раздела и не попадает в менее плотную среду, происходит полное внутреннее отражение. Справа (при наблюдении против светового потока) от предельного луча D1 находится затемнённое поле, слева – освещённое поле.
Рефрактометрия основана на измерении относительных показателей преломления веществ. Показатель преломления – постоянная величина для каждого вещества, являющаяся его характеристикой, подобно температуре плавления, кипения, плотности и т.д. Различают абсолютный N и относительный n показатели преломления.
Значение абсолютного показателя преломления воздуха по отношению к вакууму составляет:
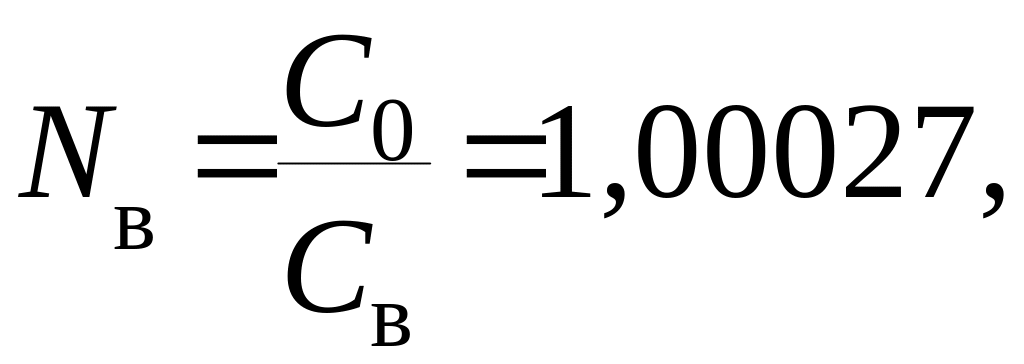 (18)
(18)
где С0 – скорость светового луча в вакууме (С0=3*108м/с);
Св – скорость светового луча в воздухе.
Наибольшую скорость световой луч имеет в вакууме. В воздухе световой луч имеет меньшую скорость из-за большей оптической плотности воздуха. Для удобства показатели преломления других веществ измеряют относительно воздуха и их значения приводят в справочниках.
Относительный показатель преломления n – это отношение скорости света в воздухе (Св) к скорости света в данной среде (Сс):
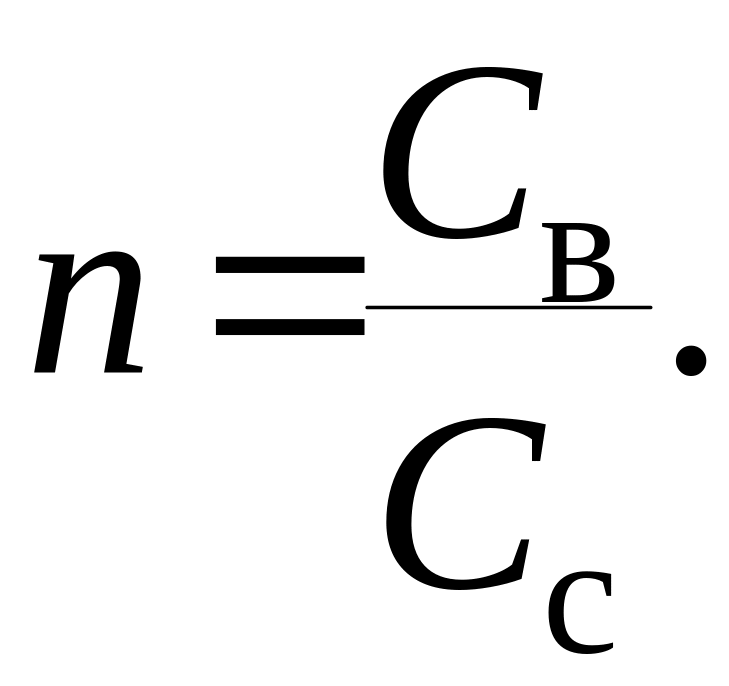 (19)
(19)
Абсолютный N и относительный n показатели преломления связаны между собой:
![]() (20)
(20)
Обычно величину n считают равной N и называют показателем преломления. Его можно представить как отношение синуса угла падения света на поверхность раздела двух сред к синусу угла преломления:
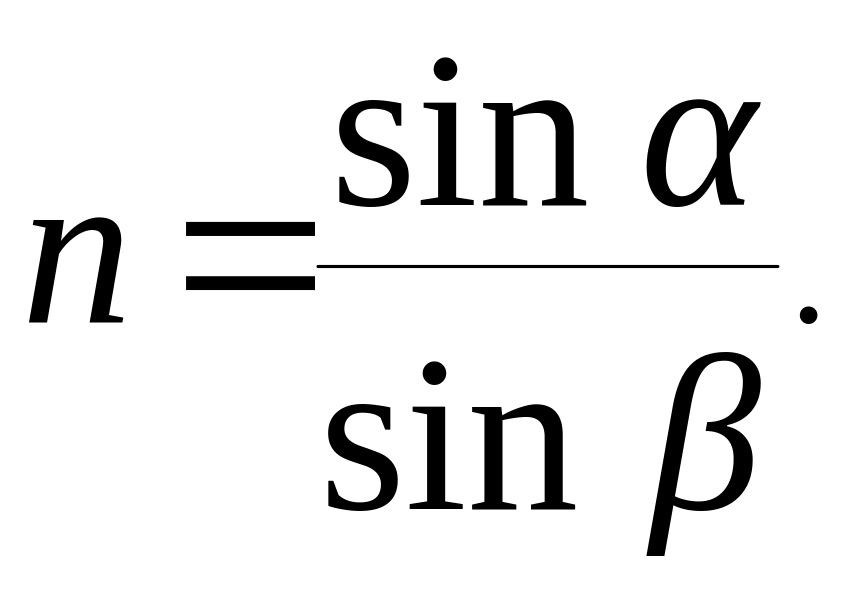 (21)
(21)
Показатель преломления зависит от длины волны падающего света, природы вещества, температуры и плотности раствора, типа растворителя. В связи с этим показатель преломления вещества измеряют при монохроматическом свете и постоянной температуре. Температуру и длину волны света указывают у символа n. При повышении температуры показатель преломления вещества уменьшается плотность вещества.
Как уже указывалось, каждое вещество имеет постоянный показатель преломления, а поэтому отношение синусов угла α и β также является постоянной величиной. Угол падения луча α можно увеличить до 90°(его предельно возможного значения), при этом падающий луч пойдет вдоль границы раздела сред и, преломившись, даст предельный угол преломления β. Так как sin 90°=1, зависимость примет вид:
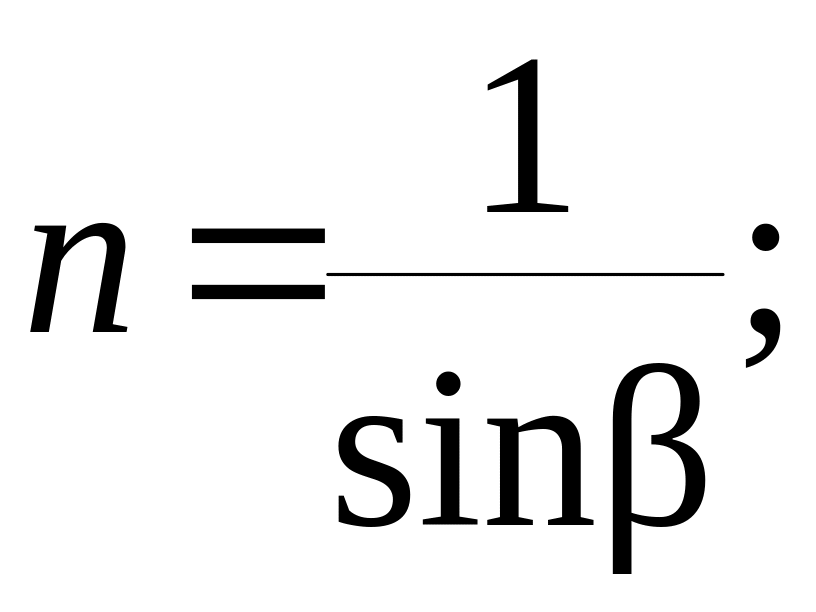
![]() (22)
(22)
Угол падения 90° называют предельным углом падения, а угол преломления при достижении предельного угла падения называют предельным углом преломления.
Если в качестве среды используют не воздух, а любые другие среды, то каждая из них характеризуется своим показателем и предельным углом преломления. В этом случае можно записать равенство:
![]()
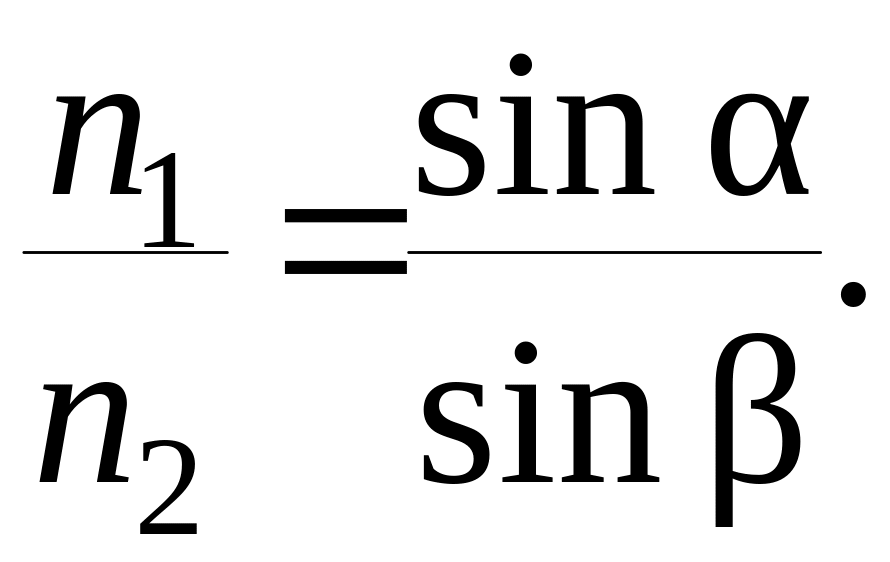 (23)
(23)
Это равенство характеризует преломление светового луча на границе любых двух сред и используется в рефрактометрах. Для измерения показателя преломления в рефрактометрах в качестве сред используют раствор вещества и стекло. Для стекла известен показатель преломления n2. Проходя границу раздела раствор – стекло, луч света преломляется. Если угол падения β1 луча в растворе равен 90°, то sinβ1=1. В этом случае мы получаем уравнение, которое позволяет измерять показатель преломления раствора n1 по значению предельного угла преломления β2 в стекле:
![]() (24)
(24)
Следовательно, чтобы определить показатель преломления исследуемого вещества, надо знать показатель преломления одной из сред и измерить величину предельного угла преломления β2.
