
- •Контрольная работа № 1 Теоретические основы строения органических соединений и факторы, определяющие иx реакционную способность
- •I. Пространственное строение органических молекул
- •II Взаимное влияние атомов и способы его передачи в молекулах opгaнических соединений
- •III. Кислотность и основность органических соединений
- •V. Реакции Sn у sр3-гибридизованного атома углерода - гетеролитические реакции, обусловленные поляризацией δ-связи углерод-гетероатом (монофункциональные производные углеводородов)
- •VI. Реакции An - гетеролитические реакции с участием π-связи углерод-гетероатом (реакционная способность альдегидов и кетонов)
- •VII. Реакции sn у sp2 -гибридизованного атома углерода (карбоновые кислоты и их функциональные производные)
- •Упражнения
V. Реакции Sn у sр3-гибридизованного атома углерода - гетеролитические реакции, обусловленные поляризацией δ-связи углерод-гетероатом (монофункциональные производные углеводородов)
17. Влияние электронных, пространственных факторов и стабильности уходящих групп на реакционную способность соединений в реакциях Sn.
18. Реакции гидролиза галогенопроизводных.
19. Реакции алкилирования спиртов, фенолов, тиолов, сульфидов, аммиака и аминов. Биороль реакций алкилирования.
20. Роль кислотного катализа в SN
21 .Реакции элиминирования (Е). Повышенная СН - кислотность как причина реакций Е.
22. Реакции дегидрогалогенирования.
23. Реакции дегидратации.
VI. Реакции An - гетеролитические реакции с участием π-связи углерод-гетероатом (реакционная способность альдегидов и кетонов)
24. Реакции карбонильных соединений с водой, спиртами. Обратимость реакций, роль кислотного катализа.
25. Реакции карбонильных соединений с тиолами, обратимость реакций. Роль кислотного катализа.
26. Реакции карбонильных соединений с аммиаком и его производными. Роль кислотного катализа.
27. Гидролиз ацеталей и иминов.
28. Образование и гидролиз иминов как химическая основа пиридоксалевого
катализа.
29. Реакции альдольного присоединения. Основный катализ. Строение енолят-иона. Биороль реакции. Альдольное расщепление как реакция, обратная альдольному присоединению. Биороль процесса.
VII. Реакции sn у sp2 -гибридизованного атома углерода (карбоновые кислоты и их функциональные производные)
30. Реакции ацилирования и обратные имреакции гидролиза. Образование ангидридов и их гидролиз. Роль кислотного катализа.
31. Образование сложных эфиров и их гидролиз. Роль кислотного и основного катализа.
32. Образование сложных тиоэфиров и их гидролиз. Роль кислотного и основного катализа.
33. Образование амидов и их гидролиз. Роль кислотного катализа.
34. Ацилирующие реагенты (ангидриды, карбоновые кислоты, сложные
эфиры, сложные тиоэфиры). Сравнительная активность этих реагентов.
35. Ацилфосфаты и ацилкофермент А - природные макроэргические ацилирующие реагенты. Биологическая роль реакций ацилирования.
36. Реакции по типу альдольного присоединения с участием кофермента А как путь образования углерод-углеродной связи.
Упражнения
Приведите строение конформаций кресла
1. 3-амицоциклогексанкарбальдегид
2. циклогександиол-1,3
3 4-фенилциклогексанол
4. 1,2-дибром-4-метилциклогексан
5. циклогександиол -1,5
Изобразите в проекциях Ньюмена следующие конформации (задания 6 – 10) и дайте им энергетическую характеристику
6. янтарной кислоты
7. 3 аминопропантиола-1
8. 3–меркаптопропаналя
9. 2-хлорэтанола
10. этандиола-1,2
11. 3-хлорпропаналя
12. 2-гидроксипропановой кислоты
Укажите вид и знак электронных эффектов заместителей в молекулах органических соединений. Обозначьте эффекты графически
Салициловая кислота (о-гидроксибензойная)
Сульфаниловая кислота (п-аминобензолсульфокислота)
4-гидроксибутановая кислота
п-аминобензойная кислота
17. м-крезол (1-гидрокси-3-метилбензол.)
18 Этиламин
19. Фенол
20. Анилин
Расположите соединения в порядке увеличения кислотности. Ответ объясните
Этанол и коламин
Фенол, 4-гидроксибензальдегид и 3-метилфенол
Трихлоруксусная кислота, 2,2-дихлорэтановая кислота и этановая
Этиленгликоль, пропанол-1 и глицерин
Фенол, меркаптобензол и бензиловый спирт
Пропанол-1, пропамин, пропантиол-1
Расположите соединения в порядке уменьшения основности.Ответ объясните
Анилин, 2-аминобензальдегид и 3-метианилин
м-метиланилин, этиамин и диэтиламин
Диэтиламин, этиламин и триметиламин
Метил-этиламин, триметиламин и трихлор-триметиламин
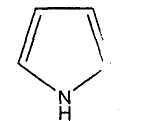
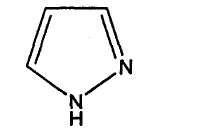
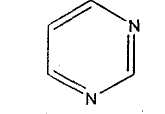
31. пиримидин 32. пиррол 33. пиразол
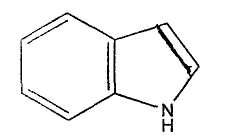
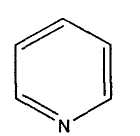
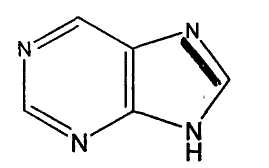
34. индол 35. пиридин 36. пурин
Укажите виды сопряжений в молекулах
37. Фенола
38. Анилина
39. Энтеросептола (5-хлор-7-иод-8-гидроксихинолина)
40. 4-аминофенола
41. Перечислите три пути генерирования радикальных частиц.
Напишите схемы и опишите механизм реакции
42. Гидратации пропена-2
43. Гидратации этилена
44. Гидрогалогенирования кротоновой (бутен-2-овой) кислоты
Укажите статистический и динамический факторы, стадии процесса, приведите современную формулировку правила Марковникова.
45. Галогенирования бензола
46. Алкилирования бензола пропеном в кислой среде
47. Алкилирования бензола йодистым метилом
48. Алкилирования бензола третичным изобутиловым спиртом в кислой среде
Приведите уравнения реакции образования Е+, стадии реакции, названия продуктов реакции (для заданий 45 – 48).
49. Напишите уравнение реакции образования S-аденозилметионина
50. Напишите уравнение реакции биосинтеза холина из коламина с участием S-аденозилметионина
Напишите схемы и опишите механизмы реакций
51. Дегидратации 2-метилбутанола-2
52. Гидратации трет. бутилхлорида
53. Взаимодействия 2-хлорпропановой кислоты с водным раствором щелочи
54. Третичного бутилового спирта с хлороводородом
55. Дигидрогалогенирования 2,3-диметил-2-хлорбутана
56. Дегидратации 2,3-диметилбутанола-2
57. Дегидрогалогенирования 2-метил-2-хлорбутана
Напишите схему реакции
58. Присоединения гидридов металлов к карбонильной группе (реакция восстановления)
59. Гидратации формальдегида. Как влияет строение субстрата на равновесие реакции?
60. Гидратации хлораля (2,2,2-трихлорэтаналь). Влияние ЭА заместителей на устойчивость гидратной формы
Напишите механизм реакции образования циклического полуацеталя
61. 4-гидроксибутаналя
62. 5-гидроксипентаналя
Напишите схемы и опишите механизмы реакций образования
63. Полуацеталя и ацеталя этанола
64. Оксима бутанола-2
65. Гидразона пропанола-2
66. Фенилгидразона пропаналя
67. Полумеркапталя и меркапталя пропанона-2 и метантиола
Напишите схемы и опишите механизмы реакций кислотного гидролиза всех полученных продуктов.
Напишите схему и опишите механизм реакции альдольной конденсации
68. Этаналя
69. Бензальдегида и этаналя
70. Пропаналя
Напишите формулы.
71. Предельных одноосновных кислот (С1-С6)
72. Непредельных одноосновных кислот (не менее трех)
73. Предельных двухосновных кислот (С2-С6)
74. Непредельных двухосновных кислот (изомеры бутен-2-диовой кислоты)
Назовите кислоты по тривиальной и заместительной номенклатуре.
75. Расположите карбоновые кислоты и их функциональные производные в порядке уменьшения ацилирующей способности (по легкости вступления в реакции SN).
76. Расположите карбоновые кислоты и их производные в порядке уменьшения стабильности уходящих анионов.
77. За счет чего возможно увеличение скорости реакции SN у sp2-гибридизованного атома углерода, каким образом оно достигается? Влияние ЭД и ЭА заместителей на увеличение или уменьшение δ+ атома углерода.
Напишите схему и опишите механизм реакции образования
78. Сложного эфира – этилацетата
79. Уксусного ангидрида
80. Амида масляной кислоты
Напишите схемы и механизмы реакции гидролиза этих соединений.
81. Напишите схему реакции образования хлорангидрида пропионовой кислоты. Напишите схему и опишите механизм реакции полученного продукта.
Напишите схемы реакций
82. Протекающих при нагревании щавелевой и адипиновой кислот, малоновой и янтарной кислот.
83. Образования неполного и полного амидов глутаровой кислоты.
Напишите схему реакции
84. Образования ацетилКоА (реакция ферментативного расщепления замещенного ацетилфостфата коферментом А)
85. Этерификации, протекающей в организме – образование ацетилхолина.
86. Опишите механизм реакции сложноэфирной конденсации (образование ацетоуксусного эфира их двух молекул этилацетата)
Опишите биороль КоА и ацетилКоА.
