
- •Тема: «Химия металлов» Технологическая карта комплекса
- •План лекции
- •Особенности электронного строения металлов.
- •Положение металлов в псхэ.
- •Закономерности в изменении свойств элементов – металлов.
- •Металлическая химическая связь. Кристаллические решетки.
- •Физические свойства металлов
- •Х имические свойства металлов.
- •Способы получения металлов
- •Закрепление знаний Контрольные вопросы
- •Задания и задачи
- •1. Написать уравнения реакций взаимодействия между веществами:
- •2. Расставить коэффициенты, найти окислитель и восстановитель в уравнениях реакций:
- •Химический диктант
- •Тест по теме «Общая характеристика металлов. Электрохимический ряд напряжений»
- •Ключ к тесту
- •Это интересно!
- •1.В начале был век медный.
- •II. Далее идёт век бронзовый.
- •III. Далее идет железный век.
- •Карточки задания для индивидуальной работы
- •Химические свойства
- •Характеристика элементов главной подгруппы II группы.
- •Химические свойства
- •Взаимодействие с простыми веществами.
- •Взаимодействуют с водой.
- •Взаимодействие с кислотами.
- •Взаимодействие с щелочами.
- •Характеристика элементов главной подгруппы III группы. Алюминий.
- •Строение атомов металлов изученных групп
- •Общие химические свойства
- •Закрепление и проверка знаний Контрольные вопросы
- •Упражнения и задачи для закрепления и проверки знаний
- •Железо.
- •Марганец
- •Химические свойства
- •Взаимодействие с неметаллами
- •Взаимодействие с водой
- •Взаимодействие с кислотами
- •Восстановление металлов из оксидов
- •Понятие о сплавах.
- •Задания для закрепления и проверки знаний Контрольные вопросы:
- •Характеристика элемента-металла на примере
- •Тест по теме «Металлы» Вариант 1
- •Вариант 2
- •Тест по теме «Металлы» Вариант 3
- •Вариант 4
- •Тест Вариант 1
- •Вариант 2
- •I уровень
- •II уровень
- •Контрольные вопросы, задания и тест для отработки нб по теме: «Химия металлов»
- •Тест «Химия металлов» Часть а (задания с выбором ответа)
- •Часть в (задания с кратким ответом)
- •Игровые задания Загадки о металлах
- •«Химические перевертыши»
- •Викторина по теме «Металлы»
- •Ответы на вопросы викторины
- •Определите металл
Понятие о сплавах.
Характерной особенностью металлов является их способность образовывать друг с другом или с неметаллами сплавы. Чтобы получить сплав, смесь металлов обычно подвергают плавлению, а затем охлаждают с различной скоростью, которая определяется природой компонентов и изменением характера их взаимодействия в зависимости от температуры. Иногда сплавы получают спеканием тонких порошков металлов, не прибегая к плавлению (порошковая металлургия). Итак сплавы - это продукты химического взаимодействия металлов.
Кристаллическая структура сплавов во многом подобна чистым металлам, которые, взаимодействуя друг с другом при плавлении и последующей кристаллизации, образуют: а) химические соединения, называемые интерметаллидами; б) твердые растворы; в) механическую смесь кристаллов компонентов.
Современная техника использует огромное число сплавов, причем в подавляющем большинстве случаев они состоят не из двух, а из трех, четырех и большего числа металлов. Интересно, что свойства сплавов часто резко отличаются от свойств индивидуальных металлов, которыми они образованы. Так, сплав, содержащий 50% висмута, 25% свинца, 12,5% олова и 12,5% кадмия, плавится всего при 60,5 градусах Цельсия, в то время как компоненты сплава имеют соответственно температуры плавления 271, 327, 232 и 321 градус Цельсия. Твердость оловянной бронзы (90% меди и 10% олова) втрое больше, чем у чистой меди, а коэффициент линейного расширения сплавов железа и никеля в 10 раз меньше, чем у чистых компонентов.
Однако некоторые примеси ухудшают качество металлов и сплавов. Известно, например, что чугун (сплав железа и углерода) не обладает той прочностью и твердостью, которые характерны для стали. Помимо углерода, на свойства стали влияют добавки серы и фосфора, увеличивающие ее хрупкость.
Среди свойств сплавов наиболее важными для практического применения являются жаропрочность, коррозионная стойкость, механическая прочность и др. Для авиации большое значение имеют легкие сплавы на основе магния, титана или алюминия, для металлообрабатывающей промышленности - специальные сплавы, содержащие вольфрам, кобальт, никель. В электронной технике применяют сплавы, основным компонентом которых является медь. Сверхмощные магниты удалось получить, используя продукты взаимодействия кобальта, самария и других редкоземельных элементов, а сверхпроводящие при низких температурах сплавы - на основе интерметаллидов, образуемых ниобием с оловом и др.
Задания для закрепления и проверки знаний Контрольные вопросы:
Как определить степени окисления металлов побочных подгрупп?
Какие степени окисления наиболее характерны для железа?
Назовите формулы оксидов и соответствующих им гидроксидов железа.
Охарактеризуйте кислотно-основные свойства гидроксидов железа (II) и железа
(III)?
Какие степени окисления характерны для хрома? Какие из них наиболее устойчивы?
Назовите формулы оксидов и гидроксидов хрома и охарактеризуйте их кислотно-основные свойства.
Как меняются окислительно-восстановительные свойства соединений хрома с
увеличением степени его окисления?
Напишите формулы хромовой и дихромовой кислот.
Какие степени окисления проявляет марганец в соединениях? Какие из них наиболее устойчивы?
Напишите формулы оксидов и гидроксидов хрома и охарактеризуйте их кислотно-основные свойства и окислительно-восстановительные свойства.
Как меняются окислительно-восстановительные свойства соединений марганца с увеличением степени его окисления?
Решение задач
Задачи первого уровня сложности
(оцениваются в 3 балла)
Сколько литров водорода (н. у.) потребуется для восстановления 6,4 г меди из оксида меди (II)?
Сколько граммов сульфида железа(II) образуется при взаимодействии 5,6 г железа с избытком серы?
Определите массу цинка, необходимого для взаимодействия с раствором, который содержит 19,6 г серной кислоты.
Задачи второго уровня сложности
(оцениваются в 4 балла)
Какой объем оксида углерода(II) (н.у.) потребуется для восстановления 4 г оксида железа(III)?
Определите массу алюминия, который потребуется для получения 78 г хрома из оксида хрома(III) алюминотермическим методом.
Какой объем оксида углерода (II) (н.у.) потребуется для восстановления 320 т оксида железа(III) до железа?
Задачи третьего уровня сложности
(оцениваются в 5 баллов)
Какой объем водорода (н.у.) выделится при взаимодействии 137 г цинка, содержащего 5 % примесей, с соляной кислотой?
Определите массу осадка, который образуется при взаимодействии растворов, один из которых содержит 9,8 г серной кислоты, а другой — 31,2 г хлорида бария.
Определите объем водорода (н.у.), который выделится при взаимодействии 230 г натрия с водой, если выход газа составляет 90 % (по объему).
Напишите уравнения реакций, соответствующие цепочкам превращения:
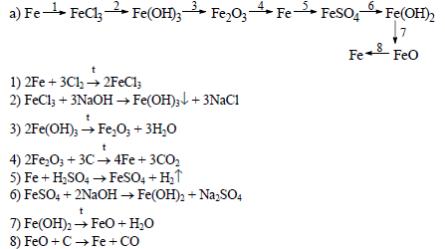
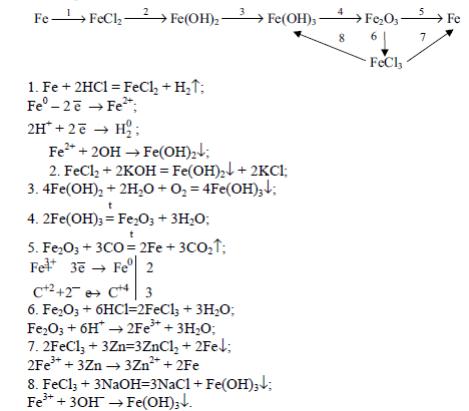
Запишите уравнения практически осуществимых реакций. Если реакция не протекает , укажите причину. Из букв, соответствующих правильным ответам, вы составите название планеты, с которой в древности соотносили железо.
а) Mg + НС1 → M
б) Zn+ H3P04→ Е
в) А1+ H2S04(pa36) → А
г) Ag + НС1 → Л
д) Fe + НС1 → Р
е) Pb+ H2S04(pa36) → К
ж) Al + НС1 → С
Составьте уравнения практически осуществимых реакций между веществами:
а) А1+ Hg(N03)2(p.p) →….
б) Zn + MgCl2(p.p→)
в) Fe+ ZnCl2(p.p) →
г) Zn+ Pb(N03)2(p.p) →….
Выберите химический элемент-металл из списка: натрий, литий, магний, калий, кальций, алюминий. Дайте его характеристику, вписав в текст пропущенные слова, цифры, знаки.
