
- •Контрольная работа № 1
- •1. Осаждение
- •Варианты
- •Расчётные формулы
- •2. Перемешивание
- •Варианты
- •Расчётные формулы
- •3. Фильтрование
- •Варианты
- •Расчётные формулы
- •Контрольная работа № 2
- •1. Теплообмен
- •Варианты
- •Расчётные формулы
- •2. Пластинчатый теплообменник
- •Варианты
- •Расчётные формулы
- •3. Выпаривание
- •Варианты
- •Расчётные формулы
- •Варианты
- •Расчётные формулы
- •4. Сушка
- •Варианты
- •Расчётные формулы
- •5. Абсорбция
- •Варианты
- •Расчетные формулы
- •Данные о равновесных составах для системы so2 – н2о
- •Характеристика насадки из колец Рашига
- •Приложения
- •Свойства насыщенного водяного пара в зависимости от давления
- •Основные теплофизические свойства воды
- •Основные физические свойства молока
Расчетные формулы
Некоторые способы выражения состава фаз двухкомпонентных систем жидкость–газ (пар) представлены в табл. 5.1.
Таблица 5.1
Концентрация |
Обозначение концентрации компонента А |
|
в жидкой фазе |
в газовой или паровой фазе |
|
Мольная доля,
|
х |
у |
Массовая доля,
|
|
|
Относительная массовая концентрация,
|
|
|
Для пересчета концентраций используются формулы
![]() ,
(5.1)
,
(5.1)
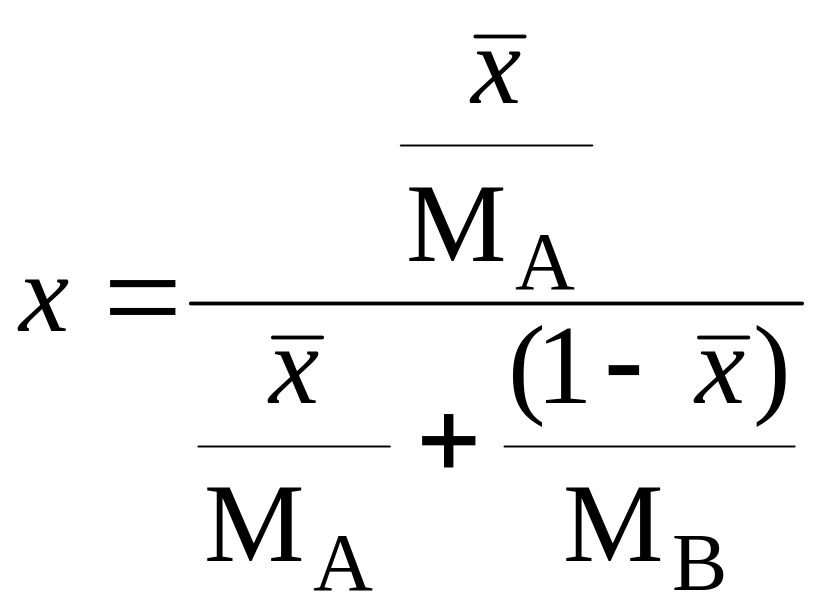 ,
(5.2)
,
(5.2)
![]() ,
(5.3)
,
(5.3)
![]() ,
(5.4)
,
(5.4)
где МА и МВ – мольная масса чистых компонентов А и В.
Уравнение равновесия для процесса абсорбции
![]() ,
(5.5)
,
(5.5)
где m – коэффициент
распределения (в общем случае величина
переменная, (см. табл. 5.2);
![]() – равновесная концентрация в компоненте
А в газовой фазе, мол. доля; х –
концентрация компонента В в жидкой
фазе, мол. доля.
– равновесная концентрация в компоненте
А в газовой фазе, мол. доля; х –
концентрация компонента В в жидкой
фазе, мол. доля.
Относительная массовая концентрация компонента А в жидкой фазе на выходе из абсорбера:
![]() .
(5.6)
.
(5.6)
Относительная массовая концентрация компонента В в газовой фазе
– на входе в абсорбер:
![]() .
(5.7)
.
(5.7)
– на выходе из абсорбера:
![]() .
(5.8)
.
(5.8)
Количество компонента А, поступающего в абсорбер с исходной смесью
![]() .
(5.9)
.
(5.9)
Количество компонента А, поглощенного в абсорбере, составит (кг/с):
![]() ,
(5.10)
,
(5.10)
где
![]() – расход компонента В, поступающего в
абсорбер, кг/с.
– расход компонента В, поступающего в
абсорбер, кг/с.
Расход воды на поглощение компонента А равен, кг/с:
![]() ,
(5.11)
,
(5.11)
или
![]() .
(5.12)
.
(5.12)
Для определения движущей силы процесса абсорбции необходимо построить на графике изображение рабочей линии и линии равновесия (см. рис. 5.1).
Уравнение рабочей линии для противоточного процесса абсорбции
![]() .
(5.13)
.
(5.13)
Линия равновесия строится по уравнению (5.4) с использованием экспериментальных данных для системы (SO2 – Н2О), полученных для t = 10ºС, П = 101,3 кПа (см. табл. 5.2), причем эти данные необходимо затем пересчитать в относительные массовые концентрации.
Таблица 5.2
