
Многоатомные спирты
Многоатомными называются спирты, содержащие в молекуле две гидроксильные группы и более. В зависимости от количества гидроксильных групп они делятся на двухатомные (две группы OH), или диолы; трехатомные, или триолы и т. д. Двухатомные спирты называют также гликолями.
Способы получения
Получают многоатомные спирты теми же способами, что и одноатомные, с той лишь разницей, что в молекулу вводится не одна, а несколько гидроксильных групп.
1. Гидролиз галогенпроизводных:
2 NaOH
CH3 – CH – CH2 – CH2 CH3 – CH – CH2 – CH2
- 2 NaCl
Cl Cl OH OH
1,3-дихлорбутан 1,3-бутандиол
2. Гидроксилирование алкенов (реакция Вагнера):
[O], H2O
СН3 – СН = СН2 СН3 – СН – СН2
пропилен
ОН ОН
1,2-пропандиол
В качестве окислителей применяется щелочной раствор КМnО4 или Н2О2.
3. Получение из α-оксидов:
H2O; H+
СН2 – СН – СН3 СН2 – СН – СН3
\ /
О ОН ОН
окись пропилена 1,2-пропандиол
При гидратации α-оксидов обычно образуются гликоли.
Физические и химические свойства
По своим физическим свойствам низшие гликоли – хорошо растворимые в воде вязкие жидкости, многие из которых обладают сладким вкусом. Введение в молекулу второй гидроксильной группы сильно сказывается на свойствах спиртов: диолы кипят при более высоких температурах, чем одноатомные спирты, что связано с появлением дополнительных водородных связей.
Химические свойства многоатомных спиртов близки к свойствам одноатомных. В реакциях может участвовать одна или несколько гидроксильных групп.
Повышенная подвижность атомов водорода гидроксильных групп (рКа СН2ОН–СН2ОН равна 14,7) – особенность многоатомных спиртов. Они превращаются в алкоголяты не только при взаимодействии с натрием или калием, но и с гидроксидами тяжелых металлов, образуя комплексные соединения:
H
H2C – O O – CH2
H2C – OH HO – CH2 \ /
+ Cu(OH)2 + Cu + 2H2O.
H2C – OH HO – CH2 / \
этиленгликоль H2C – O O – CH2
H
комплексное соединение
Окисление гликолей:
O O
СН2 – ОН [O] // [O] //
HO – CH2 – C HO – CH2 – C .
С Н2
– ОН \ \
Н2
– ОН \ \
H OH
этиленгликоль гликолевый альдегид гликолевая кислота
О О O O O O
\\ // [O] \\ // [O] \\ //
С – С C – C C – C .
/ \ / \ / \
Н Н H OH HO OH
глиоксаль глиоксиловая щавелевая
кислота кислота
Реакция протекает легко, по продукту реакции до известной степени можно судить о строении гликолей.
Получение сложных эфиров кислот

 О О
О О
СН2 – ОН СН3СООН СН2 – О – С – СН3 СН3СООН СН2 – О – С – СН3
С Н2 – ОН – Н2О СН2ОН – Н2О СН2 – О – С – СН3.
этиленгликоль неполный эфир
О
полный эфир
Дегидратация гликолей. Гликоли, отщепляя воду (в присутствии кислот или хлорида цинка), превращаются в разнообразные соединения, характер которых зависит от строения гликоля, условий реакции. Отнятие воды может протекать внутримолекулярно и межмолекулярно:
а) внутримолекулярная дегидратация:
СН2 - СН2 CH2 – CH2
H2SO4, t1 / \
СН2 СН2 CH2 CH2
– Н2О \ /
О Н
Н О О
Н
Н О О
тетрагидрофуран
б) межмолекулярная дегидратация
O
 /
\
/
\
СН2 –О Н НO – СН2 H2SO4 CH2 CH2
+
+
CH2 – O H HO – CH2 – 2 H2O CH2 CH2
\ /
O
диоксан
Водные растворы этиленгликоля замерзают при температурах ниже нуля (50 %-й при –37 oС), что позволяет применять их для приготовления антифризов – замерзающих при низких температурах жидкостей, используемых для охлаждения двигателей внутреннего сгорания.
Глицерин, 1, 2, 3 -пропантриол
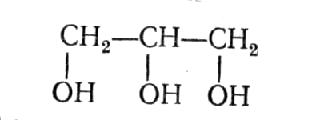 .
.
Глицерин – единственный практически важный представитель трехатомных спиртов – сиропообразная сладкая жидкость, без цвета, хорошо растворимая в воде. Водные растворы глицерина замерзают при низких температурах (67 %- й раствор при –46,5 °С); применяются в качестве антифризов.
Глицерин широко распространен в природе, является основным спиртом, участвующим в построении молекул различных групп липидов. В промышленности глицерин получают гидролизом ацилглицеринов (триглицеридов):
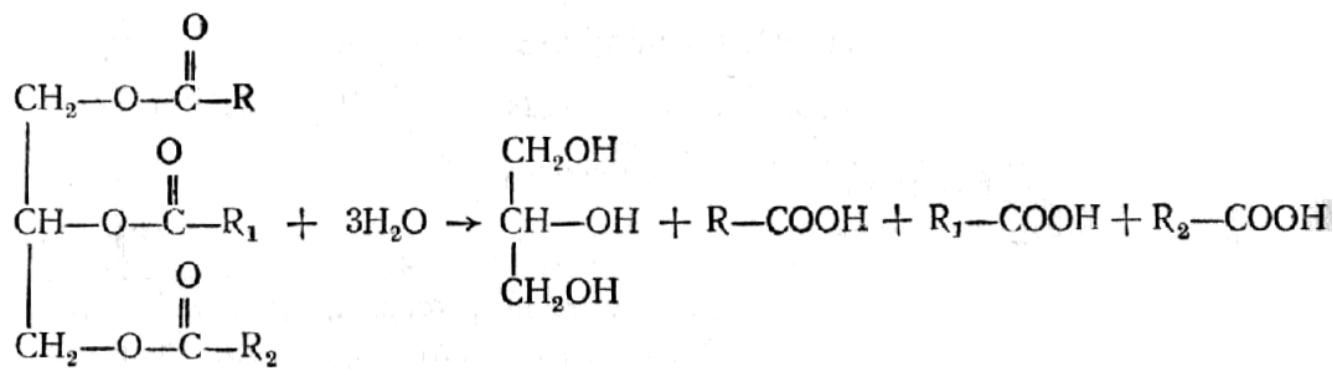
Это – старый способ, не потерявший своего значения и в настоящее время. Однако получение глицерина гидролизом триглицеридов связано с использованием для технических целей больших количеств ценных пищевых продуктов – жиров и масел, поэтому этот способ постепенно заменяется синтетическим, основным сырьем в котором является пропилен:
450–500 oC
СН2 = СН – СН3 + Cl2 CH2 = CH – CH2Cl + HCl;
пропилен аллилхлорид
150–160 oC
СН2 = СН – СН2Cl + NaOH CH2 = CH – CH2OH + NaCl;
аллиловый спирт
CH2Cl – CHOH – CH2OH
СН2 = СН – СН2ОН + HOCl –
CH2OH – CHCl – CH2OH
монохлоргидрины глицерина
CH2Cl – CHOH – CH2OH 150 oC CH2 – CH – CH2
+ 2NaOH .
CH2OH – CHCl – CH2OH – 2NaCl OH OH OH
глицерин
Глицерин широко применяется во многих отраслях промышленности. Основное его количество расходуется для получения производных – глифталевых смол, нитроглицерина. Глифталевые смолы (глифтали) – полиэфиры глицерина и фталевой кислоты – применяются для изготовления лаков. Глицеринтринитрат, или как его называют в технике, «нитроглицерин» – сложный эфир глицерина и азотной кислоты – получают действием азотной кислоты в присутствии серной кислоты на глицерин:
CH2 – OH CH2 – ONO2
H2SO4
CH – OH + 3 HONO2 CH – ONO2 + 3 H2O
CH2 – OH CH2 – ONO2
глицерин глицеринтринитрат (нитроглицерин)
Глицеринтринитрат – взрывчатое вещество огромной силы (взрывается от легкого толчка). Для взрывных работ часто применяется смесь, которая состоит из 75 % нитроглицерина и 25 % инфузорной земли, называемая динамитом, т.к. она безопаснее в работе.
