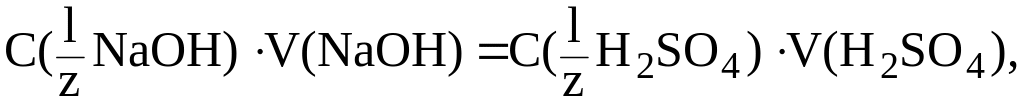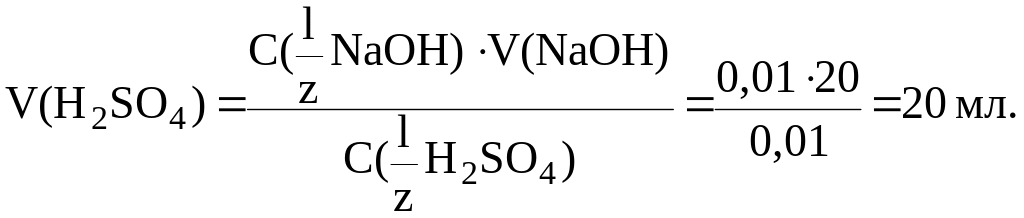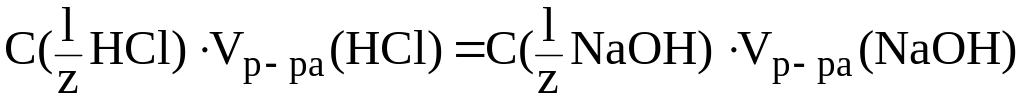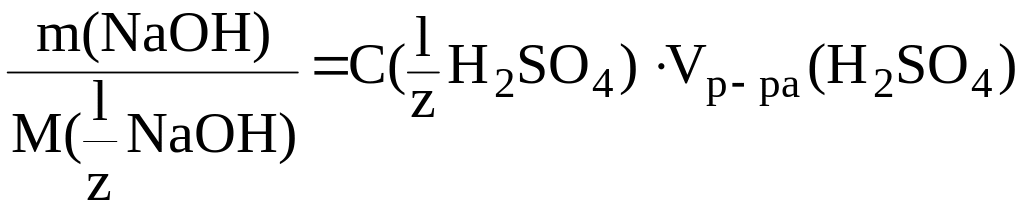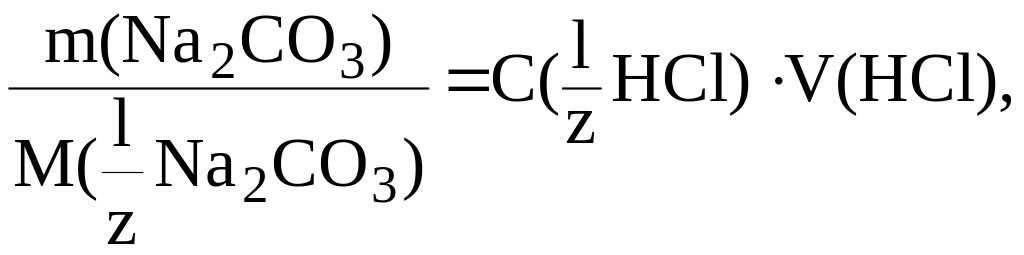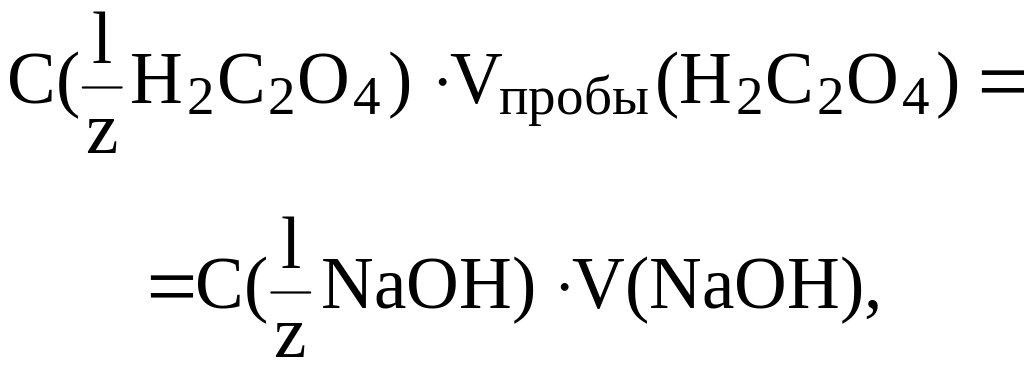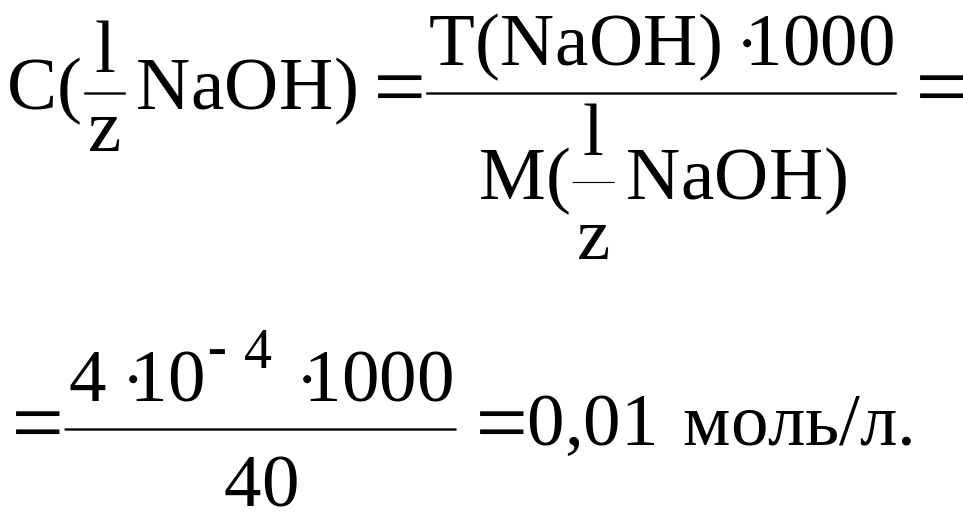- •Теория Электролитической диссоциации
- •Сильные и слабые электролиты
- •1. Теория растворов слабых электролитов.
- •2. Теория растворов сильных электролитов.
- •Кислоты и основания
- •1. Теория Аррениуса.
- •2. Теория Бренстеда и Лоури.
- •3. Теория Льюиса.
- •Эталоны решения задач
- •В зависимости от условий ион hco3– может как отдавать протоны:
- •Таким образом, в первом случае ион hco3 является кислотой, во втором основанием, т. Е. Является амфолитом.
- •Вопросы для самоконтроля
- •Ионное произведение воды. Водородный показатель
- •Шкала значений pH
- •Расчет значений рН и рОн в разбавленных растворах сильных и слабых кислот и оснований
- •Кислотно-основное равновесие биологических жидкостей
- •Эталоны решения задач
- •Вопросы для самоконтроля
- •Вариант №8
- •Вариант №9
- •Вариант №10
- •Вариант №15
- •Вариант №16
- •Вариант №17
- •Вариант №18
- •Вариант №19
- •Вариант №20
- •Гидролиз
- •Гидролиз солей
- •Количественные характеристики гидролиза
- •Усиление и подавление гидролиза
- •Значения рН растворов гидролизующихся солей
- •2. В растворах солей типа ch3cooNa:
- •3. В растворах солей типа nh4cn:
- •Эталоны решения задач
- •Вопросы для самоконтроля
- •Варианты задач для самостоятельного решения Вариант №1
- •Вариант №2
- •Вариант №3
- •Вариант №4
- •Вариант №5
- •Вариант №6
- •Вариант №7
- •Вариант №8
- •Вариант №9
- •Вариант №10
- •Вариант №11
- •Вариант №12
- •Вариант №13
- •Вариант №14
- •Вариант №15
- •Вариант №16
- •Вариант №17
- •Вариант №18
- •Вариант №19
- •Вариант №20
- •Элементы количественного анализа
- •Объемный (титриметрический) метод анализа
- •Расчеты в объемных методах анализа Закон эквивалентов
- •Методы кислотно-основного титрования
- •Титранты и их стандартизация
- •Фиксирование точки эквивалентности
- •Механизм действия индикаторов
- •Точка перехода и интервал перехода окраски индикатора
- •Правила выбора индикатора
- •1. Титрование сильной кислоты сильным основанием.
- •3. Титрование слабого основания сильной кислотой.
- •Степень окисления. Окисление и восстановление
- •Окислители и восстановители
- •Последовательность подбора коэффициентов в уравнениях окислительно-восстановительных реакций (метод электронно-ионного баланса)
- •Оксидиметрия
- •Перманганатометрия
- •Иодометрия
- •Расчет эквивалентов окислителей и восстановителей
- •Эталоны решения задач
- •Метод нейтрализации
- •Метод оксидиметрии
- •Вопросы для самоконтроля
- •Варианты задач для самостоятельного решения Вариант №1
- •Вариант №2
- •Вариант №3
- •Вариант №4
- •Вариант №5
- •Вариант №6
- •Вариант №7
- •Вариант №8
- •Вариант №9
- •Вариант №10
- •Вариант №11
- •Вариант №12
- •Вариант №13
- •Вариант №14
- •Вариант №15
- •Вариант №16
- •Вариант №17
- •Вариант №18
- •Вариант №19
- •Вариант №20
Метод нейтрализации
7. На титрование 20 мл раствора HCl с C( HCl) 0,1 моль/л затрачено 10 мл раствора NaOH. Вычислить C( NaOH) в растворе.
Дано: V(HCl) 20 мл C( HCl) 0,1 моль/л
|
Решение. Согласно закону эквивалентов (формула 3):
следовательно:
|
C( NaOH) ? |
8. На титрование раствора CH3COOH израсходовано 15,2 мл раствора NaOH c C( NaOH) 0,05 моль/л. Вычислить массу CH3COOH в растворе.
Д ано:
ано:
(NaOH) = 15,2 мл = 0,0152 л
C(![]() NaOH)
= 0,05 моль/л
NaOH)
= 0,05 моль/л
m (CH3COOH)
?
(CH3COOH)
?
Решение.
Согласно закону эквивалентов (4):
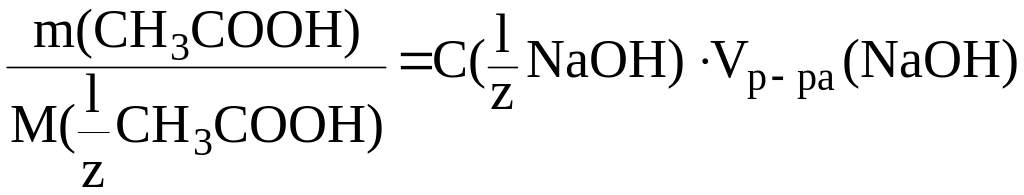
следовательно:
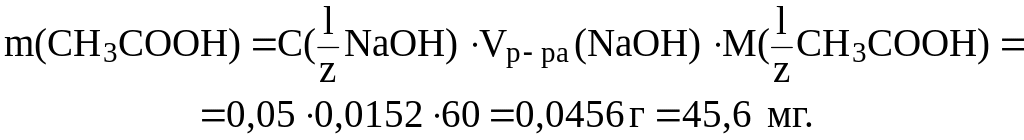
9. Рассчитать, какой объем раствора H2SO4 c молярной концентрацией эквивалента 0,2 моль/л потребуется для нейт-рализации раствора, содержащего 0,4 г NaOH.
Дано: m(NaOH) = 0,4 г C( H2SO4) = 0,2 моль/л |
Решение.
|
|
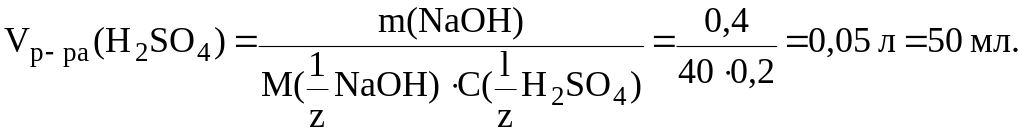
10. Имеется
раствор Na2CO3
объемом 200 мл. На титрование 10 мл этого
раствора было израсходовано 15,3 мл
раствора HCl
с C(![]() HCl)
0,1 моль/л. Найти массу соды в исходном
растворе.
HCl)
0,1 моль/л. Найти массу соды в исходном
растворе.
Дано: V0(Na2CO3) 200 мл Vпробы(Na2CO3) 10 мл (HCl) 15,3 мл C( |
|
m(Na2CO3) ? |
Решение.
По результатам титрования найдем C( Na2CO3):
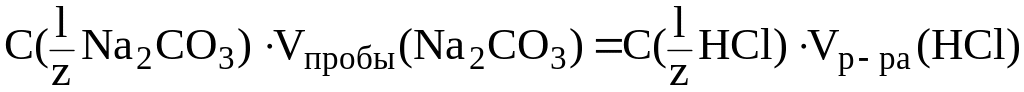 ,
,
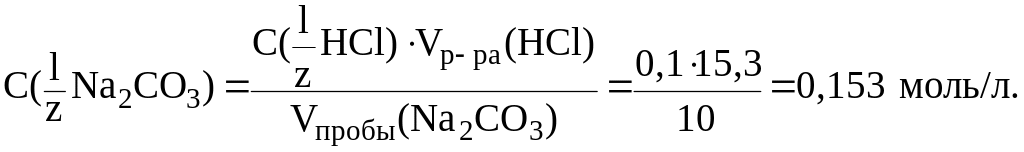
Рассчитаем Т(Na2CO3):
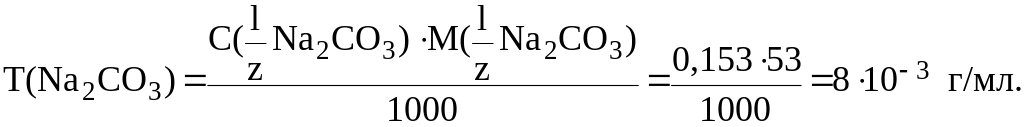
Найдем m(Na2CO3) во всем объеме раствора:
![]()
11. Вычислить массовую долю (Na2CO3) в техническом образце, если на титрование навески технической соды массой 0,212 г было израсходовано 20 мл раствора HCl с C( HCl) 0,1 моль/л.
Дано: mобр. 0,212 г (HCl) 20 мл 0,02 л C( HCl) 0,1 моль/л |
Решение. Найдем массу чистого Na2CO3:
|
(Na2CO3) ? |
![]()
Рассчитаем (Na2CO3):
![]()
12. Из 0,126 г технической щавелевой кислоты (Н2С2О42Н2О) приготовили 200 мл раствора. На титрование 10 мл полученного раст-вора израсходовали 8 мл раствора NaOH с C( NaOH) 0,01 моль/л. Найти массовую долю (Н2С2О42Н2О) в техническом образце.
Дано: mобр. 0,126 г V0(Н2С2О4) 200 мл Vпробы(Н2С2О4) 10 мл C( NaOH) 0,01 моль/л (NaOH) = 8 мл |
Решение. По результатам титрования найдем С( Н2С2О4):
|
(Н2С2О42Н2О) ? |
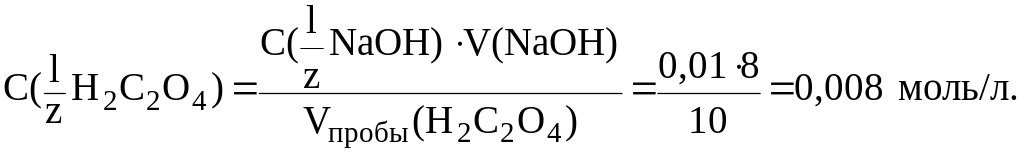
Рассчитаем Т(Н2С2О4):
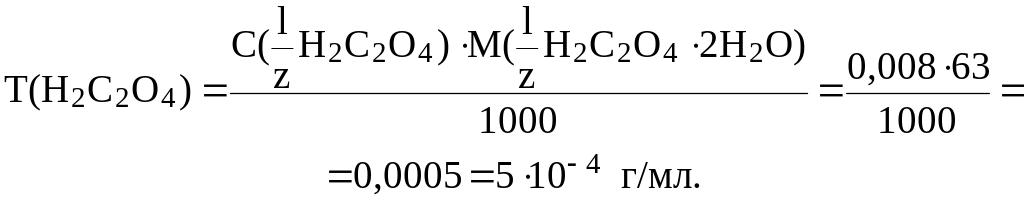
Вычислим массу чистого Н2С2О42Н2О в образце:
![]()
Рассчитаем (Н2С2О42Н2О) в техническом образце:
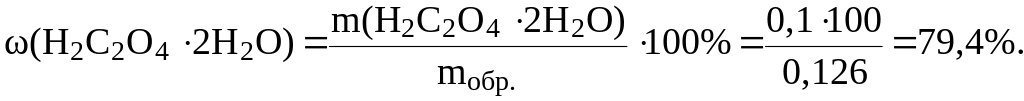
13. Рассчитать, какой объем раствора H2SO4 с молярной концентрацией эквивалента 0,01 моль/л необходимо затратить, чтобы оттитровать 20 мл раствора NaOH с T(NaOH) = 0,0004 г/мл.
Дано: С( H2SO4) = 0,01 моль/л (NaOH) = 20 мл T(NaOH) = 4104 г/мл |
Решение. Рассчитаем С( NaOH):
|
(H2SO4) ? |
Найдем V(H2SO4):