
Лекція4,5
.pdfПоняття про допоміжні речовини: загальні вимоги до них
Виробництво сучасних ліків передбачає використання різноманітних допоміжних речовин (розчинників, пролонгаторів, стабілізаторів, консервантів, розпушувачів, пластифікаторів, барвників тощо).
Допоміжні речовини є обов’язковими компонентами практично всіх лікарських форм, складають єдину фізико-хімічну систему з лікарськими речовинами й контактують з організмом разом з останніми. Вони регулюють швидкість досягнення терапевтичного ефекту діючої речовини, а також забезпечують зручність застосування й споживчі якості ліків (смак, колір, запах, зовнішній вигляд, стабільність при зберіганні, рівень мікробної контамінації).
Використання у фармацевтичній технології різноманітних допоміжних речовин, що володіють різним спектром властивостей, дозволяє значно спростити технологію багатьох ліків, механізувати процеси виробництва, поліпшити властивості ліків. Крім того, з’являється реальна можливість створення ряду нових, більш ефективних лікарських форм: емульсій і суспензій для ін’єкцій, різних препаратів пролонгованої дії, таблеток, драже й капсул з вологонепроникними плівковими покриттями, очних і стоматологічних лікарських плівок, желатинових капсул і мікрокапсул, водорозчинних суппозиторіїв, ліків в аерозольній упаковці, капсул для ректального й вагінального введення, трансдермальних препаратів, ліпосомальних лікарських форм тощо.
До сучасних допоміжних речовин пред’являються наступні вимоги:
не мати токсичну й алергенну дію;
забезпечувати прояв необхідної фармакологічної дії лікарської речовини
зурахуванням її фармакокінетики;
не взаємодіяти з активною субстанцією, а також з тароукупорювальними матеріалами й технологічним обладнанням;
бути технологічними;
не впливати на органолептичні властивості ліків (смак, запах, колір тощо);
мати хімічну й мікробіологічну чистоту (не перевищуючи норм встановлених для певних ліків);
бути стабільними, економічно доступними, по можливості вироблятися вітчизняною промисловістю.
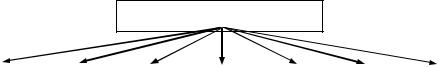
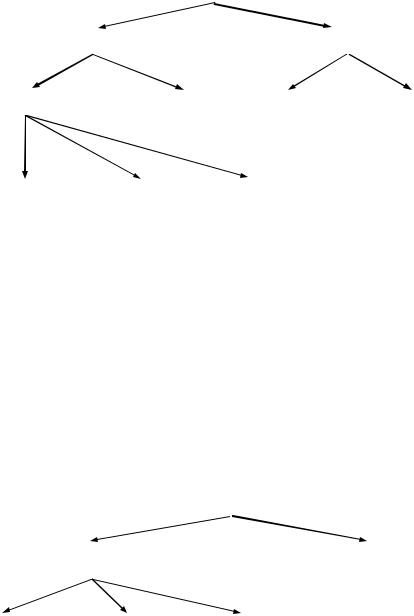
Допоміжні речовини класифікують за впливом на технологічні характеристики й фармакокінетику ліків (Рис. 1) або за природою речовин і за їх хімічною структурою (Рис. 2). Вказані класифікації умовні, оскільки в багатьох випадках допоміжні речовини можуть використовуватися в кількох напрямках.
Розглянемо окремі групи допоміжних речовин:
Допоміжні речовини
Розчинники |
|
Консерванти |
|
Пролонгатори |
|
Стабілізатори |
|
Солюбілізатори |
|
Коригенти |
|
Барвники |
|
|
|
|
|
|
|
|
|
|
|
|
|
Рис.1. Класифікація допоміжних речовин за їх впливом на технологічні характеристики та фармакокінетику ліків
За своєю природою допоміжні речовини можна розділити на природні, синтетичні й напівсинтетичні. Природні допоміжні речовини доцільно підрозділити на сполуки органічні й неорганічні.
Допоміжні речовини природного походження одержують шляхом перероблення рослинної й тваринної сировини, сировини мікробного походження й мінералів. Природні допоміжні речовини мають перевагу в порівнянні із синтетичними завдяки високій біологічній нешкідливості. Тому пошук природних допоміжних речовин, очевидно, буде тривати й надалі. У цей час із використовуваних допоміжних речовин приблизно 1/3 припадає на природні. Рослинні біополімери використовують як емульгатори, стабілізатори, пролонгатори та для інших цілей у виробництві лікарських форм.
Природні допоміжні речовини мають суттєвий недолік – вони піддаються високій мікробної контамінації, у зв’язку з чим розчини полісахаридів і білків швидко псуються. Крім того, у складі мікрофлори неорганічних сполук можуть виявлятися не тільки умовно-патогенні, але й патогенні мікроорганізми. У цьому випадку використання прийнятних методів стерилізації й додавання антимікробних речовин (консервантів) значною мірою може знизити до гранично припустимих норм мікробну контамінацію природних допоміжних речовин.
Синтетичні й напівсинтетичні допоміжні речовини знаходять широке застосування в технології лікарських форм. Цьому сприяє їхня доступність – можливість синтезу речовин із заданими властивостями, більш ефективних і менш токсичних. При одержанні напівсинтетичних допоміжних речовин є можливість удосконалювання властивостей природних речовин. Наприклад, похідні метилцелюлози: натрієва сіль метилцелюлози розчинна у воді, а оксіпропілцелюлоза нерозчинна, тому вона використовується для покриття оболонками таблеток і драже з метою захисту лікарських речовин від кислого середовища шлункового соку. Похідні ланоліну (ацетильовані, оксиетильовані тощо) на відміну від ланоліну, за складом тотожні шкірному
жиру людини, не викликають алергічних реакцій і через меншу в’язкість, у порівнянні з ланоліном, зручніші при виготовленні мазей.
|
|
|
|
|
Допоміжні речовин |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
За природою |
|
|
|
За хімічною структурою |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
Природні |
|
Синтетичні, |
|
|
ВМС |
|
ПАР |
||||
|
|
|
напівсинтетичні |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
Полісахариди |
|
Білки |
|
Неорганічні |
|
|
|
|
|
|
|
|
|
|
Рис. 2. Класифікація допоміжних речовин за природою та хімічною структурою сполук
Необхідно також враховувати, що синтетичні й напівсинтетичні допоміжні речовини можуть замінити ряд харчових продуктів. Широке використання синтетичних і напівсинтетичних допоміжних речовин висвітлене в технології кожної лікарської форми.
За хімічною структурою допоміжні речовини є високомолекулярними сполуками (ВМС), що утворюють розчини різної в’язкості залежно від концентрації. З цією властивістю пов’язане й основне їх використання в різних лікарських формах: рідких, в’язкопластичних і твердих, тобто в розчинах, мазях, таблетках тощо.
|
|
|
|
|
|
|
ВМС |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Органічні |
|
|
|
|
|
|
Синтетичні |
|
|
|
(безводні) |
|
|
|
|
|
|
(напівсинтетичні) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Целюлоза |
|
|
|
|
|
|
|
|
|
|
МЦ |
Неорганічні |
|
|
Полісахариди |
|
|
Білки |
|
|||
|
|
|
|
|
|
Натрій-МЦ |
||||
|
|
|
|
|
|
|
|
|
|
Етилцелюлоза |
Аеросил |
|
|
Крохмаль |
|
|
Желатин |
|
|||
|
|
|
|
|
Оксипропілцелюлоза |
|||||
Бентоніт |
|
|
Камеді |
|
|
Желатоза |
|
|||
|
|
|
|
|
Етилметилцелюлоза |
|||||
|
|
|
Альгінати |
|
|
Колаген |
|
|||
|
|
|
|
|
|
Поліакриламід |
||||
|
|
|
Мікробні |
|
|
|
|
|
||
полісахариди |
Карбопол |
|
Пропіленгліколь |
||
Декстрин |
||
Полівініловий спирт |
||
Пектин |
||
Силікони |
||
|
||
|
Полівінілпіролідон |
|
|
Поліетиленоксид |
Рис. 3. Класифікація високомолекулярних сполук
До ВМС належать природні й синтетичні речовини, що мають молекулярну масу не менше 10 000 (Рис.3). Їх молекули (макромолекули)
являють собою довгі нитки, що переплітаються між собою або закручені в клубки. Від будови молекул часто залежить специфіка виготовлення розчинів (в основному ВМС у технології лікарських форм використовуються у вигляді розчинів).
Властивості ВМС і їх розчинів розглядаються в курсах органічної, фізичної й колоїдної хімії. При використанні ВМС у технології лікарських форм необхідно базуватися на раніше отриманих знаннях.
ВМС використовуються в технології практично всіх лікарських форм: як основи для мазей, суппозиторіїв, пігулок тощо; як стабілізатори; як пролонгатори; як коригенти смаку; крім того як пакувальні й укупорювальні матеріали. Введення в технологію нових ВМС дозволило створити нові лікарські форми: багатошарові таблетки тривалої дії; спансули (гранули, просочені розчинами ВМС); мікрокапсули; очні лікарські плівки; дитячі лікарські форми тощо.
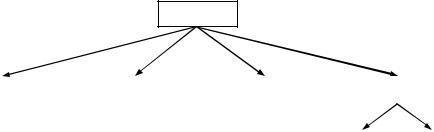
Широке застосування ВМС у технології лікарських форм засноване також і на їх поверхнево-активних властивостях. Залежно від хімічної структури розрізняють 3 типи поверхнево-активних речовин (ПАР): катіонні, аніонні, неіоногенні (Рис.4). Всі типи ПАР, в тій або іншій мірі, використовуються у фармацевтичній технології як гідрофілізатори, солюбілізатори, емульгатори, стабілізатори тощо. Це обумовлено властивістю їх молекул: дифільністю, певною величиною гідрофільноліпофільного балансу (ГЛБ) і поверхневою активністю.
Однак найбільше застосування останнім часом знаходять неіоногенні ПАР (НПАР), насамперед як сполуки, що мають найменшу токсичністю й не подразнюють слизові оболонки й тканини, а також мають ряд інших переваг. Групу НПАР становлять оксиетильні похідні ряду органічних сполук, моноефіри сахарози, гліцериди високомолекулярних жирних кислот, ефіри жирних кислот і багатоатомних спиртів і їх оксиетильні похідні, що одержали назву спенів тощо.
Серед різних груп ПАР катіоноактивні ПАР – найсильніші бактерицидні засоби. Завдяки сполученню поверхнево-активних і бактерицидних властивостей вони перспективні для застосування у фармацевтичній технології. Це солі моночетвертинних амонієвих сполук (етонію хлорид, тіонію хлорид).
Погіршення бактеріостатичних властивостей катіонних ПАР при додаванні до них неіоногенних ПАР, очевидно, пов’язане з їх спільним міцелоутворенням. Включення в лікарські форми представників цих 2 класів ПАР одночасно нераціонально, оскільки вимагає підвищення концентрації четвертинних амонієвих сполук, що буде призводити до збільшення токсичних властивостей готових лікарських препаратів.
ПАР
Аніоноактивні |
|
Катіоноактивні |
|
Неіоногенні |
|
|
Амфотерні |
||
|
|
|
|
|
|
|
|
|
|
солі вищих жирних |
|
четвертинні амонієві |
вищі жирні спирти і |
|
|
|
|
||
|
та піридинові |
|
кислоти, складні |
|
|
|
|
||
кислот, солі |
|
|
|
|
|
|
|||
|
|
|
Білки |
|
Ліпіди |
||||
сполуки (бензалконій |
|
ефіри гліколів та |
|
|
|||||
сульфоефірів |
|
|
|
||||||
|
хлорид, |
|
жирних кислот |
|
|
|
|
||
вищих жирних |
|
|
|
|
|
|
|||
|
|
|
желатин |
лецетин |
|||||
|
цетилпіридиновий |
|
(жиросахара, твіни, |
|
|||||
спиртів (натрію |
|
|
желатоза |
бетаїн |
|||||
|
хлорид, етоній) |
пентол, емульгатори, |
|||||||
лаурилсульфат) |
|
|
казеїн |
кефалін |
|||||
|
|
|
спирти синтетичні |
|
|||||
|
|
|
|
сухе молоко |
стерини |
||||
|
|
|
|
жирні первинні |
|||||
|
|
|
|
|
|
|
|
||
фракції С16-С21)
Рис. 4. Класифікація поверхнево-активних речовин
Під дією ПАР (в силу дифільної будови молекул) різко змінюються молекулярні властивості тієї поверхні, на якій вони адсорбуються. Позитивна адсорбція молекул призводить до зниження поверхневого або міжфазного поверхневого натягу. З адсорбційною здатністю ПАР пов’язані їх технологічні властивості. У розведених розчинах молекули ПАР піддаються максимальній гідратації, що сприяє утворенню істинного розчину. З підвищенням ГЛБ покращуються гідрофільні властивості ПАР, що супроводжується зростанням їхньої розчинності у воді. Неполярні групи молекул ПАР при підвищенні критичної концентрації міцелоутворення (ККМ) дегідратуються, з’єднуються одна з одною під дією міжмолекулярного притягання й утворюють міцели. Збільшення довжини аліфатичного ланцюга сприяє міцелоутворенню (із цим пов’язана солюбілізація олеофільних сполук). Сильно розведені розчини неіоногених ПАР подібні до звичайних електролітів. Однак при підвищенні концентрації до ККМ різко змінюються багато їхніх фізико-хімічних властивостей: електропровідність, осмотичний тиск, поверхневий натяг, солюбілізувальна дія, в’язкість тощо.
Біофармацевтичні дослідження показали, що ПАР, змінюючи фізикохімічні властивості лікарських форм, можуть помітно впливати на терапевтичну ефективність лікарських препаратів. Низькі концентрації ПАР збільшують всмоктування сульфаніламідів, барбітуратів, деяких ефірів кислоти саліцилової, гідрокортизону, і, навпаки, високі концентрації багатьох ПАР знижують резорбцію лікарських речовин з розчинів. Залежність, що спостерігається, пояснюють зміною під дією ПАР проникності клітинних мембран і підвищенням розчинності лікарських речовин, міцелоутворенням, зниженням поверхневого натягу й коефіцієнту розподілу на границі розподілу фаз.
Таким чином, використання ПАР у фармацевтичній технології дозволяє розробляти лікарські форми з необхідними фізико-хімічними властивостями, підвищувати агрегативну стійкість різних дисперсних систем і запобігати
розкладанню лікарських речовин, регулювати процеси їхнього вивільнення, розподілу й всмоктування при різних шляхах введення.
Класифікація допоміжних речовин за природою й хімічною структурою доцільна для знання й подальшого використання їх фізичних, фізикохімічних і фізико-механічних властивостей.
Розвиток синтетичної хімії, особливо хімії полімерів, в останні десятиліття створив можливість для спрямованого пошуку нових допоміжних речовин. До них належать метилцелюлоза і її похідні, поліетиленгліколі, полівінілпіролідон, поліакриламід, силікони, різноманітні емульгатори тощо.
Природні допоміжні речовини
Крохмаль (Amylum) складають полісахариди (97,3 – 98,9%), білкові речовини (0,28 – 1,5%), клітковина (0,2 – 0,69 %), мінеральні речовини (0,3 – 0,62 %). Крохмаль складається з 2 фракцій – амілози й амілопектину. Молекула амілози являє собою довгий ланцюг, що складається із глікозидних залишків (до 700). Амілопектин має більш складну будову й складається з розгалужених молекул, що містять до 2000 залишків D-глюкопіранози. Чим коротший ланцюг, тим краще фракція розчиняється у воді. Так, амілоза розчиняється в теплій воді, а амілопектин тільки набухає. Клейстерізація виражається в сильному набуханні крохмальних зерен, їхньому розриві й утворенні в’язкого гідрозолю.
Крохмаль використовують у твердих лікарських формах, у тому числі пігулках (у суміші із глюкозою й цукром), мазях. Як стабілізатор суспензій і емульсій застосовують 10% розчин.
Альгінати (Alginata) використовуються як допоміжні речовини. Особливе значення серед них набувають кислота альгінова та її солі. Кислота альгінова – ВМС, яку одержують з морських водоростей (ламінарій). Вона завдяки своїм фізико-хімічним властивостям здатна утворювати в’язкі водні розчини й пасти, володіє гомогенізувальними, розпушувальними, стабілізувальними властивостями тощо. Це послужило підставою для широкого використання альгінатів у складі різних фармацевтичних препаратів як розпушувачів, емульгаторів, пролонгаторів, плівкоутворювальних допоміжних речовин, а також для виготовлення мазей і паст.
Кислота альгінова і її натрієва сіль практично нешкідливі. Вони є найбільш перспективними допоміжними речовинами, особливо для виробництва готових лікарських засобів.
Агароїд (Agaroidum) являє собою ВМС різного ступеня полімеризації з малою реакційною здатністю. До складу полімеру входять глюкоза й галактоза, а також мінеральні елементи (кальцій, магній, сірка тощо). Агароїд, що отримують з водоростей в концентрації 0,1% має стабілізувальну, розпушувальну і ковзну дію. В суміші із гліцерином в концентрації 1,5% може також бути використаний як основа для мазей. Агароїд має й коригувальні властивості.
Пектин (Pectinum) і пектинові речовини входять до складу клітинних стінок багатьох рослин. Це ВМС – за структурою полігалактуронова кислота, частково етерифікована метанолом. Характерною властивістю розчинів пектину є висока желатинізуювальна здатність. Пектин використовують для створення дитячих лікарських форм.
Мікробні полісахариди (Polysaccharida microbica) є важливим класом природних полімерів, що володіють різноманітними властивостями (пролонгувальні, стабілізувальні гетерогенні системи тощо), завдяки яким вони можуть застосовуватися як основи для мазей, лініментів. Із групи цих речовин найбільшого поширення одержав аубазідан – позаклітинний полісахарид, що одержують при мікробіологічному синтезі з дріжджового гриба Aureobasidium pullulans. Завдяки своїй будові, розгалуженій структурі, конфігурації й конформації моносахаридів у молекулі полімеру (М.М. 6 – 9 млн) він добре розчинний у воді, дає в’язкі розчини, пластичні гелі. Аубазідан (0,6% і вище) утворює гелі, які можуть використовуватися як основи для мазей, 1% – для плівок і губок. У концентрації 0,1 – 0,3% аубазідан використовується як пролонгатор очних крапель. У цьому випадку позитивним моментом є стійкість розчинів при термічній стерилізації до 120°С. Аубазідан також є ефективним стабілізатором і емульгатором.
Колаген (Coilagenum) є основним білком сполучної тканини, складається з макромолекул, що мають трьохспіральну структуру. Головним джерелом колагену слугує шкіра великої рогатої худоби, у якій міститься його до 95%. Колаген одержують шляхом лужно-сольового оброблення.
Колаген застосовують для покриття ран у вигляді плівок з фурациліном, борною кислотою, метилурацилом і також у вигляді очних плівок з антибіотиками. Застосовуються губки гемостатичні та з різними лікарськими речовинами. Колаген забезпечує оптимальну активність лікарських речовин, що пов’язана з глибоким проникненням і тривалим контактом із тканинами організму лікарських речовин, включених у колагенову основу.
Сукупність біологічних властивостей колагену (відсутність токсичності, повна резорбція й утилізація в організмі, стимуляція репаративних процесів) та його технологічні властивості створюють можливість широкого використання його в технології лікарських форм.
Желатин (Gelatina) одержують при випарюванні обрізків шкіри. Основною амінокислотою сумішшю желатину є глікокол (25,5%), міститься багато аланіну (8,7%), аргініну (8,2%), лейцину (7,1%), лізину (5,9%) і глютамінової кислоти. Желатин – ВМС білкової природи. Він є активним емульгатором і стабілізатором, але через гелеутворювальні властивості досить рідко застосовується в аптечній практиці. Емульсії виходять густими, щільними, вони швидко піддаються мікробної контамінації. Желатин завдяки високим гелеутворювальним властивостям використовують для виготовлення мазей, суппозиторіїв, желатинових капсул і інших лікарських форм.
Желатоза (Gelatosa) являє собою продукт неповного гідролізу желатину. Не має властивості желатинізуватися, але має високі
емульгувальні властивості. Негативною властивістю є нестандартність речовини, тому в ряді випадків розчини желатози можуть мати високу в’язкість і пружністю.
З неорганічних полімерів найчастіше використовуються бентоніт, аеросил, тальк.
Бентоніт (Bentonitum) – природний неорганічний полімер. Зустрічається у вигляді мінералів кристалічної структури з розмірами часток менш 0,01 мм. Має складну будову і складається в основному з алюмогідросилікатів із загальною формулою:
Al2O3∙SiO2∙mH2O
У складі глинистих мінералів міститься 90% оксидів алюмінію, кремнію, магнію, заліза й води. Катіонами є К+, Na+, Ca2+, Mg2+, тому глинисті мінерали можуть вступати в іонообмінні реакції. Це дозволяє регулювати їх фізико-хімічні властивості й одержувати системи із заданими властивостями, так звані модифіковані бентоніти. Бентоніти активно взаємодіють із водою. Внаслідок утворення гідратної оболонки частки глинистих мінералів здатні міцно утримувати воду й набрякати в ній, значно збільшуючись в об’ємі. Найкраще набрякають натрієві солі бентонітів (об’єм збільшується у 17 разів), кальцієві солі бентонітів збільшуються в об’ємі тільки в 2,5 рази. Ще більше збільшуються в об’ємі напівсинтетичні бентоніти – триетаноламінобентоніти (у 20 – 22 рази). Бентоніти біологічно нешкідливі.
Індиферентність бентонітів до лікарських речовин, здатність до набрякання й гелеутворення дозволяють використовувати їх при виробництві багатьох лікарських форм: мазей, таблеток, порошків для внутрішнього й зовнішнього застосування, пігулок, гранул. Зі здатністю бентонітів підвищувати в’язкість (особливо натрієвих форм) пов’язана можливість використовувати їх у концентрації 3 – 5% для стабілізації суспензій. Бентоніти, особливо триетаноламінові форми, мають і емульгуювальні властивості.
Бентоніти надають лікарським препаратам м’якість, дисперсність, високі адсорбційні властивості, легку віддачу лікарських речовин і стабільність.
Аеросил (Aerosilum), як і бентоніти, належить до неорганічних полімерів. Аеросил – колоїдний діоксид Si – білий, дуже легкий, високодисперсний з великою питомою поверхнею порошок, що має виразні адсорбційні властивості. У воді аеросил у концентрації 1 – 4% утворює драглеподібні системи із гліцерином, олією вазеліновою.
Аеросил широко застосовують для стабілізації суспензій з різним дисперсійним середовищем. Це сприяє кращій фіксації суспензій на шкірі, підсилюючи терапевтичний ефект. Згущувальну здатність аеросилу використовують при одержанні гелів для мазевих основ. У порошках застосовують при виготовленні гігроскопічних сумішей і як диспергатор. Адсорбційні властивості використовують із метою стабілізації сухих екстрактів (зменшується їх гігроскопічність). Додавання аеросилу до таблеток значно підвищує їх стійкість до висихання в процесі зберігання. Він підсилює в’язкість супозиторної маси, надає їй гомогенний характер,
забезпечує рівномірний розподіл лікарських речовин, дозволяє вводити рідкі й гігроскопічні речовини.
Тальк (Talcum) – природний магнієвий силікат – кисла кремнемагнієва сіль Mg3H2(Si03)4 з домішками силікатів алюмінію та інших речовин. Одержують порошкуванням природного матеріалу. Тальк білий (іноді зеленуватий), жирний на дотик порошок, нерозчинний у воді, органічних розчинниках, розбавлених мінеральних кислотах. Має мінімальну твердість (1 – 2 бали) за шкалою Мооса. Для медичних потреб тальк має бути звільнений від солей заліза та розчинних у воді або спирті домішок, порошок тальк має бути найдрібнішим (сито М/50). В побуті використовується для запобігання тертя різних поверхонь (в резинових рукавичках, у взутті), а також для попередження злипання пластмасових виробів при довготривалому зберіганні. Широко використовується як адсорбційна присипка, відрізняється від органічних присипок (крохмаль, лікоподій) своєю стійкістю, нездатністю слугувати середовищем для розвитку мікроорганізмів та дешевизною. До складу таблеток входить як антифрикційна речовина, що запобігає злипанню та покращує ковзні властивості маси для таблетування. В харчовій промисловості зареєстрований в якості харчової добавки E553b.
Синтетичні й напівсинтетичні допоміжні речовини
Особливе місце серед ВМС, що використовуються у технології лікарських форм, займають ефіри целюлози. Фізіологічна нешкідливість, цінні фізико-хімічні й технологічні властивості цих допоміжних матеріалів дозволяють застосовувати їх як стабілізувальні, пролонгувальні, формоутворювальні засоби, а також для надання відповідної якості багатьох лікарських форм.
У технології лікарських форм використовують прості й складні ефіри целюлози. Вони є продуктами заміщення водневих атомів гідроксильних груп целюлози на спиртові залишки – алкіди (при одержанні простих ефірів) або кислотні залишки – ацили (при одержанні складних ефірів).
Загальна формула целюлози виглядає так:
[С6Н7О2(ОН)3-х(OR)x)]n
де х – число заміщених ОН-груп в одній ланці; n – число полімеризації.
Метилцелюлозу розчинну (Меthylcellulosum solubile) краще використовувати в технологічній практиці. Відносна М. М. метилцелюлози (МЦ) складає 150 – 300 тис. МЦ розчинна являє собою простий ефір целюлози й метанолу. Може мати вигляд трохи жовтуватого порошку, гранульованого або волокнистого продукту без запаху й смаку. МЦ розчинна в холодній воді, гліцерині, нерозчинна в гарячій воді. Для виготовлення водних розчинів МЦ заливають водою, що нагріта до температури 80 – 90°С, у кількості 1/2 від необхідного об’єму одержуваного розчину. Після зниження температури до кімнатної додають холодну воду. Охолоджені розчини прозорі. При нагріванні до температури вище 50°С водні розчини МЦ коагулюють, але при охолодженні гель знову переходить у розчин. Розчини мають виразні поверхнево-активні властивості. Концентровані
розчини МЦ псевдопластичні. При висиханні розчини утворюють прозору міцну плівку.
Водні розчини МЦ мають високу сорбційну, емульгувальну і змочувальну здатність. У технології застосовують 0,5 – 1% водні розчини як згущувачі і стабілізатори, для гідрофілізації гідрофобних основ мазей і лініментів, як емульгатори й стабілізатори при виготовленні суспензій і емульсій, а також як пролонгатори для очних крапель. Водні розчини (3 – 8%-ві), іноді з додаванням гліцерину, утворюють гліцерогелі, які застосовують як основу для мазей, що не висихають.
Натрій-карбоксіметилцелюлоза (Methylceilulosum-natrium) є іншим похідним метилцелюлози. Це натрієва сіль простого ефіру целюлози й гліколевої кислоти (Na-КМЦ):
[С6Н7О2(ОН)3-х(OCH2COONa)x)]n
де х – число заміщених ОН-груп в одній ланці; n – число полімеризації. Na-КМЦ (М.М. 75 – 85 тис) має вигляд білого або трохи жовтуватого
порошку, або волокнистого продукту без запаху, розчинного в холодній і гарячій воді. Натрій-КМЦ у різних концентраціях (0,5 – 2%) застосовують як пролонгатори дії лікарських речовин в очних краплях і ін’єкційних розчинах, стабілізатори, формоутворювальні речовини в емульсіях і мазях (4 – 6%). Гелі натрій-КМЦ на відміну від гелів МЦ сумісні з багатьма консервантами.
Крім МЦ і натрій-КМЦ у технології готових лікарських засобів використовують оксіпропілметилцелюлозу й ацетилцелюлозу.
Полівінол (Polyvinolum) – найпоширеніший синтетичний водорозчинний полімер вінілацетату. Полівінол (полівініловий спирт – ПВС) належить до синтетичних полімерів аліфатичного ряду, що містить гідроксильні групи.
ПВС являє собою порошок білого або трохи жовтуватого кольору, розчинний у воді при нагріванні. Має високу реакційну здатність завдяки наявності гідроксильних груп.
За молекулярною масою ПВС поділяються на чотири групи: олігомери (4 – 10 тис); низькомолекулярні (10 – 45 тис); середньомолекулярні (45 – 150 тис); високомолекулярні (150 – 500 тис).
У технології лікарських форм 1,4 – 2,5% розчини ПВС застосовують як емульгатори, згущувачі й стабілізатори суспензій; 10% розчин – для мазевих основ і очних плівок.
Полівінілпірролідон (Polyvinyl pyrrolidonum) – полімер N-
вінілпірролідону. Полівінілпірролідон (ПВП) одержують при полімеризації мономера – вінілпірролідона.
ПВП – безбарвний і прозорий гігроскопічний полімер (М.М. 10 – 100 тис). Найбільшого поширення у технології лікарських форм набув ПВП, що має молекулярну масу 12,6 – 35 тис. Він розчинний у воді, спиртах, гліцерині, легко утворює комплекси з лікарськими сполуками (вітамінами, антибіотиками).
ПВП використовується в медицині й фармацевтичній технології як стабілізатор емульсій і суспензій, як пролонгатор, наповнювач для таблеток і драже. Він також входить до складу плазмозамінників крові, аерозолів, очних
