
Лекція4,5
.pdfлікарських плівок. Гелі на основі ПВП використовують для виготовлення мазей, у тому числі призначених для нанесення на слизові оболонки.
Поліакриламід (Polyacrilamidum). В останні роки набули дуже широкого поширення поліакриламід (ПАА) і його похідні.
ПАА – полімер білого кольору, без запаху, розчинний у воді, гліцерині. Водні розчини є типовими псевдопластичними рідинами. Отримали й біорозчинний полімер, він широко використовується для лікарських біорозчинних очних плівок, які забезпечують максимальний час контакту з поверхнею кон’юнктиви. 1%-ві розчини ПАА використовують для пролонгування дії очних крапель. Успішно застосовують і інші види лікарських плівок – тринітролонг. Водні розчини ПАА сумісні з багатьма електролітами, ПАВ і консервантами. ПАА перспективний для створення нових лікарських форм.
Поліетиленоксиди (Polyaethylenoxyda) являють собою полімери етиленоксиду:
H( – OCH2 – CH2 – )nOH
Поліетиленоксиди (ПЕО) або поліетиленгліколі (ПЕГ) одержують шляхом полімеризації етиленоксиду в присутності води й гідроксиду калію.
Консистенція ПЕО залежить від ступеня полімеризації. Випускають ПЕО з різним ступенем полімеризації (М.М. 400 – 4 тис). ПЕО – 400 – в’язка прозора безбарвна рідина, ПЕО – 1500 – віск (температура плавлення 35 – 41°С), ПЕО – 4000 – тверда речовина білого кольору з температурою плавлення 53 – 61°С.
Характерною властивістю ПЕО є гарна розчинність у воді, етанолі. Вони не змішуються з вуглеводнями й жирами, не утворюють з ними емульсій; малочутливі до зміни рН, стабільні при зберіганні.
ПЕО мають низьку токсичність, що обумовлює досить широке застосування їх у фармацевтичній практиці – у технології мазей, емульсій, суспензій, супозиторіїв і інших лікарських форм. Основи для мазей найчастіше – це композиції рідких і твердих ПЕО, що мають в’язкопластичну консистенцію. Однак вони призводять до підвищеної сухості слизових оболонок.
ПЕО зручно використовувати також для супозиторних основ. Похідними полімерів етиленоксиду є спени й твіни.
Спени (Spans) – ефіри з вищими жирними кислотами.
Найчастіше застосовуються спени – ефіри вищих жирних кислот: спен – 20 – ефір лауринової кислоти С11Н33СООН; спен – 40 – ефір пальмітинової кислоти С15Н31СООН; спен – 60 – ефір стеаринової кислоти С17Н35СООН; спен – 80 – ефір олеїнової кислоти С17Н33СООН.
Спени є ліпофільніми сполуками. Вони розчинні в оліях, а також етанолі, утворюють емульсії типу вода/олія. У зв’язку з неіоногенним характером сумісні з багатьма лікарськими речовинами.
Твіни (Twins) – це моноефіри поліоксиетильованого сорбітану (спену) і вищих жирних кислот. Твіни одержують шляхом оброблення спенів етиленоксидом у присутності гідроксиду натрію (в якості каталізатору).
Етерифікація відбувається за місцем вільних гідроксидів. Твіни добре розчиняються у воді й органічних розчинниках. До медичного застосування дозволений твін – 80, що є моноефіром олеїнової кислоти.
Твін – 80 є неіоногенною ПАР. Він добре розчинний у воді, рослинних і мінеральних оліях. Слугує гарним емульгатором з високим значенням ГЛБ (15 – 16), тому застосовується і як солюбілізатор. Як емульгатор і стабілізатор твін – 80 застосовують для стабілізації емульсій і суспензій, у тому числі й для ін’єкційного введення.
Жиросахара (Adiposacchara) – неповні складні ефіри сахарози з вищими жирними кислотами (стеаринова, пальмітинова, лауринова тощо). Жиросахара – новий клас ПАР твердої, в’язкої і рідкої консистенції з досить цінними властивостями. Вони не мають запаху й смаку, в організмі розпадаються на жирні кислоти, фруктозу й сахарозу, індиферентні для шкіри. Застосовуються як солюбілізатори, емульгатори (при виготовленні емульсій для парентерального введення), стабілізатори.
Силікони (Siliconum) являють собою кремнійорганічні полімери. За структурою поділяються на лінійні, сітчасті й циклічні.
Серед кремнійорганічних полімерів найбільшого інтересу із фармацевтичної точки зору набувають поліорганосилоксани з лінійними ланцюгами молекул, що випускають у вигляді олігомерів (кремнійорганічні рідини). Основу силіконів складає силоксановий кістяк – ланцюг атомів, що чергуються, кремнію й кисню. Вільні зв’язки кремнію заповнені органічними радикалами (метильними, етильними, фенільними тощо). Найбільш широкого застосування одержали діетилполіорганосилоксанові рідини: полімер зі ступенем полімеризації 5 одержав назву есілон-4, а полімер зі ступенем конденсації 15 – есілон-5. Це безбарвні, прозорі, в’язкі, гігроскопічні рідини без запаху й смаку.
Силікони мають ряд цінних властивостей, що обумовлюють можливість їх застосування. У зв’язку з відсутністю хімічно активних груп вони характеризуються високою хімічною інертністю: не окиснюються, не піддаються дії агресивних середовищ, мають гідрофобні властивості, термостійкі, не змішуються з водою, етанолом, гліцерином. Силікони сумісні з компонентами мазей і лініментів (вазеліном, парафіном, рослинними оліями). У силіконах добре розчиняються полярні речовини (ментол, камфора, фенол тощо).
Біологічна інертність силіконів свідчить про їх перспективність для застосування як носіїв в лікарських препаратах за різних шляхів введення. Вони також використовуються для силіконізації скляної тари з метою підвищення хімічної й термічної стійкості, зниження гігроскопічності сухих екстрактів. Силіконові рідини використовують для захисту шкіри як креми, лосьйони і мазі. Гарна сумісність зі шкірою (не порушують дихання тканин, теплообмін), тканинами й слизовими оболонками, тривала стабільність і сумісність із багатьма лікарськими речовинами послужила підставою для їх використання як розчинників або носіїв у лікарських формах для внутрішньом’язового й нашкірного застосування.
Узагальнити сфери застосування полімерних матеріалів можна у Табл. 1.
Таблиця 1
Асортимент і сфера застосування полімерних матеріалів, дозволених для виготовлення виробів фармацевтичного призначення
№ |
|
Найменування |
|
Сфера застосування |
|
|
|
|
матеріалів |
|
|
|
|
|
|
|
ЕФІРИ ЦЕЛЮЛОЗИ |
|
|
|
1 |
|
Метилцелюлоза |
Згущувач і стабілізатор основ мазей і лініментів, |
|||
|
|
водорозчинна |
емульгатор і стабілізатор при вигтовленні рідких |
|||
|
|
|
емульсій, диспергуючий агент і покриття для пілюль і |
|||
|
|
|
таблеток, стабілізатор і пролонгатор дії лікарських |
|||
|
|
|
речовин в очних краплях |
|
|
|
2 |
|
Найтрійкарбо- |
Пролонгатор дії лікарських речовин в очних краплях та |
|||
|
|
ксиметицелюлоза |
ін’єкційних розчинах, емульгатор, стабілізатор і |
|||
|
|
|
||||
|
|
|
формоутворювач у мазях та емульсіях, зв’язувальний і |
|||
|
|
|
розпушувальний засіб у виробництві таблеток |
|||
3 |
|
Оксіпропілме- |
Плівкове покриття твердих лікарських форм (марки 15), |
|||
|
|
тилцелюлоза |
емульгатор у медичних аерозолях (марки 50А та 50В), |
|||
|
|
|
зв’язувальний засіб у виробництві таблеток (марки 100) |
|||
4 |
|
Етилцелюлоза |
При конструюванні лікарських форм: у технології |
|||
|
|
|
виготовлення таблеток (як коригент смаку), водозмивних |
|||
|
|
|
бактерицидних плівок |
|
|
|
5 |
|
Ацетилцелюлоза |
Сполучна речовина у виробництві таблеток, покриття для |
|||
|
|
|
таблеток |
|
|
|
6 |
|
Ацетилфталілц |
Покриття для кишково-розчинних таблеток і гранул |
|||
|
|
елюлоза |
|
|
|
|
|
|
ПОЛІМЕРИ І СОПОЛІМЕРИ ВЕНІЛАЦЕТАТУ |
|
|||
7 |
|
Полівініловий |
Використовується як дезінтоксикаційний засіб: при |
|||
|
|
спирт і його |
перитоніті, непрохідності кишківника, панкреатиті, |
|||
|
|
похідні |
холециститі, |
ураженнях |
печінки, |
різноманітних |
|
|
|
септичних станах, опіках і сепсисі. У технології |
|||
|
|
|
виготовлення ліків – емульгатор, згущувач і стабілізатор |
|||
|
|
|
суспензій, пролонгатор дії лікарських речовин, |
|||
|
|
|
плівкоутворювач для капсул і таблеток, компонент |
|||
|
|
|
мазевих основ |
|
|
|
8 |
|
Полівінілацетат |
Захисні колоїди та ПАР для виготовлення емульсій і |
|||
|
|
|
суспензій гідрофобних полімерних органічних матеріалів |
|||
9 |
|
Полі-N-вініл- |
Компонент різних лікарських форм драже, таблеток і |
|||
|
|
піролідон |
капсул, стабілізувальна емульсія і суспензія, пролонгатор |
|||
|
|
|
дії багатьох лікарських речовин |
|
||
|
ПОЛІМЕРИ І СОПОЛІМЕРИ АКРИЛОВОЇ І МЕТАКРИЛОВОЇ КИСЛОТ |
|||||
10 |
|
Поліакрилова і |
Для виготовлення аерозолів, лікарських плівок, мазей, |
|||
|
|
поліметакрилова |
рідких пластирів (клею шкірного), очних крапель, |
|||
|
|
кислоти |
таблеток, мікрокапсул, суспензій, емульсій |
|
||

|
|
|
|
Продовження таблиці 6.1 |
|
|
ПОЛІМЕРИ І СОПОЛІМЕРИ АКРИЛАМІДУ |
|
|||
11 |
Поліакриламід |
Матриця-носій лікарських речовин для одержання плівок, |
|||
|
|
пролонгатор дії очних крапель та анестезувальних і |
|||
|
|
знеболювальних лікарських речовин; використовується |
|||
|
|
для іммобілізації біопрепаратів (ферментів, гормонів); у |
|||
|
|
виробництві таблеток |
|
|
|
|
ПОЛІМЕРИ І СОПОЛІМЕРИ ОКИСУ ЕТИЛЕНУ ТА ЇХ ПОХІДНИХ |
||||
12 |
Твіни |
Для створення мазей, емульсій, суспензій, аерозолів, |
|||
|
|
таблетованих лікарських форм, твердих дисперсних |
|||
|
|
систем |
|
|
|
|
|
НЕОРГАНІЧНІ ПОЛІМЕРИ |
|
|
|
13 |
Бентоніти |
При виготовленні багатьох лікарських форм: мазей, |
|||
|
|
таблеток, гранул, пілюль, емульсій, зубних паст |
|||
14 |
Аеросили |
Для стабілізації суспензій, олійних лініментів, гелів. Як |
|||
|
|
допоміжні речовини у виробництві таблеток, порошків, |
|||
|
|
екстрактів, суппозиторіїв, пілюль |
|
||
|
|
|
ПОЛІОЛЕФІНИ |
|
|
15 |
Поліетилен |
Для виготовлення поліетиленових пакетів, флаконів, |
|||
|
високого тиску |
банок, |
призначених |
для |
розфасовування |
|
|
порошкоподібних і рідких лікарських засобів. Шприц- |
|||
|
|
тюбики – для тривалого зберігання ін’єкційних розчинів. |
|||
|
|
Тюбик-крапельниці – для тривалого зберігання розчинів |
|||
|
|
очних крапель |
|
|
|
16 |
Поліетилен |
Застосовується мало, але в перспективі – для |
|||
|
низького тиску |
виготовлення банок, пробірок, флаконів для таблеток, |
|||
|
|
порошків, мазей, і рідких лікарських засобів (більш |
|||
|
|
термостійкий порівняно з поліетиленом високого тиску) |
|||
17 |
Поліпропілен |
Плівка, листи, плити, труби, об’ємні вироби: сулії, |
|||
|
|
флакони, тюбики, ємності для аерозолів, пробірки, |
|||
|
|
коробки, банки для мазей та паст, коробки і банки для |
|||
|
|
таблеток, драже, гранул і порошків, пробірки для |
|||
|
|
таблеток і драже |
|
|
|
18Полі-4-метил- Плівки для контурної упаковки, коробки, стаканчики, пентен-1 пробірки, тара для лікарських засобів
19Поліізобутилен Герметизувальний засіб
|
|
ПОЛІВІНІЛХЛОРИД |
20 |
Полівінілхлорид |
Для виготовлення чарункової упаковки коміркового типу |
|
|
«Сервак», для пакування таблеток, драже і супозиторіїв в |
|
|
умовах промислового виробництва |
21 |
Сополімери |
Для пакування готових лікарських форм: порошків, |
|
вінілхлориду |
таблеток, гранул, рідин |
|
|
ПОЛІКАРБОНАТИ |
22 |
Полікарбонати |
Для виготовлення чашок Петрі, фільтрів для крові, |
різноманітних інструментів, очних лінз, шприців, зубних протезів, закупорювального та пакувального матеріалу, флаконів, сулій, банок, коробок, пакетів, коробок
Формотворні речовини (розчинники)
Розчинники є основними допоміжними речовинами у технології ліків з рідким дисперсійним середовищем.
Розчинники – хімічні сполуки або їх суміші, здатні розчиняти різноманітні речовини, тобто утворювати з ними однорідні системи – розчини, що складаються з двох або більше компонентів.
Відомо багато класифікацій розчинників. Найпоширенішої є хімічна класифікація (Рис. 5), відповідно до якої розчинники поділяються на органічні (неводні) і неорганічні (водні).
На теперішній час у технології розчинів для збільшення розчинності важкорозчинних лікарських речовин використовуються комбіновані (змішані) розчинники, число яких практично не обмежене, такі, як водногліцеринові, спиртово-водно-гліцеринові, суміші рослинних олій з бензилбензоатом, етилолеатом тощо. Саме комбіновані (змішані) середовища можуть виявитися найкориснішими розчинниками, що сполучать здатність до стабілізації гідрофільних і гідрофобних розчинених речовин. Різниця в поверхнево-активних властивостях води й гідрофільних неводних розчинників дозволяє за рахунок їхнього змішування у необхідних пропорціях керувати ліофільністю дисперсійного середовища, а це – найважливіший фактор впливу на властивості дисперсних систем.
Розчинники
|
|
Органічні |
|
|
Комбіновані |
|
Неорганічні |
||||
|
|
(неводні) |
|
|
(змішані) |
|
(водні) |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Вода-гліцерин |
|
|
|
|
|
|
|
|
|
|
|
Етиловий спирт- |
|
|
|
Леткі |
|
|
Не леткі |
|
|
|||||
|
|
|
|
|
вода-гліцерин |
|
|||||
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
Етиловий спирт - |
|
|
Етиловий спирт |
|
Гліцерин |
|
ПЕО |
|
||||||
Ефір медичний |
|
Олії жирні |
|
Бензил бензоат- |
|
||||||
|
Хлороформ |
Олії мінеральні |
|
рослинне масло |
|
||||||
Бензиловий спирт |
|
Силікони |
Спирт бензиловий- |
|
|||||||
Бензил бензоат |
|
|
ПЕО |
|
вода |
|
|||||
Рис. 5. Класифікація розчинників
При виборі розчинника для конкретних цілей необхідно виходити з найважливіших фізичних властивостей, що характеризують його природу. До них, в першу чергу, належать точка кипіння, густина, питома електрична провідність, діелектрична проникність, в’язкість тощо.
Розчинники повинні мати високу стійкість, хімічну й фармакологічну індиферентність, мати високу розчинювальну здатність, не мати неприємного запаху, смаку, не повинні слугувати середовищем для розвитку мікроорганізмів, бути загальнодоступними, дешевими.
Пролонгувальні речовини Пролонгаторами називаються допоміжні речовини, які зберігають в
організмі впродовж тривалого (заданого) часу терапевтично активну концентрацію діючої речовини, у тому числі надходження її із заданою швидкістю. Лікарські засоби пролонгованої дії – це лікарські речовини у спеціальній лікарській формі, що забезпечує збільшення тривалості дії лікарського препарату.
Пролонгувальна дія ліків становить значний інтерес для фармакотерапії й замісної терапії, де необхідне забезпечення тривалої й постійної концентрації препарату в біологічних рідинах організму. Створення пролонгованих ліків має не тільки медичне, але й економічне значення, оскільки дозволяє збільшити їх стабільність у процесі зберігання й застосування.
До пролонгувальних речовин, окрім загальних вимог до допоміжних речовин, варто ще віднести підтримання оптимального рівня концентрації діючих речовин в організмі, зменшення швидкості вивільнення їх з лікарської форми, можливості депонування в органах і тканинах, інактивації їхніми ферментами й зменшення швидкості виведення з організму.
У наш час при розробленні ліків пролонгованої дії застосовуються хімічні, фізіологічні й технологічні методи.
Пролонгування ліків хімічними методами основане на збільшенні молекули лікарської речовини шляхом зв’язування її з іонообмінними смолами або утворенням важкорозчинних комплексів. При цьому лікарські речовини основного характеру приєднуються до катіонів із сульфогрупами –
–О–SO2 або до карбоксильних груп.
Речовини кислого характеру (наприклад, похідні барбітурової кислоти) з метою пролонгування приєднують до аніонітів. Іноді лікарські речовини, що містять аміногрупи, зв’язуються таніном. Амінотаніновий комплекс утворюється в результаті реакції взаємодії спиртового розчину діючої речовини з надлишком таніну. Комплекс нерозчинний, але в присутності електролітів або при зниженні рН здатний поступово вивільняти лікарську речовину. Однак слід зазначити, що пролонгація лікарських речовин хімічними методами не завжди можлива.
Фізіологічні методи пролонгування полягають у впливі різних факторів (найчастіше таких речовин, як етамід, лонгацид тощо) на організм із метою затримки виведення лікарської речовини. Цей метод часто небезпечний для хворого, у зв’язку з чим мало використовується.
Уповільнення всмоктуваності лікарських речовин може бути досягнуте за рахунок введення судинозвужувальних речовин (наприклад, прокаїна з адреналіном), фенольних четвертинних амонієвих основ або органічних
фосфатів, що затримують виділення холінестерази, завдяки чому уповільнюється гідроліз ацетилхоліну. Порушення ж рівноваги ацетилхолінхолін зменшує утворення ацетильних груп, у результаті чого уповільнюється метаболізм, оснований на реакціях ацетилювання.
На практиці найчастіше застосовують технологічні методи пролонгування ліків: підвищення в’язкості дисперсійного середовища (включення лікарської речовини в гель), іммобілізація лікарських речовин на різних носіях, суспендування розчинних лікарських речовин, створення нових сполук лікарських і допоміжних речовин за рахунок утворення ковалентних або іонних зв’язків, укладання діючих речовин у плівкові оболонки (мікрокапсули), створення очних або стоматологічних лікарських плівок.
Так, при розробленні ін’єкційних ліків пролонгувального ефекту можна досягти одержанням солей різної розчинності або ж зміною в’язкості розчину: чим в’язкість більша, тим повільніше відбувається процес всмоктування. На цьому принципі засноване використання в ін’єкційних ліках рослинних олій, етилолеату. Однак збільшення в’язкості розчинника може бути досягнуте й за рахунок використання водних розчинів з додаванням до них метилцелюлози, натрій-карбоксиметилцелюлози, полівінілпірролідону, желатину, декстрану тощо.
Пролонгуювальний ефект можна одержати й у результаті використання неводних розчинників (пропіленгліколю, поліетиленоксиду) як дисперсійного середовища. Широке розповсюдження у фармацевтичній практиці одержали гелі й гідролі високомолекулярних сполук. Вони застосовуються як пролонгатори у м’яких лікарських формах (мазях, лініментах, пластирах, капсулах тощо), а також можуть слугувати компонентами (резервуарами) макромолекулярних терапевтичних систем як матричного, так і мембранного типу, у яких регулюють швидкість виділення діючих речовин.
Значний інтерес у пролонгації лікарських речовин представляє мікрокапсулювання. Цей метод полягає у включенні діючих речовин (ферментів, антибіотиків, вітамінів) в оболонки з полімеру – мікрокапсули. Останнім часом, як такі пролонгатори використовуються полімери полісахаридної природи (альгінати, декстрани, а також деякі синтетичні полімери).
Ефективним методом пролонгування, а одночасно й збільшення стабільності лікарських речовин є метод включення їх у структуру клатратів
– клатратоутворення або ж «сполучення – включення». До речовин, що утворюють клатратні сполуки належать сечовина, тіосечовина, холеїнові кислоти, протеїни, циклодекстрини тощо.
Для зменшення швидкості вивільнення лікарських речовин з очних крапель вводять високомолекулярні речовини: метилцелюлозу (0,5 – 2%), натрійкарбоксіметилцелюлозу (0,5 – 1%), полівініловй спирт (1,5%), аубазідан (0,1 – 0,3%), полівінілпірролідон, альгінати, колаген тощо.
Як пролонгатори лікарських речовин в очних мазях використовують оксіпропілцелюлозу, поліакриламід, натрій альгінат, полівініловий спирт, полівінілпірролідон, карбопол і інші, здатні утворювати гелі, що мають значну перевагу перед ланолін-вазеліновою основою.
Таким чином, пролонгація лікарських речовин з використанням різних природних і синтетичних речовин не тільки підвищує їх стабільність, але й призводить до значного збільшення ефективності самих ліків. Варіюючи природу допоміжної речовини, що використовується для пролонгації, можна в значній мірі підвищувати або знижувати розчинність лікарських препаратів. Пролонгатори дозволяють тривалий час підтримувати терапевтичні концентрації лікарських речовин у внутрішніх середовищах й тканинах організму.
Стабілізатори Стабілізаторами (стабілізувальними речовинами) називаються
речовини, що сприяють збереженню фізико-хімічних, мікробіологічних властивостей, активності ліків, передбачених вимогами відповідної НТД впродовж строку їх зберігання.
Процес стабілізації ліків варто розглядати як досить актуальну комплексну проблему, що включає вивчення стійкості ліків до мікробної контамінації у вигляді різних дисперсних систем. Класифікація стабілізаторів, що використовуються у фармації, представлена на Рис. 6.
На стійкість ліків впливають фізичний стан речовини, температура зберігання, оточуюча атмосфера й світло, упаковка, спосіб виготовлення ліків, підбір допоміжних речовин, вид лікарської форми.
У наш час відомі два методи стабілізації ліків – фізичний і хімічний, які часто доповнюють один одного. Широта їхнього застосування обумовлена, головним чином, природою й властивостями лікарських речовин, видом лікарської форми, рівнем технологічного процесу виготовлення й фізіологічною доцільністю застосування.
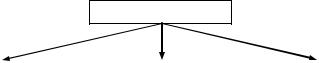
СТАБІЛІЗАТОРИ
Фізико-хімічні |
|
Протимікробні |
|
|
|
|
|
|
стабілізатори |
|
Хімічні речовини |
|
|||
(дисперсні системи) |
|
|
|
||||
|
(консерванти) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
желатоза |
|
|
речовини, |
які |
гальмують |
||
похідні целюлози |
|
|
гідролітичні |
процеси |
(HCl, |
||
мікробні полісахариди |
|
|
NaHCO3, NaOH буферні |
||||
полівінілпіролідон |
|
|
розчинники, |
|
поверхнево- |
||
альгінати |
|
|
активні |
|
речовини); |
||
пектини |
|
|
речовини, |
які |
гальмують |
||
полівініловий спирт |
|
|
окислювально-відновні |
|
|||
бентоніти |
|
|
процеси |
|
(прямі |
||
пентол |
|
|
антиоксиданти |
– |
Na2S, |
||
твіни |
|
|
ронгаліт, |
|
тіосечовина, |
||
спени |
|
|
параамінофенол аскорбінова |
||||
емульгатор Т-2 |
|
|
кислота; консерванти – |
||||
емульгатор №1 та ін. |
|
|
ЕДТА, трилон-Б, тетацин- |
||||
|
|
|
|
кальцій). |
|
|
|
Рис. 6. Класифікація стабілізаторів
Найбільш фізіологічно виправданими можуть вважатися методи фізичної стабілізації ліків, як кращі з позиції біофармації й нешкідливості фармацевтичних препаратів, що містять високоактивні інгредієнти, які характеризуються широким спектром дії.
Фізичні методи стабілізації, як правило, основані на захисті лікарських речовин від несприятливих впливів зовнішнього середовища, припускають використання високоякісних допоміжних речовин, сучасного технологічного оснащення й наукових досліджень у технології ліків.
В останні роки запропонований ряд фізичних прийомів підвищення стійкості ліків у процесі їх виготовлення й зберігання. Це використання неводних розчинників (поліетиленгліколь, пропіленгліколь, полівініловий спирт, бензилбензоат), сублімаційне (ліофільне) сушіння термолабільних речовин (так, водний розчин бензилпеніциліну зберігає свою активність упродовж 1 – 2 діб, у той час як зневоднений препарат активний впродовж 2
– 3 років), ампулювання розчинів у струмі інертних газів, нанесення захисних покриттів на тверді гетерогенні системи (таблетки, драже, гранули), а також мікрокапсулювання.
Для підвищення антимікробної стабільності використовують одержання ліків разового застосування (розчини для ін’єкцій, очні краплі тощо).
Однак методи фізичної стабілізації не завжди ефективні. Тому хімічні методи стабілізації основані на введенні в ліки особливих допоміжних речовин – стабілізаторів, знаходять широке застосування. Даний вид стабілізації має важливе значення для ліків, які піддаються різним видам стерилізації, особливо термічній. Хімічний метод стабілізації використовується при виготовленні гетерогенних і гомогенних ліків.
Механізм дії хімічних стабілізаторів зводиться до створення певного рН середовища, попередження окисно-відновних процесів і до збільшення розчинності лікарських речовин – солюбілізації.
Необхідне значення рН середовища в гомогенних ліках досягається буферними розчинами, кислотами й лугами. Наприклад, при використанні як стабілізаторів слабких розчинів мінеральних кислот (найчастіше – хлористоводневої) досягається стабільність ін’єкційних розчинів, які є солями слабких основ і сильних кислот (апоморфіну гідрохлорид, атропіну сульфат, гомотропіну гідробромід, дибазол, дикаїн тощо).
Додавання до цих розчинів кислоти, тобто надлишку водневих іонів, пригнічує процес гідролізу, що помітно підсилюється при їх нагріванні під час стерилізації. Стабільність препаратів, що є солями сильних основ і слабких кислот (кодеїн-бензоат натрію, натрію нітрат, натрію тіосульфат, нікотинова кислота, еуфілін тощо) вдається підвищити додаванням як стабілізатора розчину натрію гідроокису або натрію гідрокарбонату.
Стабілізація лікарських препаратів (ін’єкційних розчинів) за рахунок зміни рН середовища – не єдиний спосіб захистити діючі речовини від гідролізу. Як стабілізатори можуть бути використані неіоногенні й аніонактивні ПАР, які впливають на кінетику хімічних реакцій за рахунок зменшення швидкості реакції шляхом утворення міцел – асоціатів. Міцели ПАР мають порожнини, у які під впливом сил міжмолекулярної взаємодії можуть проникати відносно невеликі молекули лікарської речовини. Комплексні сполуки, які утворюються, більш стійкі, ніж лікарські речовини. У зв’язку з цим ПАР використовують для зменшення гідролізу анестетиків, антибіотиків і інших речовин. У кожному конкретному випадку використання стабілізатора вимагає ретельного вивчення його впливу на організм при введенні до складу лікарського препарату.
Як стабілізатори ліків, що легко окиснюються під впливом кисню (адреналіну гідротартрат, вікасол, дипразін, салюзид, сульфацил-натрію тощо), широко використовуються на практиці різні антиоксиданти, які можна розділити на прямі й непрямі антиоксиданти.
До прямих антиоксидантів належать сильні відновники, що мають вищу здатність до окиснювання, ніж стабілізовані ними лікарські речовини: натрію сульфіт, натрію метабісульфіт, кислота аскорбінова, ронгаліт, карбамід, параамінофенол.
Механізм стабілізації діючих речовин прямими антиоксидантами полягає в тому, що антиокиснювачі легше окиснюються, ніж діючі речовини, і кисень, розчинений в ін’єкційному розчині, витрачається на окиснювання стабілізатора, тим самим захищаючи субстанцію від окиснювання.
До непрямих антиоксидантів–комплексоутворювачів належать речовини, що зв’язують у практично недисоційовані сполуки катіони металів (Сu, Fе, Ni, Мn, Со і ін.), які можуть потрапляти в розчини лікарських речовин як домішки до них, а також вимиватися зі скла, апаратури.
Іони важких металів, приймаючи участь у ланцюговій окисно-відновній реакції, здатні відривати електрони від присутніх разом з ними в розчинах
