
- •210104 «Микроэлектроника и твердотельная электроника».
- •2.Тесты первого промежуточного контроля знаний по общей химии Контролируемые темы:
- •3.Тесты второго промежуточного контроля знаний по общей химии Контролируемые темы:
- •4.Тесты третьего промежуточного контроля знаний по общей химии Контролируемые темы:
- •5.Образец итогового экзаменационного теста.
2.Тесты первого промежуточного контроля знаний по общей химии Контролируемые темы:
Основные понятия и законы химии. Закон эквивалентов.
Состав и строение атома.
Свойства элементов и их соединений
Химическая связь
Типы взаимодействия молекул
А. Основные понятия и законы химии. Закон эквивалентов.
Найдите ошибочное утверждение. К химическим свойствам вещества относят: а)взаимодействие с кислотами б) электропроводность в) изменение цвета при нагревании г) горение
Количество вещества – это: а)порция вещества, измеренная в молях б) число структурных единиц, равное 6ּ1023 в)масса вещества г) навеска вещества
Чистыми называют вещества, которые: а) обладают постоянными свойствами б) нельзя обнаружить под микроскопом разнородные частицы в) состоят из молекул одного вида г) не содержат примесей
Вычислить количество вещества и количество эквивалентов вещества в 39 г Na2S.
a) ν Na2S =1 моль б ) νNa2S=0,5моль в)νNa2S=νэкв. г)νNa2S=39
ν экв=0,5 νэкв=1 моль νэкв=0,5 моль νэкв=19,5
Рассчитать молярную массу эквивалента KMnO4 восстановленной до MnO2.
а ) 52,6 г б) 31,6 в) 158 г г) 48,6
Рассчитать молярную массу эквивалента HNO3 при ее восстановлении до NO2.
а ) 21 г б) 63 г в) 0,031 г г) 3,1 г
Чему равна молярная масса эквивалента ортофосфорной кислоты в обменных реакциях?
а ) 21 г б) 32,6 в) 31 г г) 27 г
Объем равный 11,2 л занимает: а) 14 г N2 б) 2 г H2 в) 8 г O2 г) 17 г Cl2
Б. Состав и строение атома.
Укажите сколько нейтронов в ядре изотопа бария
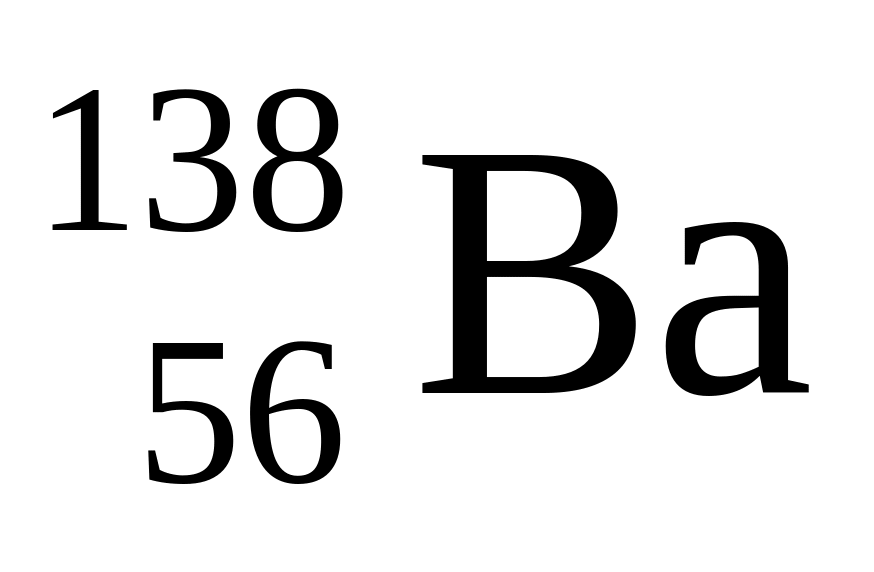 а
)56 б )82 в )138 г ) 194
а
)56 б )82 в )138 г ) 194
Укажите сколько электронов в атоме изотопа калия
 а
)40 б )19 в )21 г ) 59
а
)40 б )19 в )21 г ) 59
Какому иону соответствует формула: 1S22S22P63S23P63d104S2
a ) Zn2+ б ) Са2+ в ) As3+ г ) Se
Какая формула соответствует F-?
а ) 1S22S22P4 б ) 1S22S22P6 в ) 1S22S22P3 г ) 1S22S22P5
Какому иону соответствует формула: 1S22S22P63S23P63d10
а ) As5+ б ) Са2+ в ) Fe2+ г ) Br-
Какие электроны атома хрома участвуют в образовании химических связей?
а ) 3 d54S1 б ) 3 d 64S0 в ) 3d44S2 г ) 3 d 7
Указать электронную конфигурацию азота в степени окисления +5.
а) 2s22p6 б) 2s02p0 в) 2s22p3 г)2s22p5
Электронная конфигурация атома углерода в возбужденном состоянии:
а) 2s22p2 б) 2s22p4 в) 2s12p3 г) 2s22p4
На энергетическом уровне с главным квантовым числом, равным 3, максимально может расположиться электронов: а) 2 б) 18 в) 32 г) 26
Химический элемент, завершающий седьмой период, еще не открыт. Однако научный прогноз позволяет определить его порядковый номер: а) 120 б) 118 в) 110 г) 116
На каком подуровне энергия электрона максимальна:
а) 2s б) 2p6 в) 3d г) 4P
На энергетическом подуровне с орбитальным квантовым числом, равным 3, максимально может расположиться электронов: а) 2 б) 6 в) 10 г) 14

В. Свойства элементов и их соединений
Как меняется электроотрицательность в ряду: F, CI, Br, I?
а ) возрастает, б ) убывает в ) периодически меняется г) остается постоянной.
У какого из перечисленных элементов наибольшее сродство к электрону?
а ) О б ) S в ) Se г ) Те
Энергия ионизации атомов в группе растет
а) слева-направо б ) снизу вверх в) от бора а астату
г) справа – налево.
Атом, какого элемента имеет наибольший радиус?
а ) С б ) В в ) О г ) F
Для какого элемента справедливо уравнение реакции:
Э2О7 + Н2О ↔ 2НЭО4
а ) Р б ) N в ) CI г ) S
Для какого элемента справедливо уравнение реакции
Э2О5 + 3 Н2О ↔ 2 Н3ЭО4
а ) В б ) Р в ) CI г) N
Формула высшего оксида элемента, образующего летучий гидрид состава ЭН2:
а ) ЭО б ) ЭО2 в ) ЭО4 г ) ЭО3
При взаимодействии, какого элемента с кислородом образуется пероксид?
а ) Fe б ) Na в ) Li г )Mg
Какие из ниже написанных оснований будут реагировать с едким натром?
а ) Zn(OH)2 б ) Al(OH)3 в ) Mg(OH)2 г ) Fe(OH)2
Укажите, какие из ниже написанных окислов можно отнести к кислотным:
а ) SO2 б ) FeO3 в ) Cr2 O3 г ) СаО
Установите, в каком случае наблюдается несоответствие соответствие между левыми и правыми частями уравнений реакций взаимодействия:
а )![]() б
)
б
)
![]()
в )
![]() г )
г )
![]()
Правые части уравнений реакций взаимодействия:
|
|
|
|
|
|
|
|
12. При взаимодействии SO2с избытком едкого натра образуются:
а ) гидросульфит натрия б ) гидросульфат натрия в ) сульфит натрия и вода г ) сульфат натрия и вода.
13.В каком случае происходит реакция образования соли? а )K2O + FeO → б )HgO + CaO → в ) Na2O + N2O3 → г )P2O5 + CO2 →
14. В какой смеси веществ возможна химическая реакция?
а ) SO2 + HCI ↔ б ) SO2 + Na2O↔
в ) SO2 + CO2 ↔ г ) SO2 + Na2SO4
14.Какое из приведенных ниже соединений имеет название сульфид натрия? ٱ Na2S2O3 ٱ Na2SO3 ٱ Na2SO4 ٱ Na2S
Г. Химическая связь
В каком из соединений образуется наиболее прочная химическая связь?
а ) LiF б ) LiCI в ) LiBr г ) LiI
Укажите вещества с преимущественно ионным типом связи: ٱ Na2O ٱ H2O ٱ HCl ٱ H2
Вещества, содержащие только ковалентные полярные связи:
а)H3PO4, BF3, CH3COONH4
б) H2SO4, F2, P2O5
в) PF5, Cl2O7, NH4Cl
г)NO2, SOCl2, CH3COOH
4.В каком веществе нет химических связей между атомами серы? а) натрий дисульфид б) сероуглерод в) натрий дитионит г)натрий тиосульфат
5.Определите, каким кислотам принадлежат приведённые ниже графические формулы:
1.
![]() 2.
2.

6.Определите, графическая формула какой соли приведена ниже, напишите ее химическую формулу:
|
|
|
|
|
|
Какие элементы, химические знаки которых приведены ниже, способны к образованию межмолекулярных водородных связей:а) Sе,б) C,в) O,г) Te,
Г. Типы взаимодействия молекул
Какой заряд имеет ион [Fe2+(NC)5OH2] ?
а) 3- б ) -2 в ) 3+ г ) +2
Определить степень окисления и к.ч. комплексообразователя в NH4CI.
a) +1, 4 б) -3, 1 в) -3,4 г ) +1,1
Чему равен заряд комплексного иона [Fe(NO)6]CI3
a) 3+ б) 1+ в) 4+ г) 2+
Чему равно к.ч. кобальта в соединении К2[Со(NH3)2(NO2)4]?
а) 2 б) 4 в) 6 г) 8
Степень окисления и к.ч. комплексообразователя [Pt(NH3)4CI2]2+
а ) +2;4 б) +4;6 в) +2;6 г) +4; 4
Какой заряд комплексного иона К3[Cr(OH)6]?
а ) 3+ б) 3- в) 1- г) 1+
Ртуть(II) нитрат при действии избытка калий иодида перейдет в: а) ртуть(I) иодид б) ртуть(II) иодид в) ртуть г) калий тетраиодомеркурат(II)
Какой комплексный ион образуется при взаимодействии двух солей CrCl3 + 3KCl: а) [KCl6]3- б)[K3(CrCl6)]3+ в) [CrCl6]3- г) [Cr(K3Cl)]3+
ВСЕГО 50 тестов

