
- •Тема 1.5. Виробництво алюмінію
- •Властивості і застосування алюмінію
- •Алюмінієві руди
- •Виробництво глинозему
- •Електроліз глинозему
- •Рафінування алюмінію
- •Алюмінієві сплави
- •Тема 1.6. Виробництво магнію
- •Властивості і застосування магнію
- •Магнієві руди
- •Одержання магнію в електролізері
- •Магнієві сплави
- •Тема 1.7. Виробництво міді
- •Властивості міді
- •Сировина для виробництва міді
- •Одержання мідних штейнів
- •Переробка мідного штейну і одержання чорнової міді
- •Рафінування міді
- •Мідні сплави
Тема 1.5. Виробництво алюмінію
Властивості алюмінію та його застосування.
Алюмінієві руди.
Виробництво глинозему.
Електроліз глинозему.
Рафінування алюмінію.
Алюмінієві сплави, їх класифікація, марки.
Властивості і застосування алюмінію
Алюміній – другий після заліза метал сучасної техніки, найпоширеніший в земній корі (8,8%).
Густина алюмінію 2,7 г/см3; температура плавлення tпл = 660оС; температура кипіння tкип близько 2500оС; межа міцності на розрив σВ = 90 – 180 МПа; твердість НВ 20-40.
Алюміній має добру електропровідність, високу теплопровідність та теплоємкість, хімічну стійкість проти органічних кислот, добру опірність азотній кислоті. На повітрі вкривається оксидною плівкою, яка захищає його від корозії.
Має високу пластичність, важко обробляється різанням, має значну лінійну усадку.
Застосування:
чистого алюмінію – виготовлення електропроводів, кабелів, посуду, фольги, захист інших металів і сплавів від окислення;
алюмінієвих сплавів – деталі літаків, автомобілів, вагонів, приладів і т.п.
Алюмінієві руди
Алюміній зустрічається у вигляді мінералів:
боксити (алюміній у вигляді гідрооксидів Al(ОН)3);
нефеліни (Na(K)2O.Al2O3.2SiO2);
кіаніти (Al2O3. SiO2);
алуніти (К2SO4.Al2(SO4)3.4 Al(ОН)3;
каоліни (Al2O3. 2SiO2.2Н2О).
Всі руди містять глинозем Al2O3.
Основні етапи виробництва алюмінію:
одержання глинозему з руди;
електроліз глинозему;
рафінування алюмінію.
Виробництво глинозему
Розглянемо один із способів – спікання.
Шихта (боксит, вапняк, водний розчин соди Na2CO3) тонко розмелюється і направляється в трубчасті обертові печі, де при температурі 300 – 400оС волога випаровується. Потім шихта переміщується в гарячу зону з температурою 1200 – 1250оС, де глинозем з’єднується з содою з утворенням алюмінату натрію Na2O.Al2O3, розчинного у воді. Його охолоджують, подрібнюють і поміщають в слабкий розчин соди. Алюмінат натрію переходить в розчин, який фільтрують і піддають карбонізації (продуванню вуглекислим газом СО2):
Na2O.Al2O3 + СО2 + 3Н2О = Na2CO3 + Al2O3.3 Н2О
Гідрат окису алюмінію Al2O3.3 Н2О випадає в осад, який відокремлюють фільтрацією, а потім випаровують вологу в трубчастих обертових печах і одержують безводний глинозем для електролізу.
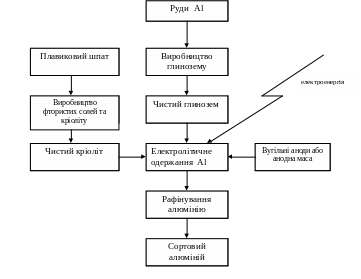
Загальна схема виробництва алюмінію
Електроліз глинозему
Алюміній одержують електролізом розплавлених солей – пропусканням струму крізь розплавлений електроліт. Електроліт складається з кріоліту Na3AlF6 та 1 – 8% глинозему.
Схема будови електролізера для одержання алюмінію наведена на рисунку 1.5.
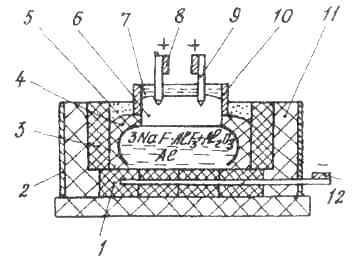
Рисунок 1.5. Схема будови електролізеру для одержання алюмінію:
1 - під; 2 - кожух; 3 – вугільні блоки; 4 – кірка електроліту; 5 - глинозем; 6 - анод; 7 - анодна маса; 8, 12 - шина; 9 - штир; 10 - кожух анодної маси; 11 – футерівка.
Електролізер складається із зварного корпусу, футерованого вугільними блоками. До поду підведено катод (негативний полюс). Над корпусом знаходяться вугільні аноди (позитивний полюс).
В електролізер заливається електроліт з температурою 1000оС, в розплав опускають аноди, пропускають електричний струм. Електроліт залишається в розплавленому стані за рахунок теплоти, що виділяється при проходженні струму. Електроліт, що захолонув, утворює тверду кірку, на яку насипають порошкоподібний глинозем.
Процес електролізу полягає в дисоціації глинозему на іони:
Al2O3 → 2 Al3+ + 3О2-
та розряді цих іонів. Іони алюмінію осідають на катоді, і на дні ванни під шаром розплавленого електроліту утворюється шар розплавленого алюмінію. Іони кисню розряджаються на аноді з утворенням СО і СО2.
Анодний ефект виникає, коли в електроліті стає менше 1% глинозему. Його прояви: стрибок напруги (від 4 В до 30 – 50 В), поява електродуг біля аноду, перегрів електроліту. Для ліквідації анодного ефекту пробивають кірку електроліту і розчиняють у ньому глинозем, завчасно насипаний на кірку. Після цього анодний ефект припиняється, процес електролізу нормалізується.
Дістають алюміній з електролізеру не частіше одного разу на добу (як правило, один раз за 3-4 доби), пробиваючи кірку, відкачують алюміній у вакуумний ківш футерованою стальною трубкою. Видобутий алюміній продувають газом у ковші для видалення неметалевих включень, направляють в електропечі опору, з яких розливають у зливки.
Для одержання 1 т алюмінію витрачають:
14 – 17 МВт.г електроенергії;
близько 2 т глинозему.
Первинний алюміній ділиться на:
алюміній особливої чистоти – А999;
алюміній високої чистоти – А995; А99; А97; А95;
алюміній технічної чистоти – А85; А8; А7; А6; А5; А0.
Цифри після букви А вказують вміст алюмінію, наприклад: А85 – первинний алюміній, що містить 99, 85% алюмінію, решта – домішки.
В електролізері одержують алюміній технічної чистоти. Для одержання алюмінію вищої чистоти проводять рафінування.
