
- •Термохімія
- •Молекулярність і порядок реакції
- •Кінетика необоротних реакцій
- •Необоротна реакція першого порядку
- •Необоротна реакція другого поряду
- •3.1 Електрохімічні процеси та їхнє медико-біологїчне значення. Розчини електролітів.
- •3.3 Кондуктометричне визначення ступеня та константи йонізації слабкого електроліту. Закон розведення Оствальда.
- •3.4 Кондуктометричне титрування. Застосування кондуктометрії в медицині.
- •4.1 Електродні потенціали та механізм їх виникнення. Рівняння
- •4.3 Електрохімічні (гальванічні) елементи та електрорушійні сили.
- •4.4. Дифузійні та мембранний потенціали, їхнє біологічне значення. Рівняння Нернста.
- •4 .5 Потенціометрія: потенціометричне визначення рН за допомогою воднево-хлорсрібного та хлорсрібного скляного елемента. Потенціометричне титрування.
- •Ізотерма адсорбції Ленгмюра
- •5.2 Адсорбція на межі поділу рідина - газ та рідина - рідина. Рівняння Гіббса. Орієнтація молекул поверхнево-активних речовин у поверхневому шарі.
- •5.3 Уявлення про структуру біологічних мембран. Адсорбція на межі поділу тверде тіло - газ.
- •5.4 Адсорбція із розчину на поверхні твердого тіла. Фізична та хімічна адсорбція. Закономірності адсорбції розчинених речовин, парів та газів. Рівняння Фрейндліха.
- •6.1 Адсорбція електролітів: специфічна (вибірна) та йонообмінна. Правило Панета- Фаянса.
- •6.2. Йонообмінники природні та синтетичні. Роль адсорбції та йонного обміну в процесах життєдіяльності рослин і організмів.
- •6.3. Хроматографія. Класифікація хроматографічних методів аналізу за ознакою агрегатного стану фаз, техніки виконання та механізму розподілу. Адсорбційна, йонообмінна та розподільча хроматографія.
- •6.4. Застосування хроматографії в біології та медицині. (спрс)
- •7.1 Загальна характеристика дисперсних систем: основні визначення та класифікація.
- •7.3 Електричні властивості колоїдно-дисперсних систем: механізм утворення подвійного електричного шару. Рівняння Гельмгольца-Смолуховського. Електрофоретична рухливість.
- •7.4 Електрокінетичні явища: електроосмос, електрофорез, потенціали перебігу та седиментації. Застосування електрофорезу в дослідницькій та клініко-лабораторній практиці.(спрс)
- •8.1 Стійкість та коагуляція дисперсних систем. Коагуляція гідрофобних золів під дією електролітів. Поріг коагуляції. Правило Шульце—Гарді.
- •9.1 Високомолекулярні сполуки - основа живих організмів. Глобулярна та фібрилярна структура білків. Порівняльна характеристика розчинів високомолекулярних сполук, істинних та колоїдних розчинів.
- •9.3 Аномальна в'язкість розчинів вмс. В'язкість крові. Мембранна рівновага Доннана.
- •9.4 Ізоелекгричний стан білка. Ізоелєктрична точка та методи її визначення. Йонний стан біополімерів в водних розчинах.
- •9.5 Значення високомолекулярних сполук (вмс) у медицині та фармації. (спрс).
4.4. Дифузійні та мембранний потенціали, їхнє біологічне значення. Рівняння Нернста.
Дифузійні потенціали
Стрибок потенціалів у гальванічних елементах може виникати не лише на поверхні розділу електрод - розчин, але і на межі розділу розчин - розчин (двох електродних розчинів, розділених напівпроникною перегородкою). Цей потенціал виникає за рахунок різної швидкості руху різних за природою іонів через межу розділу і називається дифузійним потенціалом. Виникнення такого потенціалу можна розглянути на прикладі наступного концентраційного ланцюга
Рt(Н2) | НСІ(α1) | (НС1(α2) | Рt(Н2), φ1 φд φ2
в якому електрорушійна сила виникає за рахунок вирівнювання концентрації НС1 у напівелементах. Припустимо, що α1 > α2. В такому ланцюгу виникають дві електродні різниці потенціалів φ1 φ2 один дифузійний потенціал φд. Перші два потенціали виникають за рахунок різниці активностей НС1 в лівому і правому напівелементах і величина їх Розраховується за рівнянням
RT α2
E = φ2 - φ1 = ------- ln ------ ;
z F α1
Дифузійний потенціал φд, виникає таким чином.
Через межу розділу між двома розчинами справа наліво переміщуються іони гідроксонію Н3О+ і хлору Сl- , прагнучи зрівняти концентрацію в обох осередках. Перехід НС1 із разчину з більшою концентрацією в розчин з меншою концентрацією здійснюється дифузією іонів - катіона Н3О+ і аніона Сl- . Але іон Н3О+ є більш рухливим, ніж іон Сl- . Тому із самого початку іони Н3О+ дифундують через поверхню розділу в більшій кількості, ніж іони Сl- . Внаслідок цього виникає стрибок потенціалу, більш розведений розчин, куди перемістилися іони гідрогену, заряджається позитивно, а "відстаючі" іони хлору надають більш концентрованому розчину від'ємний заряд. Таким чином, на межі розділу двох розчинів виникає дифузійний потенціал, величина якого може бути розрахована за рівнянням Гендерсона:
lK - la RT α1
φд = --------- . ------ ln -----
lK + la z F α2
де lK - рухливість катіона, lа - рухливість аніона, z-величина заряду іона, F- стала Фарадея, α – активність іонів.
Останнє співвідношення показує, що дифузійний потенціал тим більший, чим більша різниця концентрацій (активностей іонів) розчинів і чим більша різниця в рухливостях іонів.
Величина дифузійних потенціалів, коли в напівелементах містяться розчини солей, не перевищує 3-5 мВ. Але у випадках, коли в напівелементах містяться розчини кислот і лугів, дифузійний потенціал стає значно більшим (порядку 25-75 мВ). Це пояснюється тим, що іони Н3О+ і ОН- мають значно більшу рухливість, ніж всі інші іони. З цього випливає, що при потенціометричних вимірах рН середовища дифузійні потенціали можуть вносити похибки.
З метою зменшення впливу дифузійного потенціалу на виміри, між розчинами різних концентрацій вміщують насичений розчин КCl. Сполучення електродних розчинів за допомогою проміжного розчину здійснюється через сифон, наповнений агар-агаром, настояним на концентрованому розчині однієї з вказаних солей. Оскільки рухливість іонів калію і хлору
приблизно однакова lк+ =73,5.10-4 м/с.В і lCl- =76,4- 10-4 м /с.В, то
дифузійний потенціал або зовсім не виникає, або має мінімальне значення.
В живих організмах дифузійний потенціал може виникати у випадках механічного пошкодження оболонок клітин. При цьому порушується вибірковість їх проникності і електроліти починають дифундувати з пошкоджених клітин у непошкоджені, що є причиною виникнення так званого потенціалу пошкодження, який може досягати величин порядку 30—40 мВ. Причому пошкоджена тканина заряджається від' ємно по відношенню до непошкодженої.
Мембранні потенціали. Потенціал дії.
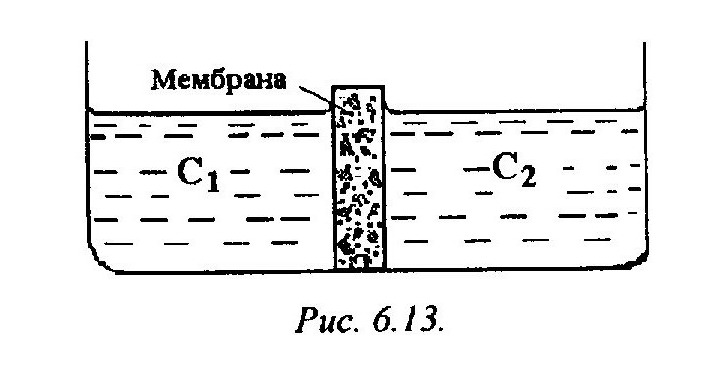
Дифузійний потенціал може значно зрости, якщо розчини електролітів різних концентрацій розділити спеціальною мембраною, яка є проникною тільки для іонів одного певного знака У більшості випадків виникнення мембранного потенціалу пов'язано з тим, що пори мембрани не відповідають розмірам іонів певного знака. В тканинах рослинних і тваринних організмів навіть в середині одної клітини виникають мембранні і дифузійні потенціали, які обумовлені хімічною і морфологічною неоднорідністю внутрішньоклітинного вмісту. Наявність різниці концентрацій іонів (с1 і с2) по обидва боки мембрани клітини приводить до виникнення мембранного потенціалу (рис. 6.13). Для окремого проникаючого іона X різниця потенціалів на мембрані може бути розрахована за рівнянням Нернста
RT c1 RT [ X]зовн.
φ1= -------- ln ------ = ------ ln ---------
z F c2 z F [ X]внутр.
де індекси вказують на внутрішню і зовнішню області клітини.
Як відомо, нервова клітина живих організмів складається з тіла клітини та одного довгого відростка діаметром 10 -7 10- 5 м, який називається аксоном. Клітина та аксон, що відходить від неї, оточені мембраною. Мембрани нервових клітин у стані спокою (незбудженому) приблизно у 100 разів більш проникні для іонів К+, ніж для Na+. Це означає, що між внутрішньою і зовнішньою сторонами клітинної стінки виникла різниця потенціалів у -75 мВ. Хоча клітинні мембрани у стані спокою приблизно у двічі більш проникні для іонів Сl-, ніж для іонів К+, іони Сl- відіграють другорядну роль у генерації мембранного потенціалу. На відміну від іонів К+ і Na+, іони Сl- не накачуються крізь мембрану проти градієнта концентрації. Крім того, від'ємно заряджена внутрішня поверхня клітинної стінки відштовхує аніони, що приводить до низької концентрації іонів Сl- у середині клітин. Таким чином, мембранний потенціал майже повністю визначається іонами К+.
Якщо нервову клітину збудити електрично, хімічно чи механічно, то клітинна мембрана стає більш проникною для іонів Nа+, ніж К+ (РNa + /РK+ ≈12). Це означає, що іони натрію почнуть рухатися всередину клітини, викликаючи зміну мембранного потенціалу. Таким чином, протягом дуже короткого часу (біля 1O-4 с) мембранний потенціал міняє свій знак і величину від -75 мВ до +50 мВ. Зміна знака заряду при русі іонів Nа+ всередину клітини деполяризує мембрану. Зразу після цих змін мембрана знов стає проникною для іонів K+ і непроникною для іонів Nа+. При рівновазі, (після того, як надлишок іонів Nа+ був "відкачаний" назовні з клітини) мембранний потенціал повертається до свого початкового значення. Раптова зміна мембранного потенціалу (підвищення і падіння) називається потенціалом дії. Такий приблизно механізм передачі збудження у нервових клітинах. В залежності від довжини аксона і інших факторів, швидкість передачі потенціала дії складає від 30 до 150 м/с. Як тільки потенціал дії видаляється з точки збудження клітини, мембрана в цій точці знову готова для збудження.
Потенціал дії розповсюджується по аксону до тих пір, поки не досягне синоптичного сполучення (області контакту між нервовими клітинами), або нервово-м'язового контакту. Прибуття потенціалу дії у синапсис запускає виділення нейротрансміттера, який являє собою невелику молекулу, що здатна проникати крізь мембрану. Такою молекулою може бути ацетилхолін, який з сінаптичних бульбашок дифундує до постсинаптичної мембрани, викликаючи в ній зміни проникності. Проникність мембрани для іонів К+ і Nа+ під дією ацетилхоліну різко зростає, що приводить до виникнення великого потоку іонів натрію всередину клітини і потоку іонів калію у зворотному напрямку. .Спрямований всередину потік іонів Nа+ знову деполяризує постсинаптичну мембрану і запускає потенціал дії у сусідньому аксоні. В решті-решт ацетилхолін гідролізується ферментом ацетилхолін-естеразою з утворенням оцтової кислоти і холіна:
O
║║
H3C – C – O - CH2 – CH2 – N – (CH3)3 + H2O
Ацетилхолін
O
HO - CH2 - CH2 - N - (CH3)3 + H+ + H3C
холін O
ацетат
Аналогічним шляхом потенціал дії, який генерується нервовою клітиною, може бути переданий в м'язову тканину. Наприклад, перед кожним ударом серця виникає великий потенціал дії, який створює певний струм. За допомогою електродів, розміщених на грудній клітці і підключених до самописця можна фіксувати потенціали дії. Такий запис потенціалів дії називається електрокардіограмою (ЕКГ), і має велике значення для діагностики захворювань серця.
Таким чином, мембранні та дифузійні потенціали виникають у клітинних та тваринних організмах і приводять до утворення різних біопотенціалів та біострумів.
