
- •Термохімія
- •Молекулярність і порядок реакції
- •Кінетика необоротних реакцій
- •Необоротна реакція першого порядку
- •Необоротна реакція другого поряду
- •3.1 Електрохімічні процеси та їхнє медико-біологїчне значення. Розчини електролітів.
- •3.3 Кондуктометричне визначення ступеня та константи йонізації слабкого електроліту. Закон розведення Оствальда.
- •3.4 Кондуктометричне титрування. Застосування кондуктометрії в медицині.
- •4.1 Електродні потенціали та механізм їх виникнення. Рівняння
- •4.3 Електрохімічні (гальванічні) елементи та електрорушійні сили.
- •4.4. Дифузійні та мембранний потенціали, їхнє біологічне значення. Рівняння Нернста.
- •4 .5 Потенціометрія: потенціометричне визначення рН за допомогою воднево-хлорсрібного та хлорсрібного скляного елемента. Потенціометричне титрування.
- •Ізотерма адсорбції Ленгмюра
- •5.2 Адсорбція на межі поділу рідина - газ та рідина - рідина. Рівняння Гіббса. Орієнтація молекул поверхнево-активних речовин у поверхневому шарі.
- •5.3 Уявлення про структуру біологічних мембран. Адсорбція на межі поділу тверде тіло - газ.
- •5.4 Адсорбція із розчину на поверхні твердого тіла. Фізична та хімічна адсорбція. Закономірності адсорбції розчинених речовин, парів та газів. Рівняння Фрейндліха.
- •6.1 Адсорбція електролітів: специфічна (вибірна) та йонообмінна. Правило Панета- Фаянса.
- •6.2. Йонообмінники природні та синтетичні. Роль адсорбції та йонного обміну в процесах життєдіяльності рослин і організмів.
- •6.3. Хроматографія. Класифікація хроматографічних методів аналізу за ознакою агрегатного стану фаз, техніки виконання та механізму розподілу. Адсорбційна, йонообмінна та розподільча хроматографія.
- •6.4. Застосування хроматографії в біології та медицині. (спрс)
- •7.1 Загальна характеристика дисперсних систем: основні визначення та класифікація.
- •7.3 Електричні властивості колоїдно-дисперсних систем: механізм утворення подвійного електричного шару. Рівняння Гельмгольца-Смолуховського. Електрофоретична рухливість.
- •7.4 Електрокінетичні явища: електроосмос, електрофорез, потенціали перебігу та седиментації. Застосування електрофорезу в дослідницькій та клініко-лабораторній практиці.(спрс)
- •8.1 Стійкість та коагуляція дисперсних систем. Коагуляція гідрофобних золів під дією електролітів. Поріг коагуляції. Правило Шульце—Гарді.
- •9.1 Високомолекулярні сполуки - основа живих організмів. Глобулярна та фібрилярна структура білків. Порівняльна характеристика розчинів високомолекулярних сполук, істинних та колоїдних розчинів.
- •9.3 Аномальна в'язкість розчинів вмс. В'язкість крові. Мембранна рівновага Доннана.
- •9.4 Ізоелекгричний стан білка. Ізоелєктрична точка та методи її визначення. Йонний стан біополімерів в водних розчинах.
- •9.5 Значення високомолекулярних сполук (вмс) у медицині та фармації. (спрс).
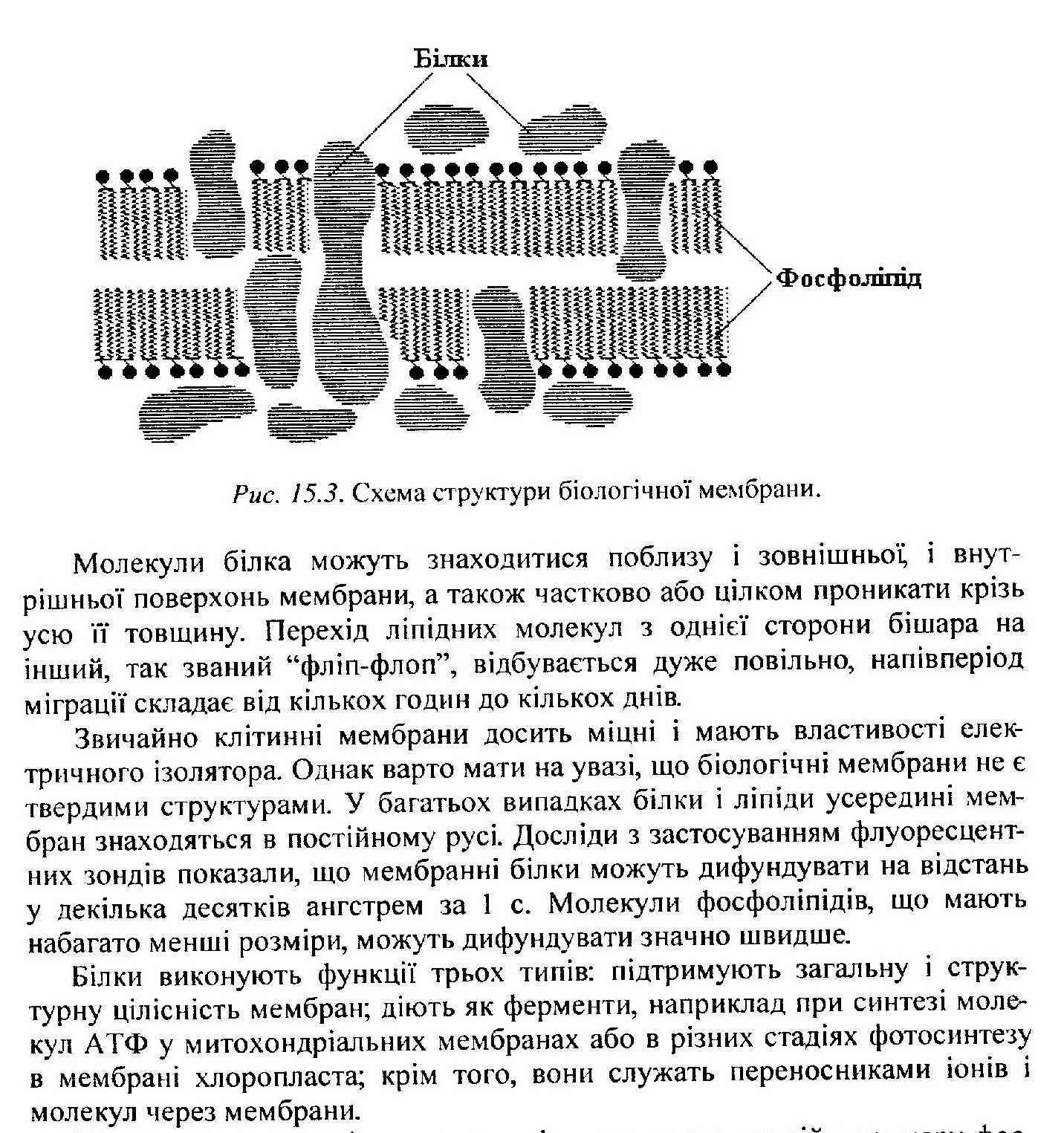
5.3 Уявлення про структуру біологічних мембран. Адсорбція на межі поділу тверде тіло - газ.




5.4 Адсорбція із розчину на поверхні твердого тіла. Фізична та хімічна адсорбція. Закономірності адсорбції розчинених речовин, парів та газів. Рівняння Фрейндліха.




Фізична та колоїдна хімія
Лекція № 6. Адсорбція електролітів. Хроматографія та її
застосування в біології й медицині
6.1 . Адсорбція електролітів: специфічна (вибірна) та йонообмінна. Правило Панета- Фаянса.
6.2. Йонообмінники природні та синтетичні. Роль адсорбції та йонного обміну в процесах життєдіяльності рослин і організмів.
6.3. Хроматографія. Класифікація хроматографічних методів аналізу за ознакою агрегатного стану фаз, техніки виконання та механізму розподілу. Адсорбційна, йонообмінна та розподільча хроматографія.
6.4. Застосування хроматографії в біології та медицині. (СПРС)
Самостійна робота : Застосування хроматографії в біології та медицині.
6.1 Адсорбція електролітів: специфічна (вибірна) та йонообмінна. Правило Панета- Фаянса.
Адсорбція електролітів твердими адсорбентами становить особливий інтерес через ту роль, яку вона грає в багатьох природних і штучно здійснюваних процесах. Важливо відзначити, що явище адсорбції електролітів лежить в основі таких процесів, як поглинання живильних речовин грунтом, надходження мінеральних речовин із грунту в клітини рослинних організмів, хімічна меліорація грунтів та ін. Адсорбція електролітів з розчинів відіграє важливу роль у багатьох явищах, що спостерігаються в колоїдних системах.
Адсорбція іонів твердими адсорбентами одержала назву полярної, або іонної адсорбції. Розрізняють кілька видів іонної адсорбції. Важливим і широко розповсюдженим видом іонної адсорбції є обмінна адсорбція Сутність обмінної адсорбції полягає в тім, що адсорбент поглинає з розчину іони одного знака, тобто або катіони, або аніони, причому це поглинання супроводжується переходом з адсорбенту в розчин іонів того ж знака.
Якщо адсорбованість якої-небудь речовини значно перевершує адсорбованість інших, то можна говорити про його виборчу адсорбцію даним адсорбентом. Ця обставина має надзвичайно велике практичне значення. Підбираючи потрібні адсорбенти, можна витягувати з складних сумішей строго певні речовини.
Одним з прикладів виборчої адсорбції є іонна. За правилом Панета-Фаянса на твердому адсорбенті переважно адсорбуються іони, що мають загальне з адсорбентом угрупування.
Так, на частинках ВаSО4, що утворюються при реакції Н2SО4 + ВаС12, адсорбуються або іони SО42-, або Ва2+, але не Н+ або Сl-.
Багатовалентні іони адсорбуються сильніше одновалентних. Рівновалентні іони також адсорбуються неоднаково у зв'язку з відмінностями в розмірах і ступені гідратації. По їх здібності до адсорбції вони розташовані в так звані ліотропні ряди.
Сs+ > Rb+ >K+> Nа+ >Li+.
СNS- > I- > Вr- > Сl-.
Аніони і катіони адсорбуються також не однаково. Викладені особливості іонної адсорбції мають дуже велике значення для процесів стабілізації і коагуляції колоїдів.
БІОЛОГІЧНЕ ЗНАЧЕННЯ ВИБІРКОВОСТІ АДСОРБЦІЇ
Важливо відзначити, що на одному і тому ж адсорбенті можуть бути активні центри з різною вибірковістю, тому одні речовини краще адсорбуватимуться на одних центрах, інші - на інших. Як приклад можна привести отруєння нікелю тіофеном: це приводить, до пригноблення каталітичного впливу нікелю на процес гідрування ароматичних ядер при збереженні колишньої дії на гідрування неграничних вуглеводнів. Очевидно, що два види каталізу - здійснюються різними активними центрами нікелю, на одному з яких вибірково адсорбується тіофен.
Явище вибірковості адсорбції має відношення до фактів різної адсорбованості токсинів і інших речовин різними тканинами і клітками. Так, наприклад, токсини збудників правця (стовбняк), ботулізму і ін. вражають перш за все клітки центральної нервової системи а токсини збудників дизентерії - вегетативну нервову систему; при висипному тифі вражаються переважно судини шкіри, мозку і частково серця і т.д.
Дуже високою вибірковістю володіють імунні білки (антитіла), що з'єднуються тільки із строго визначеними для кожного антитіла чужорідними білками (антигенами). Вивчення за допомогою електронного мікроскопа показало, що антитіла адсорбуються, наприклад, на поверхні черевнотифозних бактерій не рівномірно, а ділянками, як би по «активних центрах».
Введення в організм навіть невеликих кількостей отрут і токсинів, що володіють високою адсорбованістю на активних центрах деяких ферментів і інших, біологічно активних сполук, часто приводить до їх блокади. Так, введення в організм ціаністих сполук приводить до смерті через декілька секунд.
Для вибірковості адсорбції безперечне значення мають електричні заряди адсорбенту і адсорбтіва, оскільки різнойменно заряджені частинки легше з'єднуватимуться. Саме цим пояснюється хороша забарвлюваність лужних білків ядер кліток, заряджених в нейтральному середовищі позитивно, кислими (отріцательно- зарядженими) фарбами, а кислих білків протоплазми - основними (позитивно зарядженими) фарбами.
Нарешті, не можна не згадати про так звану адсорбційну терапію, що полягає у введенні хворому адсорбентів для поглинання шкідливих речовин. Так, часто застосовують карболен ( активоване вугілля) для скріплення отрут, токсинів, що потрапили в шлунково-кишковий тракт, а також для адсорбції тих, що накопичуються іноді в кишечнику газів (при метеоризмі).
