
- •Термохімія
- •Молекулярність і порядок реакції
- •Кінетика необоротних реакцій
- •Необоротна реакція першого порядку
- •Необоротна реакція другого поряду
- •3.1 Електрохімічні процеси та їхнє медико-біологїчне значення. Розчини електролітів.
- •3.3 Кондуктометричне визначення ступеня та константи йонізації слабкого електроліту. Закон розведення Оствальда.
- •3.4 Кондуктометричне титрування. Застосування кондуктометрії в медицині.
- •4.1 Електродні потенціали та механізм їх виникнення. Рівняння
- •4.3 Електрохімічні (гальванічні) елементи та електрорушійні сили.
- •4.4. Дифузійні та мембранний потенціали, їхнє біологічне значення. Рівняння Нернста.
- •4 .5 Потенціометрія: потенціометричне визначення рН за допомогою воднево-хлорсрібного та хлорсрібного скляного елемента. Потенціометричне титрування.
- •Ізотерма адсорбції Ленгмюра
- •5.2 Адсорбція на межі поділу рідина - газ та рідина - рідина. Рівняння Гіббса. Орієнтація молекул поверхнево-активних речовин у поверхневому шарі.
- •5.3 Уявлення про структуру біологічних мембран. Адсорбція на межі поділу тверде тіло - газ.
- •5.4 Адсорбція із розчину на поверхні твердого тіла. Фізична та хімічна адсорбція. Закономірності адсорбції розчинених речовин, парів та газів. Рівняння Фрейндліха.
- •6.1 Адсорбція електролітів: специфічна (вибірна) та йонообмінна. Правило Панета- Фаянса.
- •6.2. Йонообмінники природні та синтетичні. Роль адсорбції та йонного обміну в процесах життєдіяльності рослин і організмів.
- •6.3. Хроматографія. Класифікація хроматографічних методів аналізу за ознакою агрегатного стану фаз, техніки виконання та механізму розподілу. Адсорбційна, йонообмінна та розподільча хроматографія.
- •6.4. Застосування хроматографії в біології та медицині. (спрс)
- •7.1 Загальна характеристика дисперсних систем: основні визначення та класифікація.
- •7.3 Електричні властивості колоїдно-дисперсних систем: механізм утворення подвійного електричного шару. Рівняння Гельмгольца-Смолуховського. Електрофоретична рухливість.
- •7.4 Електрокінетичні явища: електроосмос, електрофорез, потенціали перебігу та седиментації. Застосування електрофорезу в дослідницькій та клініко-лабораторній практиці.(спрс)
- •8.1 Стійкість та коагуляція дисперсних систем. Коагуляція гідрофобних золів під дією електролітів. Поріг коагуляції. Правило Шульце—Гарді.
- •9.1 Високомолекулярні сполуки - основа живих організмів. Глобулярна та фібрилярна структура білків. Порівняльна характеристика розчинів високомолекулярних сполук, істинних та колоїдних розчинів.
- •9.3 Аномальна в'язкість розчинів вмс. В'язкість крові. Мембранна рівновага Доннана.
- •9.4 Ізоелекгричний стан білка. Ізоелєктрична точка та методи її визначення. Йонний стан біополімерів в водних розчинах.
- •9.5 Значення високомолекулярних сполук (вмс) у медицині та фармації. (спрс).
4.3 Електрохімічні (гальванічні) елементи та електрорушійні сили.
В гальванических (вольтовых) ячейках источник электрического тока — химическая реакция.
ЭЛЕМЕНТ ДАНИЭЛЯ
Рассмотренная ранее (см. рис. 13.1) цинк-медная пара в растворах их ионов — это элемент Даниэля; его э. д. с. равна 1,1 В.
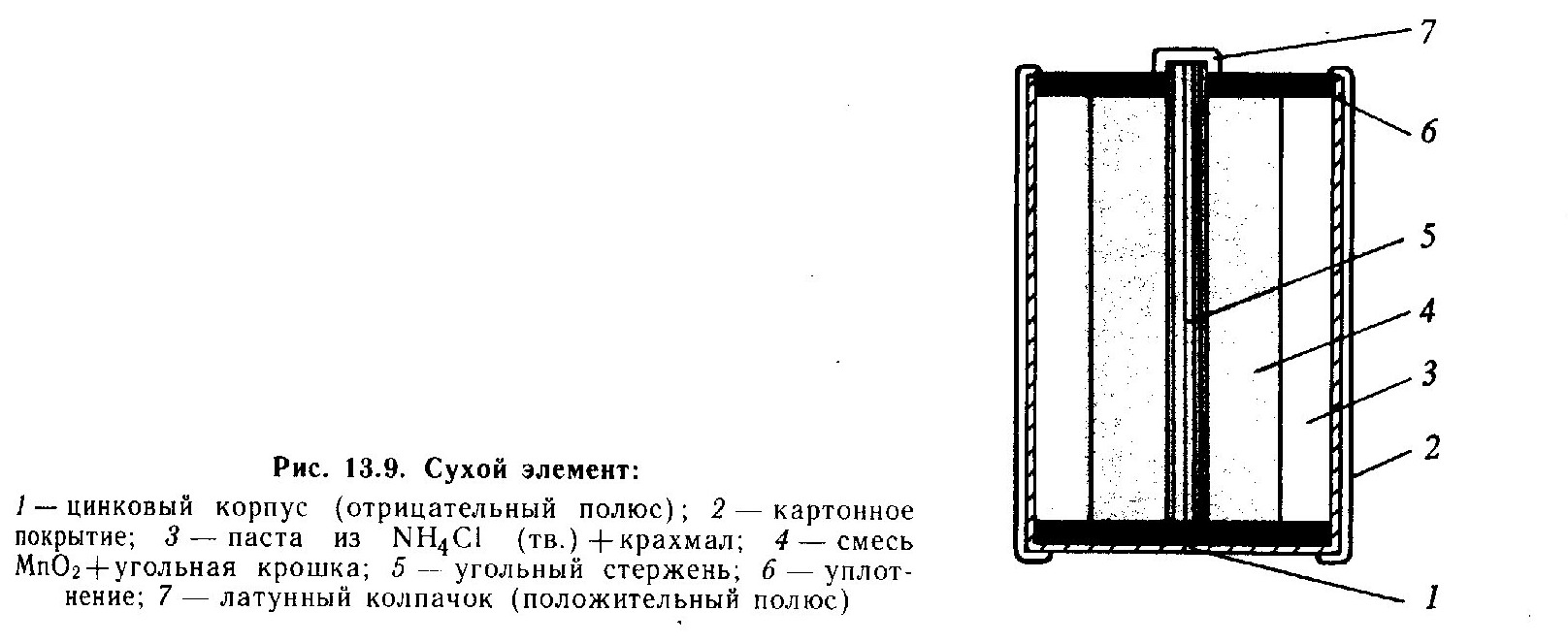
СУХИЕ ЭЛЕМЕНТЫ
Стремление преодолеть трудности, вызванные утечкой раствора электролита из таких элементов, как элемент Даниэля, послужило толчком к разработке сухих элементов. В последних электролит — это паста (рис. 13.9). Элементы подобного типа используют в радиотехнике; они служат источником питания в фотолампах-вспышках, часах. Их достоинство — портативность.
Э. д. с. элемента, приведенного на рис. 13.9, равна 1,5 В, а электродные реакции описываются уравнениями:
анод — Zn (тв.) → Zn2+ (водн.) + 2е- ;
катод — 2NН4+ (водн.) + 2е- → 2NН3 (г.) + 2Н2 (г.).
СВИНЦОВЫЙ АККУМУЛЯТОР
В этом элементе, в котором запасен (аккумулирован) электрический заряд, две свинцовые пластины погружены в 30 %-ный раствор серной кислоты, в результате чего они покрываются пленкой нерастворимого сульфата свинца (II).
Сначала аккумулятор необходимо зарядить, для чего через него пропускают постоянный электрический ток -
Заряд
положительная пластина — РbSО4 (тв.) + 2е- → Рb (тв.) + SО42- (водн.);
отрицательная пластина — РbSО4 (тв.) + 2Н2О (ж.) →
→ РbО2 (тв.) +4Н+ (вод.) +SО4 (вод.) +2е-.
В результате пропускания электрического тока пластины становятся химически различными; следовательно, различными делаются и их потенциалы, так что при соединении пластин между ними начинает течь электрический ток. Происходит раз-
ряд, т. е. аккумулятор становится поставщиком электрического тока —
Разряд
отрицательная пластина — Рb (тв.) + SО4- (вод.) → РbSО4 (тв.) + 2е-;
положительная пластина — 2РbО2 (тв.) + 4Н+ (водн.) + SО4- (водн.) + 2е- →
→ РbSО4 (тв.) + 2Н2О (ж.).
Элемент перестает быть источником электрического тока, когда вся РbO2 и весь Рb превращаются в РbSО4, т. е. когда пластины перестают различаться.
Из приведенного следует, что Рb-пластина заряжается положительно в процессе зарядки и отрицательно в процессе разрядки. Полярность РbO2-пластины также меняется — от отрицательной при разрядке до положительной при зарядке. Суммарную
реакцию можно описать уравнением:
заряд
Рb(тв.) + РbО2(тв.) + 2Н2SО4(водн.) 2РbSО4(тв.) + 2Н2О(ж.).
Разряд
Автомобильный аккумулятор состоит из шести соединенных вместе свинцовых ячеек; его э. д. с. равна 12 В. При движении автомобиля аккумулятор заряжается через генератор. При частых остановках и включениях стартера аккумулятор теряет заряд, «садится». Тогда его приходится заряжать постоянным электрическим током. Разрядка аккумулятора приводит к «истощению» электролита, т. е. к уменьшению плотности серной кислоты. За состоянием электролита и, следовательно, аккумулятора, следят при помощи ареометра.
