
- •Содержание
- •2 Лабораторные работы
- •2. 1 Титриметрический анализ, химическая посуда
- •Способы выражения концентрации растворов
- •Химическая посуда
- •Контрольные вопросы:
- •2. 2 Дисперсные системы и электрокинетические явления
- •Двойной электрический слой.
- •Электрокинетические явления.
- •Цель работы.
- •Приборы и реактивы
- •Выполнение работы.
- •Обработка результатов.
- •Контрольные вопросы.
- •2. 3 Коагуляция и седиментация.
- •Цель работы:
- •Приборы и реактивы
- •Выполнение работы.
- •Обработка результатов.
- •Контрольные вопросы.
- •2. 4 Определение критической концентрации мицеллообразования. Поверхностно-активные вещества, классификация.
- •Адсорбция на границе раздела фаз.
- •Мицеллообразование
- •Гидрофильно-липофильный баланс
- •Солюбилизация.
- •Методы определения ккм
- •Цель работы:
- •Приборы и реактивы:
- •Выполнение работы
- •Обработка результатов
- •Контрольные вопросы.
- •2. 5 Расчет параметров кристаллической решетки сдг
- •Цель работы:
- •Выполнение работы
- •Обработка результатов
- •Контрольные вопросы.
- •3 Примеры решения задач по теме «Неорганические мицеллы»
- •3.1 Задачи на выпадение осадка (Произведение растворимости)
- •3.2 Задачи на определение формулы мицеллы
- •3.3 Задачи для самостоятельного решения:
- •4 Темы для самостоятельного изучения
- •4.1 Адсорбция.
- •Уравнение изотермы адсорбции Ленгмюра (Лэнгмюра)
- •Уравнение изотермы адсорбции Фрейндлиха
- •Теория полимолекулярной адсорбции Поляни (1915)
- •Уравнение изотермы адсорбции бэт
- •Контрольные вопросы.
- •4.1 Анализ твердой поверхности на содержание кислотно-основных центров
- •Контрольные вопросы:
- •4.3 Жидкие кристаллы
- •Контрольные вопросы:
- •5 Вопросы к аттестационному тестир
- •5.1 По предмету «Физикохимия наночастиц и наноматериалов»
- •5.2 По предмету «Физикохимия наноструктурированных материалов»
- •Приложение Лабораторный журнал
Цель работы:
Рассчитать параметры a и с слоистых гидроксидов по данным дифрактограммам. Сравнить данные полученные разными методами.
Выполнение работы
Получить у преподавателя индивидуальный вариант набора дифрактограмм СДГ. Рассчитать параметры a и с слоистых гидроксидов по данным дифрактограммам. Параметр с рассчитать двумя способами: по формуле (1) и (2), (3), с учетом n=1, λ = 1,542. Рассчитать относительную погрешность расчетов.
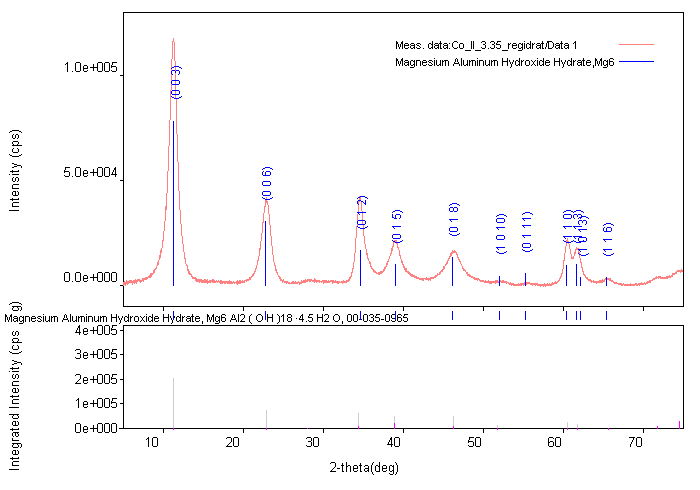
2-theta (deg) |
Height (cps) |
Int. I(cpsҐdeg) |
11.241(4) |
77339(568) |
138672(249) |
22.884(6) |
26843(334) |
50263(158) |
28.06(5) |
997(64) |
3151(180) |
34.368(4) |
26357(331) |
42118(172) |
38.851(12) |
12436(228) |
35598(211) |
46.224(15) |
9815(202) |
34302(213) |
51.75(9) |
888(61) |
11316(1824) |
60.452(8) |
14106(242) |
18937(357) |
61.711(11) |
10193(206) |
14127(318) |
65.61(3) |
1733(85) |
3329(78) |
71.79(8) |
2331(99) |
8868(32965) |
74.55(12) |
4015(129) |
22006(40491) |
Обработка результатов
Результаты измерений записывают в виде таблицы:
Таблица.
Параметры кристаллической решетки c и а слоистых гидроксидов.
№п/п |
Образец СДГ (формула) |
c1, нм |
c2, нм |
|
а, нм |
1. |
|
|
|
|
|
2. |
|
|
|
|
|
3. |
|
|
|
|
|
Контрольные вопросы.
Дайте определения терминов: «слоистые двойные гидроксиды», «гидроталькит», «эффект памяти».
Какова кристаллическая решетка гидроталькитоподобных соединений?.
Как производят идентификацию слоистой структуры СДГ.
Как рассчитывают параметры кристаллической решетки СДГ.
Перечислите области применения СДГ.
3 Примеры решения задач по теме «Неорганические мицеллы»
3.1 Задачи на выпадение осадка (Произведение растворимости)
Растворимость, выражается в моль/л или в г/л, показывает сколько вещества растворено в одном литре.
Ионное произведение (ИП) – произведений молярных концентраций ионов, на которые диссоциирует данное вещество, взятых в степени соответствующей количеству данных ионов в исходной молекуле (равно индексу при ионе).
CaSO4 ↔ Ca2+ + SO42-
Растворимость: s s s
ИП(CaSO4 ) = [Ca2+][SO42-] = s2
CaCl2 ↔ Ca2+ + 2 Cl–
Растворимость: s s 2 s
ИП(CaCl2 ) = [Ca2+][Cl–]2 = s·(2s)2 = 4s3
AlCl3 ↔ Al3+ + 3 Cl–
Растворимость: s s 3 s
ИП(AlCl3 ) = [Al3+][Cl–]3 = s·(3s)3 = 27s4
Al2(SO4)3 ↔ 2 Al3+ + 3 SO42-
Растворимость: s 2 s 3 s
ИП(Al2(SO4)3 ) = [Al3+]2 [SO42-]3 = (2s)2·(3s)3 = 4·27s5 = 108 s5
Произведение растворимости (ПР) – ионное произведение для насыщенного раствора, т.е. раствора, находящегося в равновесии над осадком. Является постоянной величиной для данного соединения при данных условиях. Существуют таблицы в которых приведены данные о максимальной растворимости и ПР для труднорастворимых веществ.
Если ионное произведение больше произведение растворимости, вещество выпадает в осадок.
Пример 1. Выпадает ли осадок при смешении раствора хлорида кальция объемом 20 мл и концентрацией 0,02 М и раствора сульфата натрия объемом 30 мл и концентрацией 0,003М.
CaCl2 |
+ |
Na2 SO4 |
↔ |
2 NaCl |
+ |
CaSO4 |
|
0,02 моль/л |
|
0,003 моль/л |
|
|
|
ПР=9,1·10-8 |
|
20мл=0,02л |
|
30мл=0,03л |
|
|
|
|
|
1) Найдем
количество вещества хлорида кальция:
![]() (моль).
(моль).
2) Объем
раствора после смещения:
![]() (л).
(л).
3) Найдем концентрацию хлорида кальция после смешения двух растворов:
![]() (моль/л).
(моль/л).
4) Найдем
количество вещества сульфата натрия:
![]() (моль).
(моль).
5) Найдем концентрацию сульфата натрия после смешения двух растворов:
![]() (моль/л).
(моль/л).
6)
Концентрация ионов кальция равна
концентрации хлорида кальция:
![]() моль/л, а концентрация сульфат-ионов
равна концентрации сульфата натрия:
моль/л, а концентрация сульфат-ионов
равна концентрации сульфата натрия:
![]() (моль/л).
(моль/л).
7) Ионное
произведение сульфата кальция:
![]()
![]()
8) 1,44·10-5 > 9,1·10-8 , т.е. ИП>ПР, и следовательно осадок выпадает.
Ответ: осадок выпадает
Пример 2. Выпадает ли осадок при добавлении в раствор хлорида кальция объемом 20 мл и концентрацией 0,02 М навески сульфата натрия массой 0,0015 г.
CaCl2 |
+ |
Na2 SO4 |
↔ |
2 NaCl |
+ |
CaSO4 |
|
0,02 моль/л |
|
0,0015 г |
|
|
|
ПР=9,1·10-8 |
|
20мл=0,02л |
|
|
|
|
|
|
|
1) Найдем
количества вещества сульфата натрия:
![]() (моль).
(моль).
2) Найдем
концентрацию сульфата натрия:
![]() (моль/л).
(моль/л).
3)
Концентрация ионов кальция равна
концентрации хлорида кальция:
![]() моль/л, концентрация сульфат-ионов равна
концентрации сульфата натрия:
моль/л, концентрация сульфат-ионов равна
концентрации сульфата натрия:
![]() (моль/л).
(моль/л).
4) Ионное
произведение сульфата кальция:
![]()
8) 1,06·10-5 > 9,1·10-8 , т.е. ИП>ПР, и следовательно осадок выпадает.
Ответ: осадок выпадает
Пример 3. Навеску 0,058 г одноводного сульфата лития растворили в 35 мл воды, выпадет ли осадок при добавлении 55 мл 0,001М карбоната натрия.
Na2CO3 |
+ |
Li2 SO4 |
↔ |
Na2 SO4 |
+ |
Li2 CO3 |
0,001моль/л |
|
m(Li2 SO4·Н2О)=0,058г |
|
|
|
ПР=1,9·10-3 |
55мл=0,055л |
|
35мл=0,035л |
|
|
|
|
1) Найдем
количество кристаллогидрата одноводного
сульфата лития:
![]() (моль).
(моль).
2)
Количество лития:
![]() (моль).
(моль).
3) Общий
объем после смешения двух растворов:
![]() (л).
(л).
4)
Концентрация ионов лития в образовавшемся
после смешения растворе:
![]() (моль/л).
(моль/л).
5) Найдем
количество вещества карбоната натрия:
![]() (моль).
(моль).
6)
Концентрация карбоната натрия
образовавшемся после смешения растворе:
![]() (моль/л).
(моль/л).
7)
Концентрация сульфат-ионов:
![]() (моль/л).
(моль/л).
8) Ионное
произведение: ИП карбоната лития:
![]() .
.
9) ИП < ПР, т.к. 6,1·10-8 < 1,9·10-3, следовательно, осадок не выпадает.
Ответ: осадок не выпадает
Пример 4. Выпадает ли осадок при смешении 0,2% раствора хлорида кальция объемом 20 мл, плотностью 1,1г/мл и раствора сульфата натрия объемом 30 мл и концентрацией 0,001М.
CaCl2 |
+ |
Na2 SO4 |
↔ |
2 NaCl |
+ |
CaSO4 |
|
0,02%=2·10-4 |
|
0,001 моль/л |
|
|
|
ПР=9,1·10-8 |
|
20мл=0,02л |
|
30мл=0,03л |
|
|
|
|
|
|
|
|
|
|
|
|
|
1) Найдем
молярную концентрацию хлорида кальция:
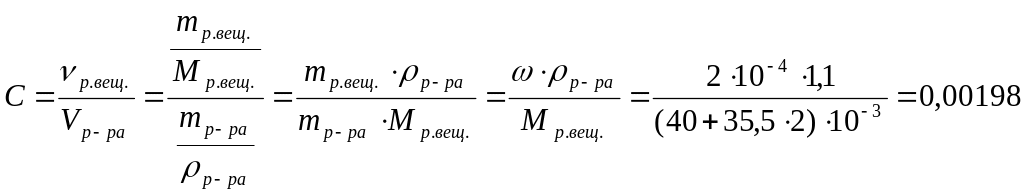 (моль/л).
(моль/л).
Проверка
размерности:
![]()
2) Объем раствора после смещения: (л)
3) Найдем
количества вещества хлорида кальция:
![]() (моль).
(моль).
4) Найдем концентрацию хлорида кальция после смешения двух растворов:
![]() (моль/л).
(моль/л).
4) Найдем
количество вещества сульфата натрия:
![]() (моль).
(моль).
5) Найдем концентрацию сульфата натрия после смешения двух растворов:
![]() (моль/л).
(моль/л).
6)
Концентрация ионов кальция равна
концентрации хлорида кальция:
![]() моль/л, а концентрация сульфат-ионов
равна концентрации сульфата натрия:
моль/л, а концентрация сульфат-ионов
равна концентрации сульфата натрия:
![]() моль/л.
моль/л.
7) Ионное
произведение сульфата кальция:
![]()
8) 5·10-7 > 9,1·10-8 , т.е. ИП>ПР, и следовательно осадок выпадает.
Ответ: осадок выпадает
Пример 5. Выпадает ли осадок при добавлении 7·10-6г карбоната натрия к насыщенному раствору сульфита кальция, объемом 60мл.
Na2CO3 |
+ |
Сa SO3 |
↔ |
Ca CO3 |
+ |
Na2 SO3 |
7·10-5г |
|
ПР=3,2·10-7 |
|
ПР=3,8·10-9 |
|
|
|
|
60 мл=0,06 л |
|
|
|
|
1) Найдем
количество Na2CO3:
![]() (моль).
(моль).
2) Найдем
молярную концентрацию Na2CO3:
![]() (моль/л).
(моль/л).
3) Найдем растворимость (s) сульфита кальция: ПР (Сa SO3) = [Сa2+]∙[SO32–]=s2.
![]() (моль/л).
(моль/л).
4) Найдем
ионное произведение Ca
CO3. Концентрация
ионов кальция равна концентрации Сa
SO3, а концентрация
карбонат-ионов равна концентрации
Na2CO3.
![]() .
.
5) 6,2∙10-9 > 3,8·10-9 , т.е. ИП>ПР, и следовательно осадок выпадает.
Ответ: осадок выпадает.
Пример 5. Определить массу ионов серебра в 280 мл насыщенного раствора хромате серебра. ПР (Ag2CrO4)= 1,1·10-12.
1) Если растворимость хромата серебра – s,
Ag2CrO4 |
↔ |
2 Ag+ |
+ |
CrO42– |
s |
|
2s |
|
s |
концентрация серебра [Ag+]=2s, хромат-иона [CrO42–]=s.
2)
ПР (Ag2CrO4)=
[Ag+]∙[CrO42–]
= (2s)2∙s
= 4s3.
![]() (моль/л).
(моль/л).
3) Концентрация серебра: [Ag+] = 2s = 2∙6,5∙10-5 = 13∙10-5 = 1,3∙10-4 (моль/л).
4)
Количество вещества ионов серебра:
![]() (моль).
(моль).
5) Масса
ионов серебра:
![]() (г).
(г).
Или 3,93 мг
Ответ: 3,93мг.
