
- •Моделирование и применение эвм в химической технологии
- •Часть 1
- •Введение
- •1 Организация выполнения и требования к оформлению лабораторных работ
- •2 Отладка программы в интегрированной среде
- •3 Лабораторные работы
- •3.1 Расчет ячеечного реактора
- •3.1.1 Постановка задачи
- •3.1.2 Вывод математического описания
- •3.1.3 Условия однозначности
- •3.1.4 Выбор метода реализации
- •3.1.5 Блок – схема реализации
- •3.1.6 Идентификация переменных
- •3.1.7 Варианты заданий
- •3.2 Расчет теплообменника
- •3.2.1 Постановка задачи
- •3.2.2 Вывод математического описания
- •3.2.3 Условия однозначности
- •3.2.4 Выбор метода реализации
- •3.2.5 Блок – схема реализации
- •3.2.6 Идентификация переменных
- •4.7 Варианты заданий
- •3.3 Расчет подогревателя
- •3.3.1 Постановка задачи
- •3.3.2 Вывод математического описания
- •3.3.3 Условия однозначности
- •3.3.4 Выбор метода реализации
- •3.3.5 Блок – схема реализации
- •3.3.6 Идентификация переменных
- •3.3.7 Варианты заданий
- •3.4 Расчет изоляции
- •3.4.1 Постановка задачи
- •3.4.2 Вывод математического описания
- •3.4.3 Условия однозначности
- •3.4.4 Выбор метода реализации
- •3.4.5 Блок – схема реализации
- •3.4.6 Идентификация переменных
- •3.4.7 Варианты заданий
- •7 Расчет насадочного абсорбера
- •7.1 Постановка задачи
- •3.5.2 Вывод математического описания
- •3.5.3 Условия однозначности
- •3.5.4 Выбор метода реализации
- •3.5.7 Варианты заданий
- •3.6 Расчет тарельчатого абсорбера
- •3.6.1 Постановка задачи
- •3.6.2 Вывод математического описания
- •3.6.3 Условия однозначности
- •3.6.4 Выбор метода реализации
- •3.6.7 Варианты заданий
- •3.7 Расчёт ректификационной колонны
- •3.7.1 Постановка задачи
- •3.7.2 Вывод математического описания
- •3.7.3 Условия однозначности
- •3.7.4 Выбор метода реализации
- •3.7.5 Блок – схема реализации
- •3.7.6 Идентификация переменных
- •3.7.7 Варианты заданий
- •Зарезервированные слова turbo pascal 7.0
- •Клавиши быстрого управления среды
3.1.2 Вывод математического описания
Математическое описание для нестационарных условий проведения процесса имеет вид:
![]() (1)
(1)
где Ri,j – суммарная скорость по j-му компоненту в i-м реакторе;
n – количество реакторов в каскаде;
m – количество реагирующих веществ.
Допустим, в каскаде реакторов в изотермических условиях протекает химическая реакция:
 А
к1
В к2
С
А
к1
В к2
С
Необходимо для установившегося режима определить количество реакторов в каскаде, при котором выход продукта В был бы максимальным, а выход побочного продукта С возможно меньшим.
Для данного химического процесса в стационарных условиях работы математическое описание будет иметь вид:
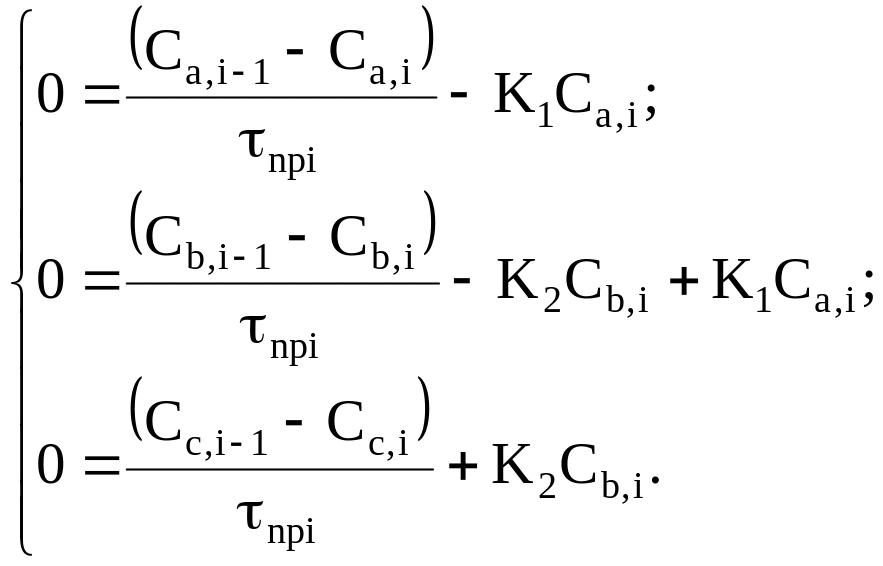 (2)
(2)
Преобразуем систему (2), разделив дроби почленно:
![]() (3)
(3)
Решаем эту систему относительно концентраций реагирующих веществ:
 (4)
(4)
Таким образом может быть вычислена концентрация реагирующих веществ вначале в первом реакторе, а затем во втором и т.д. Сравнивая концентрацию компонента В в очередном реакторе с концентрацией в предыдущем можно найти такое количество реакторов в каскаде, при котором выход продукта В будет наибольшим. Варьируя величиной констант K1 и K2, а также временем пребывания (τпр i) в реакторах каскада, можно провести исследования работы ячеечной модели и найти наилучший вариант работы.
Систему линейных уравнений (3) можно решить методом Гаусса, но для этого надо привести её к виду:
A · X = B, (5)
где А – двумерный массив коэффициентов при неизвестных;
Х – одномерный массив текущих концентраций;
В – одномерный массив свободных членов.
![]() (6)
(6)
Сгруппируем слагаемые, содержащие одинаковые концентрации и получим:
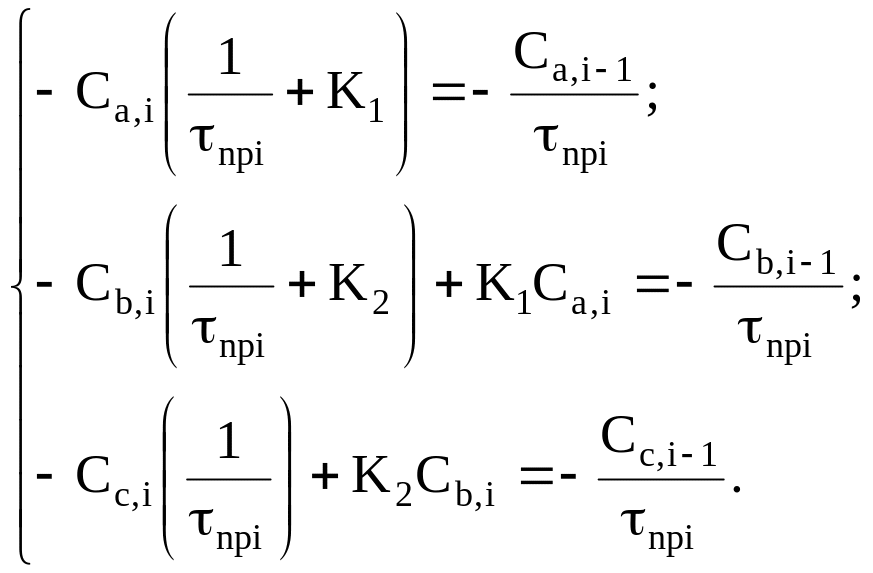 (7)
(7)
Представим полученную систему линейных уравнений в виде табл. 3.1.
Таблица 3.1 – Таблица массивов
Массив А |
Массив В |
Массив Х |
||
Ca |
Cb |
Cc |
||
|
0 |
0 |
|
Ca,i |
K1 |
|
0 |
|
Cb,i |
0 |
K2 |
|
|
Cc,i |
3.1.3 Условия однозначности
Для „привязки” математического описания к реальному объекту необходимо определить значения многих переменных, в соответствии с конструкцией конкретного аппарата и условиями его работы. Для этих целей используют условия однозначности (УО), состоящие из:
Начальные условия характеризуют значения технологических параметров в начальный момент времени (при τ=0) в любой точке объекта. При этом значение технологических параметров зависит от способа запуска или останова объекта. Так, например, если перед началом работы ячеечный реактор был заполнен реакционной смесью и в момент времени τ=0 созданы условия для протекания реакции (например, температурные условия), то распределение концентраций будет следующим:
Сa(τ=0, х=0) = 100 % Сa(τ=0, х>0) = 100 %
Cb(τ=0, х=0) = 0 % Cb(τ=0, х>0) = 0 %
Cc(τ=0, х=0) = 0 % Cc(τ=0, х>0) = 0 %
Если же вначале аппарат был пуст, а в момент времени τ=0 в него подали реакционную смесь и создали условия для протекания реакции, то распределение концентраций будет следующим:
Сa(τ=0, х=0) = 100 % Сa(τ=0, х>0) = 0 %
Cb(τ=0, х=0) = 0 % Cb(τ=0, х>0) = 0 %
Cc(τ=0, х=0) = 0 % Cc(τ=0, х>0) = 0 %
Граничные условия первого рода (ГУ-I) характеризуют значение технологических параметров на границах объекта в любой момент времени:
Сa(τ, х=0) = 100 % Сa(τ, х=L) = 0 %
Cb(τ, х=0) = 0 % Cb(τ, х=L) = 0 %
Cc(τ, х=0) = 0 % Cc(τ, х=L) = 0 %
где (х=L) определяет координату выхода из аппарата.
Граничные условия второго рода (ГУ-II) определяют значения плотностей потоков масс или энергии на границах объекта, характеризующихся соответственно законами Фика и Фурье:
qD
= -D![]() ,
qλ
= -
,
qλ
= -![]() ,
,
где D – коэффициент диффузии, м/с ;
λ – коэффициент теплопроводности, м2 ºС/м.
,
![]() –
соответственно градиенты концентраций
и температур.
–
соответственно градиенты концентраций
и температур.
Для рассматриваемого процесса в связи с отсутствием градиента ГУ-II не имеют смысла.
Граничные условия третьего рода (ГУ-III) определяют равенство плотностей потоков масс или энергии на границах раздела двух разнородных фаз (см. рис. 3.2).
Как известно, на границе соприкосновения фаз возникает псевдонеподвижный слой теплоносителя или газа в абсорбере (приведенный слой). Внутри этого слоя тепло или масса передаются на молекулярном уровне (теплопроводностью или диффузией):
qD = -D , qλ = -
В движущемся слое перенос тепла или массы происходит на молярном уровне по закону Ньютона (плотность потока пропорциональна движущей силе):
qβ = β(С-С*), qα = α(t-tпл)
При равенстве потоков можно записать:
D = β(С- С*), = α(t- tпл) ,
где С* и tпл –значение концентрации и температуры в приведенной пленке.
Граничные условия третьего рода позволяют получить при формальном делении правой части равенства на левую безразмерное соотношение (число Нуссельта), показывающее соотношение интенсивностей конвективного и кондуктивного переноса тепла. Следовательно, число Нуссельта также может быть отнесено к граничным условиям третьего рода. Для данного процесса в связи с отсутствием процесса массопереноса ГУ-III не имеют смысла.
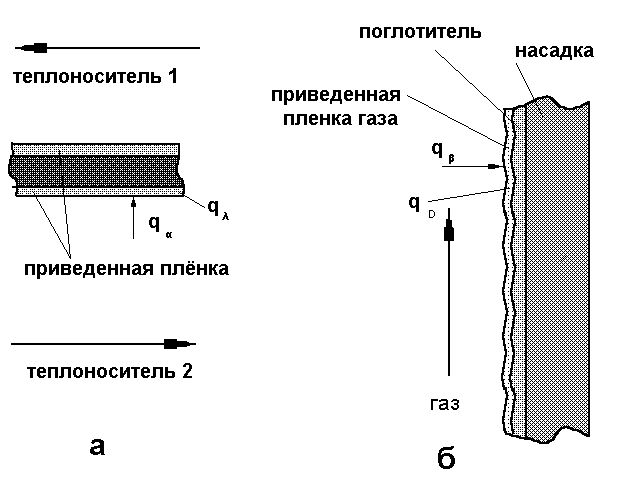
Рис 3.2. – Иллюстрация к граничным условиям третьего рода (а – теплообменные процессы; б – массообменные процессы).
Граничные условия четвертого рода (ГУ-IV) характеризуются равенством плотностей потоков массы или энергии на границе раздела двух одинаковых фаз (газ-газ, жидкость-жидкость, твердое-твердое), передаваемых на молекулярном уровне. Форма записи ГУ-IV следующая:
D1 1 = D2 2, λ1 dt1 /dx = λ2 dt2 /dx.
Для рассматриваемого процесса ГУ-IV не имеют смысла.
Геометрические условия задают размеры аппарата и отдельных его элементов (диаметр сечения, по которому движется поток технологического вещества, длина пути, размеры трубок, насадки и т.д. и т.п.).
Теплофизические условия определяют свойства технологических веществ: плотности (кг/м3), теплоемкости (Дж/кг град), теплопроводности (Дж/(м2 град/м)), коэффициенты диффузии (м2/с) и т.д.
Кинетические условия определяют линейные скорости движения технологических веществ, массовые и объемные скорости, коэффициенты скоростей процессов (коэффициенты тепло- и массообмена, коэффициенты скоростей химических реакций и т.д.).
