
- •Методические указания
- •Редактор н.Е. Гладких
- •Молекулярная физика и термодинамика
- •Основные положения молекулярно-кинетической теории идеального газа
- •2. Экспериментальные газовые законы
- •3. Уравнение состояния газа (уравнение Менделеева-Клапейрона):
- •Первое начало термодинамики
- •5. Примеры решения задач по молекулярной физике и термодинамике
МУ к практическим занятиям
1. Кинематика и динамика поступательного и вращательного движения. – Павлов
1.13, 1.14., 1.26, 1.39, 1.47, 1.153
2. Механические колебания и волны. – Мощенко
4.3, 4.25, 4.28, 4.118
3. Механика жидкости. – Ларина
1.214, 1.225, 1.229, 1.231
4. Молекулярная физика и термодинамика. – Снежков
2.7, 2.15, 2.30, 2.54, 2.58, 2.61
5. Электростатика и электромагнетизм. – Гольцов
3.10, 3.17, 3.75, 3.120, 3.143, 3.179
6. Геометрическая и волновая оптика. – Чебанова
5.7, 5.29, 5.45, 5.68, 5.88
7. Корпускулярные свойства света и тепловое излучение. – Чебанова
5.200, 5.212, 5.228, 5.178
8. Физика атома и атомного ядра. – Бугаян
6.5, 6.11, задачи 1, 2, 3 со стр. 351 (примеры решения задач)
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РОССИЙСКОЙ ФЕДЕРАЦИИ
ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ
ВЫСШЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ
«РОСТОВСКИЙ ГОСУДАРСТВЕННЫЙ СТРОИТЕЛЬНЫЙ УНИВЕРСИТЕТ»
Утверждено
на заседании кафедры физики
08 февраля 2012 г.
Методические указания
к практическим занятиям
«Молекулярная физика и термодинамика»
Методические указания для всех специальностей и
для всех профилей всех направлений бакалавриата
очной и заочной форм обучения
Ростов-на-Дону
2012
УДК 531.383
Методические указания к практическим занятиям «Кинематика и динамика поступательного и вращательного движения». – Ростов н/Д: Рост. гос. строит. ун-т, 2012. – 6 с.
Методические указания содержат краткую теорию по молекулярной физике и термодинамике, в качестве пояснений к решению серии задач данного раздела физики.
Методические указания основаны на учебном пособии «Курс физики» и на «Сборнике задач по курсу физики» Т.И. Трофимовой (изд-во Высшая школа), соответствующих действующей программе курса физики для всех специальностей и для всех профилей всех направлений бакалавриата.
Предназначены для проведения практического занятия «Молекулярная физика и термодинамика» по программе курса физики для студентов всех специальностей и всех профилей всех направлений бакалавриата очной и заочной форм обучения.
УДК 531.383
Составитель проф. А.Н. Павлов
Рецензент доц. Ю.И. Гольцов
Редактор н.Е. Гладких
Темплан 2012 г., поз. ___
Подписано в печать ____). Формат 60х84 1/16. Бумага писчая. Ризограф. Уч.-изд.л 0,5. Тираж 100 экз. Заказ
Редакционно-издательский центр
Ростовского государственного строительного университета.
334022, Ростов-на-Дону, ул. Социалистическая, 162
© Ростовский государственный
строительный университет, 2012
Молекулярная физика и термодинамика
Молекулярная физика и термодинамика изучают закономерности тепловой формы движения материи на основе ее молекулярного строения, взаимодействия и движения большой совокупности частиц.
В основе термодинамики лежат фундаментальные законы или принципы, установленные на основании обобщения опытных фактов. Первый закон устанавливает количественные превращения энергии из одного вида в другие, второй определяет условия этих превращений.
Основные положения молекулярно-кинетической теории идеального газа
Физические тела имеют дискретное строение. Они состоят из частиц
(молекул, атомов, ионов). Для измерения количества вещества введена единица, которая называется молем. Моль – это количество однородного вещества, которое содержит столько же молекул, сколько содержится атомов в 0,012 кг углерода. Число NА молекул или атомов в моле любого вещества называют постоянной Авогадро: NА = 6,023∙1023 моль-1.
□ Масса одного моля вещества называется молярной массой. Обозначается буквой М и равна произведению массы mМ молекулы данного вещества на постоянную Авогадро: М = mM NA. Масса m любого количества вещества в теле m = nM, где n = m/M - число молей.
□ Объем одного моля вещества называется молярным объемом. Если обозначить молярный объем VM, тогда объем тела V = mVM/M.
Частицы находятся в непрерывном беспорядочном движении, что
доказывают явления диффузии и броуновского движение. Броуновское движение – это беспорядочное движение нерастворимых твердых частиц малых размеров (≈ 10-6) в жидкости или газе.
Между частицами происходит взаимодействие, которое характеризуется
силами притяжения и силами отталкивания.
□ Идеальный газ – это такая модель газа, в которой не учитывают размеры молекул, их взаимодействие, а столкновение молекул рассматривают как абсолютно упругий удар.
□ Основное уравнение молекулярно – кинетической теории газа устанавливает зависимость между давлением газа на стенки сосуда и средней кинетической энергией движения молекул.
Физическую величину, равную отношению силы F, действующей перпендикулярно поверхности, к площади этой поверхности S, называют давлением p: p = F/S. За единицу давления, принимают такое давление, которое производит сила 1 Н на 1 м2. Единица давления 1 Н/м2 называется паскалем. 1 Па = 1 Н/м2. □ Давление идеального газа зависит от концентрации молекул n и их средней кинетической энергии ‹eк› молекул:
р = ⅔ n‹eк› = ⅔ n m‹v2› /2,
![]() где
концентрация n
молекул – это отношение числа всех
молекул к занимаемому ими объему V:
n
= N/V;
‹eк›
- средняя кинетическая энергия хаотического
поступательного движения одной молекулы.
□ средняя
квадратичная скорость молекул: ‹vкв›
=
где
концентрация n
молекул – это отношение числа всех
молекул к занимаемому ими объему V:
n
= N/V;
‹eк›
- средняя кинетическая энергия хаотического
поступательного движения одной молекулы.
□ средняя
квадратичная скорость молекул: ‹vкв›
= ![]() =
= ![]() ;
R
= 8,31 Дж/(моль∙К) -
универсальная (молярная) газовая
постоянная; k
= R/NA
=
1,38∙10-23
Дж/К - постоянная Больцмана; NA=
6,02∙1023
моль-1;
m
- масса молекулы.
;
R
= 8,31 Дж/(моль∙К) -
универсальная (молярная) газовая
постоянная; k
= R/NA
=
1,38∙10-23
Дж/К - постоянная Больцмана; NA=
6,02∙1023
моль-1;
m
- масса молекулы.
□ Среднее значение
модуля скорости: ‹v›
= 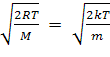 .
□ Вероятное
значение модуля скорости: vв
=
.
□ Вероятное
значение модуля скорости: vв
= 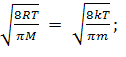
□ В состоянии теплового равновесия средние кинетические энергии всех молекул одинаковы.
□Температура – мера средней кинетической энергии теплового движения частиц. Любая температура Т по шкале Кельвина связана с той же температурой t по шкале Цельсия формулой T К = t + 273 oC.
