
3. Характерні швидкості розподілу Максвела
Середня арифметична швидкість молекул vсер. Використовуючи вираз для функції розподілу Максвела Fv, можна знайти значення середньої арифметичної швидкості молекул vсер.
За означенням середня швидкість дорівнює відношенню суми швидкостей усіх молекул в одиниці об’єму до числа усіх молекул n у цьому об’ємі. Кількість молекул dn в одиниці об’єму, швидкості яких знаходяться в інтервалі (v, v+dv),
dn = n Fvdv
Тоді сума швидкостей усіх dn таких молекул дорівнюватиме:
vdn = v n F(v)dv
Але v змінюється від v = 0 до v = . Це означає, що сума швидкостей усіх молекул газу, які мають швидкості в інтервалі від v = 0 до v = , буде дорівнювати:
![]()
Нарешті, середня арифметична швидкість запишеться так:
![]()
![]() (4)
(4)
Знайдемо значення середньої швидкості. Підставимо у вираз (4) замість F(v) її значення. Отримаємо:
 (5)
(5)
Позначимо
![]()
![]()
![]() .
.
Підставимо ці значення у вираз (5):
![]()
![]()
Проінтегрувавши
вираз
![]() частинами, отримаємо одиницю. Таким
чином, запишемо:
частинами, отримаємо одиницю. Таким
чином, запишемо:
![]()
Вираз для знаходження середньої швидкості молекул газу:

![]() .
(6)
.
(6)
Середню квадратичну швидкість можна отримати з виразу:
![]()
![]()
Але для отримання даних формул можна використати і поняття функції розподілу:
 .
.
Інтеграл у цій формулі знайдемо інтегруванням частинами:
 ,
,
звідси:
![]() ,
,
![]() .
(7)
.
(7)
Як вже було відзначено раніше, функція розподілу Максвела F(v) приймає максимальне значення при деякому значенні vvн, де vн – найбільш ймовірна швидкість молекул.
Для її знаходження продиференцюємо F(v) за v2 і похідну прирівняємо до нуля:
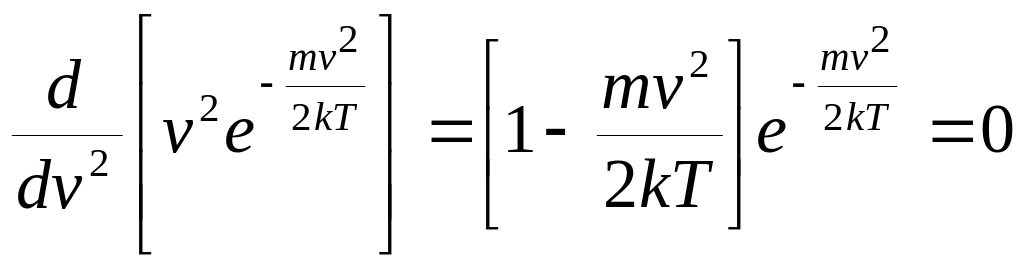
![]()
![]() .
(8)
.
(8)
П орівнюючи
вирази (6), (7) і (8), отримаємо співвідношення
між
орівнюючи
вирази (6), (7) і (8), отримаємо співвідношення
між
![]() ,
,
![]() і
і
![]() :
:
= 1,09 = 1,22
Оскільки ці швидкості відрізняються лише множником, то кожна з цих швидкостей може бути використана для характеристики теплового руху.
4. Експериментальна перевірка закону розподілу Максвела
Вперше експериментальна задачу про визначення швидкостей була вирішена в 1920 р. Отто Штерном, який вперше використав метод молекулярних пучків (м.п. - це вузькі потоки молекул, які літають у вакуумі без зіткнень прямолінійно). Але точність його методу була недостатньою.
В 1947 р. Штерн разом із Істерманом і Сімпсоном для перевірки закону розподілу закону молекул за швидкостями поставили інший більш складний і кропіткий дослід із використанням того ж методу молекулярних пучків. В цьому досліді спостерігались вільне падіння молекул пучка в полі сил тяжіння.
Д жерелом
атомів являвся розплавлений цезій
(температура його плавлення 301.1 К або
28.5 оС),
який випаровувався із певної точки А.
В ній цезій нагрівався до 450 К. З пічки
атоми цезію вилітають через вузьку
щілину шириною 0.02 мм . На відстані 1 мм
від
жерелом
атомів являвся розплавлений цезій
(температура його плавлення 301.1 К або
28.5 оС),
який випаровувався із певної точки А.
В ній цезій нагрівався до 450 К. З пічки
атоми цезію вилітають через вузьку
щілину шириною 0.02 мм . На відстані 1 мм
від
![]() розташовується друга щілина
розташовується друга щілина
![]() такої ж ширини, як і перша. Мішень
такої ж ширини, як і перша. Мішень
![]() - тонкий вольфрамовий дріт товщиною
0.02 мм знаходиться на відстані 1 м від
(дріт перпендикулярний до площині
рисунка). Повний шлях пучку – 2 м. Весь
пристрій розміщувався в посудині із
високим вакуумом. Щілини
,
та мішень
розташовувались на одній горизонтальній
прямій.
- тонкий вольфрамовий дріт товщиною
0.02 мм знаходиться на відстані 1 м від
(дріт перпендикулярний до площині
рисунка). Повний шлях пучку – 2 м. Весь
пристрій розміщувався в посудині із
високим вакуумом. Щілини
,
та мішень
розташовувались на одній горизонтальній
прямій.
Дріт-мішень нагрівають до такої температури, при якій атоми цезію, що попадають на неї, іонізуються і перетворюються на позитивні іони. Іони тут же лишають мішень і попадають на від’ємно заряджений циліндр, в якому власне дріт і розміщується (зрозуміло, що в ньому є прорізи для проходження атомів). Між дротом і циліндром тече струм, який після підсилення і вимірюється. Сила струму безпосередньо визначається кількістю іонів, а отже і кількістю атомів, що попали на дріт.
Атом
цезію під дією сили тяжіння рухається
за параболою. Отже навішень попадуть
тільки частинки, що вилетіли під деяким
кутом
![]() .
.
Для координат та будь-якої точки траєкторії можна записати
 ,
,
![]() і
і
![]() -
це
рівняння параболи.
-
це
рівняння параболи.
В точці
траєкторії атомів
![]() ,
а рівняння параболи отримує вигляд
,
а рівняння параболи отримує вигляд
![]() .
.
Звідси вираз для :
![]()
Тепер ми підставимо цю величину в рівняння параболи при x = L
![]() .
.
Остаточно,
зміщення атомів вздовж
![]() визначаються лише значенням
,
які при малих
взагалі близькі до самої швидкості.
визначаються лише значенням
,
які при малих
взагалі близькі до самої швидкості.
Якщо переміщувати дріт по висоті і вимірювати струм, то можна визначити кількість атомів, які мають різні швидкості. Тобто в такий спосіб можна переварити розподіл молекул за швидкостями.
Відзначимо, вимірявши кількість атомів на певній висоті, ми визначимо кількість атомів, які лежать у деякому інтервалі швидкостей, оскільки товщина дроту конечна і на неї попадають атоми з близькими, а не однаковими швидкостями.
В експерименті навіть найповільніші атоми зміщуються лише на 0.2 мм. Але ж товщина дроту складала 0.02 мм! Тобто вимірювання були проведені із достатньо великою точністю.
Вимірювання підтвердили розподіл Максвела.
