
- •60.Основные процессы первой стадии гликолиза, их физиологическая значимость.
- •61.Реакции второй стадии гликолиза, их физиологическая значимость.
- •62. Образование ацетил-СоА, его участие в метаболизме. Общая схема и суммарное уравнение цикла Кребса (трикарбоновых кислот).
- •63.Основные ферменты и реакции цикла Кребса.
- •64.Основные реакции и физиологическая роль глиоксилатного пути.
- •66.Основные компоненты и их последовательность расположения в митохондриальной электрон-транспортной цепи. Суммарная схема работы этц дыхания.
- •67.Характеристика комплексов I и II этц дыхания.
- •68.Характеристика комплекса III этц дыхания.
- •69.Характеристика комплекса IV этц дыхания.
- •70. Локализация и механизм сопряженного с транспортом протонов синтеза атф
- •71. Строение и механизм работы комплекса митохондриальной атф-синтазы
- •72. Строение и свойства воды, её функции в растении
- •73. Когезия и адгезия, уникальные свойства воды, роль воды в жизни растений.
- •74. Симпластический и апопластический пути переноса воды и растворенных веществ. Механизм транспорта воды через мембрану
- •76. Аквапорины: структура, функции и механизм регуляции.
- •77. Транспирация, ее механизм и роль в жизни растений. Механизм гуттации.
- •79. Механизм передвижеия воды из корня в надземные органы. Верхний и нижний концевые двигатели.
- •81. Осноные функции макро- и микроэлементов минерального питания.
- •82. Доступнось минеральных элементов, роль хелатов в минеральном обмене.
- •83. Принцип пассивного и активного транспорта веществ. Законы Фика, электрохимический потенциал ионов, его значение в жизни растений.
- •84. Потенциал Нернста, мембранный диффузионный потенциал.
- •85. Потенциал Доннана, моделирование процессов минерального обмена. Строение эпидермиса корня в связи с его поглощающей функцией.
- •86. Транспорт веществ из почвенного раствора в цитоплазму через плазматическую мембрану эпидермальных клеток корня. Особенности строения эпидермиса корня.
- •87. Примеры структуры субъединиц катионных каналов, их молекулярно-биологических и физиологических свойств.
- •5 Типов
- •93. Механизм фиксации азота бобовыми, стадии и значение нодуляции.
- •94. Химизм и физиологическая значимость реакций переаминирования.
- •96. Определения роста, развития и онтогенеза растений. Этапы онтогенеза.
- •97. Кривая роста растений, ее фазы. Скорость роста растений. Классификация типов дифференцированных клеток.
- •98. Физиологическая роль, локализация и типы меристем. Рост стебля двудольных.
- •100. Классические и современные представления о росте клетки растяжением.
- •102. Фитогормоны, признаки отнесения вещества к гормонам, критерии обнаружения рецепторов. Названия основных классов фитогормонов.
- •103. Общие принципы сигнализации при помощи рецепторов клеточной поверхности. Понятие сигнальной трансдукции и сигнальных агентов. Три основные типа мембраных рецепторов.
- •107. Строение и функции ауксинов.
- •109. Механизмы стимуляции роста ауксинами.
- •110. Структура и функции цитокининов.
- •111. Химическая природа, разнообразие и функции гиббереллинов.
- •112. Химическая природа и основные функции брассиностероидов, этилена, абсцизовой кислоты и активных форм кислорода.
- •113. Негормональные регуляторы роста растений. Их типы и применение.
- •114. Определение стресса по Селье и другим авторам, триада Селье, широта понятия стресса в современной биологии растений.
- •115. Примеры стрессоров. Наиболее важные стрессы. Определение адаптации. Специфический и неспецифический стрессовые ответы. Общие схемы эустресса и дистресса у растений
- •116. Классическое и современное определение оксидативного стресса. Важность оксидативного стресса. Основные типы активных форм кислорода, время их распада.
- •119. Основные сайты (места) биосинтеза афк в растениях, локализация синтеза афк в фотосистемах. Классический и неклассический пути синтеза гидроксильного радикала.
- •120. Детоксификация афк в органеллах растений. Сайты синтеза супероксида в пероксисомах.
- •121. Аскорбат-глутатионовый цикл, его физиологическая роль
- •122. Методы изучения оксидативного стресса, афк-сенсоры (рецепторы) в клетках растений. Кальций-связывающие белки и их физиологическая роль.
- •123. Реакции гидроперекисного окисления липидов.
- •126. Механизм поступления натрия и борьба с засолением. Способы защиты от избытка солей.
- •4. Активацяи sos2 (протеин-киназы) – напрямую под действием прямого физического взаимодействия с sos3
- •127. Оксидативное «повреждение» углеводов и нуклеиновых кислот
- •128. Основные и вспомогательные системы антиоксидатной защиты растений.
- •129. Пероксидазы растений, их структура, функция и физиологические роли.
62. Образование ацетил-СоА, его участие в метаболизме. Общая схема и суммарное уравнение цикла Кребса (трикарбоновых кислот).
Образовавшийся в аэробных условиях ацетил-СоА вступает в цикл Кребса.
В цикле Кребса после реакций отнятия и присоединения воды, декарбоксилирования и дегидрирования ацетильный остаток, поступивший в цикл в виде ацетил-СоА, полностью расщепляется.
Суммарная реакция записывается в следующем виде:
СН3СО ~ S-СоА + 3Н2О + АДФ + Н3РО4 → НS-СоА + 2СО2 + 4[Н2] + АТФ
Общая схема:
Стадия 1 – окисление глюкозы, жирных кислот и некоторых аминокислот приводит к синтезу ацетил коэнзима А.
Стадия 2 – окисление ацетильных групп в цитрате (анион лимонной кислоты) имеет 4 шага «отделения» электронов.
Стадия 3 – электроны, переносимые НАДН и ФАДH2 попадают в ЭТЦ митохондрий, приводя к восстановлению O2 до H2O. Этот поток электронов энергизирует продукцию АТФ (фермент АТФ-синтаза).
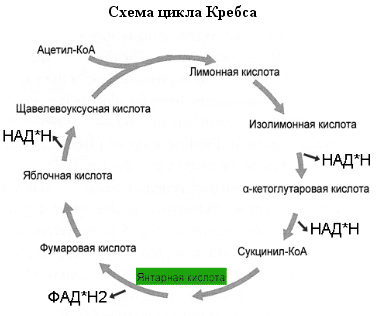
63.Основные ферменты и реакции цикла Кребса.
Ферменты:
1 – цитратсинтаза
2 – аконитаза
3 – изоцитратдегидрогеназа
4 – a-кетоглутарат-дегидрогеназный комплекс
5 – сукцинил-СоА-лигаза
6 – сукцинатдегидрогеназа
7 – фумаратгидротаза
8 – малатдегидрогеназа
Первая реакция катализируется ферментом цит-рат-синтазой, при этом ацетильная группа ацетил-КоА конденсируется с оксалоацетатом, в результате чего образуется лимонная кислота.
Второя реакция-образовавшаяся лимонная кислота подвергается дегидратированию с образованием цис-аконитовой кислоты, которая, присоединяя молекулу воды, переходит в изолимонную кислоту (изоцитрат).
Третья реакция, лимитирует скорость цикла Кребса. Изолимонная кислота дегидрируется в присутствии НАД-зависимой изо-цитратдегидрогеназы в альфа-Кетоглуторат.
Четвертой реакции происходит окислительное декарбокси-лирование α-кетоглутаровой кислоты с образованием высокоэнергетического соединения сукцинил-КоА.
Пятая реакция катализируется ферментом сукцинил-КоА-синтета-зой. В ходе этой реакции сукцинил-КоА при участии ГТФ и неорганического фосфата превращается в янтарную кислоту (сукцинат). Одновременно происходит образование высокоэргической фосфатной связи ГТФ за счет высокоэргической тиоэфирной связи сукцинил-КоА
Шестой реакции сукцинат дегидрируется в фумаровую кислоту. Окисление сукцината катализируется сукцинатдегидрогеназой, в молекуле которой с белком прочно (ковалентно) связан кофермент ФАД.
Седьмая реакция осуществляется под влиянием фермента фума-ратгидратазы (фумаразы). Образовавшаяся при этом фумаровая кислота гидратируется, продуктом реакции является яблочная кислота (малат).
Восьмой реакции цикла трикарбоновых кислот под влиянием митохондриальной НАД-зависимой малатдегидрогеназы происходит окисление L-малата в оксалоацетат.
За один оборот цикла, состоящего из восьми ферментативных реакций, происходит полное окисление одной молекулы ацетил-КоА.
64.Основные реакции и физиологическая роль глиоксилатного пути.
Глиоксилатный Цикл , циклич. ферментативный процесс, в к-ром происходит превращ. уксусной к-ты в виде ацетилкофермента А в ди- и трикарбоновые к-ты, а промежут. продуктом является глиоксиловая к-та.
Первый этап. Изоцитрат при участии изоцитратлиазы расщепляется на янтарную и глиоксиловую кислоты.
Сукцинат (янтарная кислота) выходит из цикла, а глиоксилат связывается с ацетил-СоА, и образуется малат. Реакция катализируется малатсинтазой. Малат окисляется до ЩУК, и цикл заканчивается.
Кроме двух ферментов – изоцитратазы (изоцитратлиазы) и малатсинтазы, – все остальные такие же, что и в цикле Кребса. При окислении малата восстанавливается молекула НАД+. Источником ацетил-СоА для этого цикла служат жирные кислоты, образующиеся при разрушении жиров.
Суммарное уравнение цикла можно записать в виде:
2СН3СО-S-СоА + 2Н2О + НАД+ →2НS-СоА + СООН-СН2-СН2-СООН + НАДН + Н+
Значение глиоксилатного цикла
- НАДН может окисляться с образованием трех молекул АТФ.
- сукцинат (янтарная кислота) выходит из глиоксисомы и поступает в митохондрию, где включается в цикл Кребса. Тут он преобразуется в ЩУК, затем в пируват, фосфоенолпируват и дальше в сахар.
Таким образом, с помощью глиоксилатного цикла жиры могут преобразовываться в углеводы.
Это очень важно особенно при прорастании семян, так как сахара могут транспортироваться из одной части растения в другую, а жиры лишены такой возможности.
Глиоксилат может служить материалом для синтеза порфиринов, а это значит и хлорофилла.
65. Общее выражение и основные реакции пентозофосфатного цикла.
Помимо гликолиза и цикла Кребса, существует и другой универсальный, присущий всем организмам путь полного окисления глюкозы – пентозофосфатный.
Ферменты, которые участвуют в этом процессе, локализованы в цитоплазме (гиалоплазме).
Исходным веществом для этого цикла является глюкозо-6-фосфат (Гл-6-Ф), который принимает участие и в гликолизе.
Пентозофосфатный путь, как и гликолиз, разделяют на две фазы: фазу окисления глюкозо-6-фосфата и фазу его регенерации.
При окислении глюкозо-6-фосфата образуется 6-фосфоглюколактон. Последний неустойчив и преобразуется в 6-фосфоглюконат (6-ФГ). В процессе окисления глюкозо-6-фосфата участвует фермент глюкозо-6-фосфатдегидрогеназа, коферментом которой выступает НАДФ+; последний в результате окисления глюкозо-6-фосфата восстанавливается.
6-фосфоглюконат, в свою очередь, подвергается окислительному декарбоксилированию, образуется рибулозо-5-фосфат (Рл-5-Ф), и восстанавливается НАДФ+, который является коферментом фосфоглюконатдегидрогеназы.
Если во время гликолиза одна молекула преобразуется в две триозы, то в пентозофосфатном цикле от глюкозо-6-фосфата отщепляется один атом углерода и образуется пентоза.
Образованием рибулозо-5-фосфата окислительная фаза цикла заканчивается.
В фазе регенерации участвуют только фосфорные эфиры сахаров.
Процесс идет от пентоз через образование седагептулозо-7-фосфата, эритрозо-4-фосфата, фруктозо-6-фосфата и фосфоглициринового альдегида.
Триозы могут конденсироваться до гексоз!
В результате альдольной конденсации двух триоз образуется фруктозо-1,6-дифосфат (Фр-1,6-ДФ).
Гидролиз фосфатной связи приводит к образованию фосфорной кислоты и глюкозо-6-фосфата.
Цикл заканчивается.
В результате этого цикла из шести молекул глюкозо-6-фосфата одна молекула окисляется до СО2, а пять молекул регенерируют вновь и выходят из цикла.
При этом восстанавливается 12 молекул НАДФ+.
Суммарное уравнение пентозофосфатного цикла можно записать в виде:
6 Гл-6-Ф + 12НАДФ+ + 7 Н2О →5 Гл-6-Ф + 6СО2 + 12НАДФН + 12Н+ + Н3РО4
