
- •I Физические свойства горных пород-коллекторов нефти и газа
- •II физико-механические и тепловые свойства горных пород
- •§ 1. Напряженное состояние пород в условиях залегания в массиве
- •§ 2. Напряженное состояние пород в районе горных выработок
- •§ 3. Деформационные и прочностные свойства горных пород
- •4. Упругие изменения свойств коллекторов в процессе разработки и эксплуатации нефтяных и газовых месторождении
- •§ 5. Влияние давления на коллекторские свойства пород
- •§ 6. Упругие колебания в породах и их акустические свойства
- •§ 7. Тепловые свойства горных пород
- •Глава III состав и физические свойства природных газов и нефтей
- •§1. Физическое состояние нефти газа при различных условиях в залежи
- •§ 2. Состав и классификация нефтей
- •§ 3. Состав и классификация природных газов
- •§ 4. Газовые смеси Плотность газа
- •Состав газовой смеси
- •Содержание тяжелых углеводородов в газе
- •Парциальное давление и парциальный объем компонента в смеси идеальных газов
- •§5. Жидкие смеси Состав и характеристика жидкой смеси
- •Объем паров после испарения жидкости
- •§ 6. Коэффициент сверхсжимаемости природных газов
- •§ 7. Плотности природного газа, стабильного и насыщенного углеводородного конденсата
- •§ 8. Вязкость газов и углеводородных конденсатов
- •§ 9. Определение изобарной молярной теплоемкости природных газов
- •Пругость насыщенных паров
- •§ 11. Растворимость газов в нефти и в воде
- •§ 12. Давление насыщения нефти газом
- •§ 13. Сжимаемость нефти. Объемный коэффициент
- •§ 14. Плотность пластовой нефти
- •§ 15. Вязкость пластовой нефти
- •§ 16. Структурно-механические свойства аномально-вязких нефтей
- •§ 17. Приборы для исследования свойств пластовых нефтей
- •Установка асм-зоом для исследования пластовых нефтей
- •§ 18. Фотоколориметрия нефти
- •Глава IV фазовые состояния углеводородных систем
- •§ 1. Схемы фазовых превращений углеводородов
- •Поведение бинарных и многокомпонентных систем в критической области
- •§ 2. Критическая температура и критическое давление многокомпонентных углеводородных смесей
- •§ 3. Влагосодержание природных газов и газоконденсатных систем, влияние воды на фазовые превращения углеводородов
- •§ 4. Фазовое состояние системы нефть-газ при различных давлениях и температурах
- •§ 5. Краткая характеристика газогидратных залежей
- •§ 6. Газоконденсатная характеристика залежи. Приборы для лабораторного изучения свойств газоконденсатных смесей
- •Методика исследования на установке уфр-2
- •Исследование проб сырого конденсата и отсепарированного газа
- •§ 7. Расчет фазовых равновесий углеводородных смесей
- •Константы фазовых равновесий
- •Уравнения фазовых концентраций
- •Определение констант фазового равновесия по давлению схождения
- •Аналитический расчет фазовых превращений газоконденсатных смесей при изменении давления и температуры
- •Глава V пластовые воды и их физические свойства
- •§ 1. Состояние остаточной (связанной) воды в нефтяных и газовых коллекторах
- •§ 2. Методы определения количества остаточной (связанной) воды в пластах
- •§ 3. Состояние переходных зон нефть-вода, нефть-газ и вода-газ
- •§ 4. Физические свойства пластовых вод
- •§ 5. Выпадение неорганических кристаллических осадков цз попутно добываемой воды
- •Глава VI молекулярно-поверхностные свойства системы нефть—газ—вода—порода
- •§ 1. Роль поверхностных явлений при движении нефти, воды и газа в пористой среде
- •§ 2. Зависимость поверхностного натяжения пластовых жидкостей от давления и температуры
- •§ 3. Смачивание и краевой угол. Работа адгезии. Теплота смачивания
- •§ 4. Кинетический гистерезис смачивания
- •§ 5. Свойства поверхностных слоев пластовых жидкостей
- •§ 6. Измерение углов смачивания
- •Глава VII физические основы вытеснения нефти водой и газом из пористых сред
- •§ 1. Источники пластовой энергии. Силы, действующие в залежи
- •§ 2. Поверхностные явления при фильтрации пластовых жидкостей. Причины нарушения закона дарси
- •§ 3. Электрокинетические явления в пористых средах
- •§ 4. Дроссельный эффект при движении жидкостей и газов в пористой среде
- •§ 5. Общая схема вытеснения из пласта нефти водой и газом
- •§ 6. Нефтеотдача пластов при различных условиях дренирования залежи
- •§ 7. Роль капиллярных процессов при вытеснении нефти водой из пористых сред
- •§ 8. Использование теории капиллярных явлений для установления зависимости нефтеотдачи от различных факторов
- •§ 9. Зависимость нефтеотдачи от скорости вЫтеснения нефти водой
- •§ 10. Компонентоотдача газовых и газоконденсатных месторождений
- •Глава VIII повышение нефте- и газоотдачи пластов
- •§ 2. Моющие и нефтевытесняющие свойства вод
- •§ 3. Обработка воды поверхностно-активными веществами
- •§ 4. Применение углекислого газа для увеличения нефтеотдачи пластов
- •§ 5. Вытеснение нефти из пласта растворами полимеров
- •§ 6. Щелочное и термощелочное заводнение
- •§ 7. Мицеллярные растворы
- •§ 8. Термические способы увеличения нефтеотдачи
- •§ 9. Условия взаиморастворимости углеводородов оторочки с нефтью и газом
- •§ 10. Извлечение нефти газом высокого давления
- •Список литературы
§ 9. Определение изобарной молярной теплоемкости природных газов
Удельная теплоемкость — количество теплоты, сообщаемой единице массы вещества, чтобы изменить его температуру на один градус. Для газов различают изобарную ср и изохорную сv удельные теплоемкости,
![]()
![]() Ошибка!
Ошибка связи. (Ш.59)
Ошибка!
Ошибка связи. (Ш.59)
где индексы у скобок означают давление р = const и объем V= const.
Согласно первому началу термодинамики имеем dQ=dt—Vdp, (III. 60)
где Q — количество
теплоты; V — объем системы; i—
энтальпия (теплосодержание). di = cpdT
+
![]() .
(III.61)
.
(III.61)
При изобарном процессе (р = const) изменение количества теплоты системы равно изменению ее энтальпии dQ = di = CpиdT (II1.62)
или ![]() (Ш-63)
(Ш-63)
Изобарная молярная теплоемкость идеальных газов Сри зависит от температуры. Зависимость молярной теплоемкости компонентов природных газов при атмосферном давлении от температуры приближенно можно выразить формулой
Сри
= 0,523 (8,36+0,00892t)![]() ,
кДж/(кмоль-К), (III.64)
,
кДж/(кмоль-К), (III.64)
где Mi — молекулярная масса углеводорода, являющегося компонентом природного газа (от метана до гептана включительно)
Погрешность расчетов по формуле (III. 64) для углеводородов CH4-C5H12 в интервале температур минус 40 °С плюс 120 ОС не превышает 5%, для углеводородов С6Н14—С7Н16 в том же интервале температур не превышает 10 %.
Изобарная молярная теплоемкость неуглеводородных компонентов природных газов (азота, углекислого газа, сероводорода) равна примерно половине теплоемкости углеводорода с одинаковой молекулярной массой при одинаковой температуре.
Например, изобарная молярная теплоемкость CO2(Cри=44) равна половине молярной теплоемкости пропана С3Н8 (Сри=44), которая рассчитывается по формуле (111.64).
Теплоемкость смесей газов определяется по правилу аддитивности(II1.65)
![]()
где yi - молярная доля i-ro компонента в смеси; cpi — изобарная молярная теплоемкость i-ro компонента.
Изобарная молярная теплоемкость реальных природных газов зависит от давления и температуры Ср = Сри(t) + Ср(р, t), (Ш.66)
где Ср(р, t) —изотермическая поправка теплоемкости на давление (рис. III.9).
Изобарную молярную теплоемкость природного газа можно рассчитать и по формуле, предложенной Л. М. Гухманом и Т. В. Нагаревой:
 (III.67)
(III.67)
При решении задач, связанных с добычей, транспортом, хранением и переработкой природных газов, наиболее употребительны двухконстантные уравнения состояния и восьмиконстантные.
Р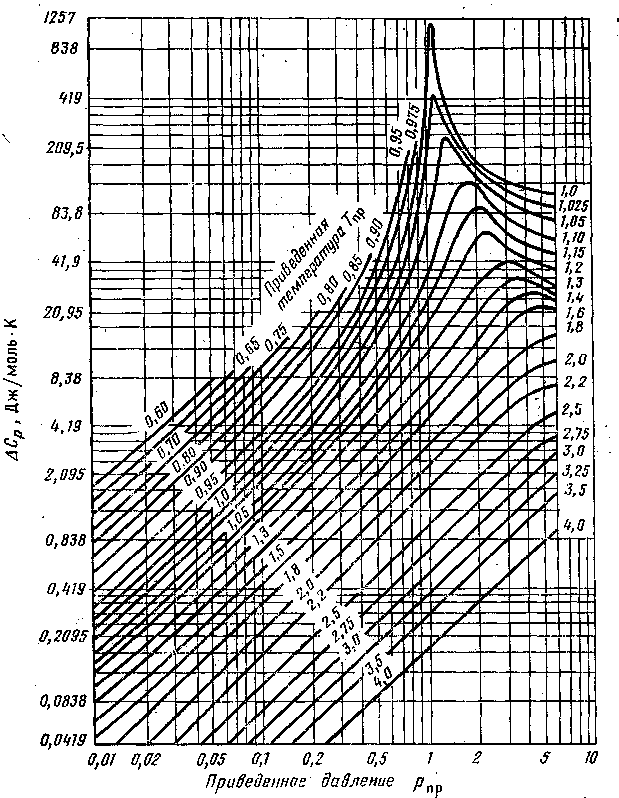 ис.
III.9. Зависимость изотермической поправки
изобарной мольной теплоемкости Ср(р,
t) от приведенных абсолютных давления
рпр и
температуры Тпр
ис.
III.9. Зависимость изотермической поправки
изобарной мольной теплоемкости Ср(р,
t) от приведенных абсолютных давления
рпр и
температуры Тпр
Последней, наиболее удачной модификацией двухконстантного уравнения состояния природных газов, предложенной в 1975 г., является уравнение состояния Пенга — Робинсона
![]() (III.68)
(III.68)
где V —молярный объем; а(Т), b — коэффициенты уравнения, определяемые критическими параметрами вещества (коэффициент а(Т) —фракция температуры).
Уравнение состояния Пенга—Робинсона, записанное относительно коэффициента сверхсжимаемости z, имеет вид z3-(1-В)z2+(А-3В2-2В)z-(АВ—В2-B3)=0, (69)
где ![]() ;
; ![]() (III.70)
(III.70)
Уравнение (III.69) имеет один или три действительных корня. Если смесь находится в двухфазном состоянии, то больший корень относится к паровой фазе, а наименьший положительный корень — к жидкой фазе.
При критических условиях (zкp = 0,307)
![]() ;
; ![]() (Ш.71)
(Ш.71)
При температурах, отличных от критической,
![]() ;
; ![]() ,
(111.72)
,
(111.72)
где
![]() — безразмерная функция приведенной
температуры Тпр
и ацентрического фактора ;
при критической температуре =1.
— безразмерная функция приведенной
температуры Тпр
и ацентрического фактора ;
при критической температуре =1.
Для всех веществ зависимость между 0,5 и Т0,5пр может быть аппроксимирована уравнением прямой 0,5 =1+m(1- Т0,5пр), (III.73)
где коэффициент m, определяющий угол наклона прямой к оси Т0,5пр, является функцией ацентрического фактора : m=0,37464+1,5422b—0,269922. (III.74)
При использовании уравнения Пенга—Робинсона для расчета термодинамических и физических свойств многокомпонентных смесей коэффициенты аcм(Т) и bсм вычисляют по следующим формулам:
![]()
![]() (111.75)
(111.75)
![]()
![]() (III.76).
(III.76).
Отклонение теплофизических свойств реальных природных газов от идеальных можно определить с использованием уравнения состояния Пенга — Робинсона.
Отклонение энтальпии реального газа
![]() (III.77)
(III.77)
г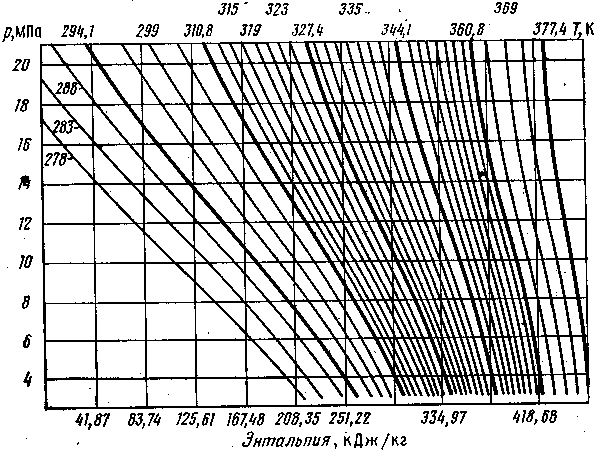 де
Н° — энтальпия идеального газа.
де
Н° — энтальпия идеального газа.
Энтальпийная диаграмма природного газа изображена на рис. III.10.
Рис. III.10. Энтальпийная диаграмма природного газа
Отклонение молярной изобарной теплоемкости реального газа
![]() .
(III_78)
.
(III_78)
Зависимость Ср от рпр и Тпр изображена на рис. III.9
Разность изобарной и изохронной молярных теплоемкостей реального газа
 (79)
(79)
где (80)
(80)
 (81)
(81)
