
- •Аллотропия веществ, состав, строение, свойства аллотропных модификаций.
- •2. Кетоны — это органические вещества, в молекулах которых карбонильная группа связана с двумя углеводородными радикалами.
- •3. Кокосохимическое производство
- •1. В расплавах или растворах происходит диссоциация электролита. Катионы смещаются к катоду, анионы — к аноду.
Билет №9
1.Окисление
Окисление
- процесс отдачи электронов, с увеличением
степени окисления.
При
окисле́нии вещества в результате отдачи
электронов увеличивается его степень
окисления. Атомы окисляемого вещества
называются донорами электронов, а атомы
окислителя — акцепторами электронов.
В
некоторых случаях при окислении молекула
исходного вещества может стать
нестабильной и распасться на более
стабильные и более мелкие составные
части (см. Свободные радикалы). При этом
некоторые из атомов получившихся молекул
имеют более высокую степень окисления,
чем те же атомы в исходной молекуле.
Окислитель,
принимая электроны, приобретает
восстановительные свойства, превращаясь
в сопряжённый восстановитель:
окислитель
+ e− ↔
сопряжённый
восстановитель.
[править]Восстановление
Восстановле́нием
называется процесс присоединения
электронов атомом вещества, при этом
его степень окисления понижается.
При
восстановлении атомы или ионы присоединяют
электроны. При этом происходит понижение
степени окисления элемента. Примеры:
восстановление оксидов металлов до
свободных металлов при помощи водорода,
углерода, других веществ; восстановление
органических кислот в альдегиды и
спирты; гидрогенизация жиров и
др.
Восстановитель,
отдавая электроны, приобретает
окислительные свойства, превращаясь в
сопряжённый окислитель:
восстановитель
— e− ↔
сопряжённый окислитель.
Несвязанный,
свободный электрон является сильнейшим
восстановителем..
2.Термодеструктивные (термический крекинг, висбрекинг, коксование, пиролиз, пекование, производство технического углерода и др.).
2.1.2. Термоокислительные (производство битума, газификация кокса, углей и др.).
В термодеструктивных процессах протекают преимущественно реакции распада (крекинга) молекул сырья на низкомолекулярные, а также реакции конденсации с образованием высокомолекулярных продуктов, например кокса, пека и др. Каталитические процессы по типу катализа можно классифицировать на следующие типы:
2.2.1. Гетеролитические, протекающие по механизму кислотного катализа (каталитический крекинг, алкилирование, полимеризация, производство эфиров и др.);
2.2.2. Гомолитические, протекающие по механизму окислительно-восстановительного (электронного) катализа (производство водорода и синтез газов, метанола, элементной серы).
2.2.3 Гидрокаталитические, протекающие по механизму бифункционального (сложного) катализа (гидроочистка, гидрокрекинг, каталитический риформинг, изомеризация, гидродеар-я, гидродепафинизация и др.).
3.

Билет № 10
1. В периодической системе элементов металлы в основном располагаются в главных подгруппах I—Ill групп, а также в побочных подгруппах.
![]()
В IA группе у атомов элементов на внешнем энергетическом уровне находится 1 электрон в состоянии s1, во IIA группе у атомов на внешнем ЭУ 2 электрона в состоянии s2. Эти элементы относятся к s-элементам. В IIIA группе у всех элементов на внешнем ЭУ 3 электрона в состоянии s2p1. Они относятся к p-элементам.
В IA группу входят щелочные металлы Li, Na, K, Rb, Cs, Fr, активность которых при движении сверху вниз увеличивается вследствие увеличения радиуса атомов, металлические свойства возрастают также, как и у щелочеземельных металлов IIA группы Be, Mg, Ca, Sr, Ba, Ra и металлов IIIA группы Al, Ga, In, Tl.
Оксиды типа R2O характерны только для Li, для всех остальных щелочных металлов характерны пероксиды R2O2, которые являются сильными окислителями.
Все металлы этих групп образуют основные оксиды и гидроксиды, кроме Be и Al, которые проявляют амфотерные свойства.
Химические свойства. Атомы металлов имеют больший радиус, чем атомы неметаллов, поэтому легко теряют валентные электроны. Вследствие этого металлы проявляют восстановительные свойства.
![]()
2.

3. Каучуки представляют собой натуральные (природные) и синтетические материалы, которые характеризуются такими свойствами, как эластичность, водонепроницаемость, а также обладают хорошей электроизоляцией. Как правило, натуральный и синтетический каучук является основным сырьем для изготовления резины и эбонита. Осуществляется этот процесс путем вулканизации, представляющей собой определенный технологический процесс, в результате которого взаимодействует каучук и вулканизирующий агент (сера, оксиды металлов и иные вещества). Натуральный или природный каучук представляет собой полимер изопрена, который в большинстве своем содержится в млечном соке гевеи и многих других растений. Основными физическими и химическими свойствами этого эластомера является его растворимость в углеводородах и их производных, нерастворимость в воде и спиртах. При комнатной температуре, как правило, природный каучук присоединяет кислород, вследствие чего происходит «старение» материла, в связи с чем, уменьшается и его эластичность и прочность. На сегодняшний день натуральный и синтетический каучук используются чрезвычайно широко, так, около 60% натурального каучука являются основным сырьем для производства автомобильных шин. Основные поставки этого материала осуществляет Индонезия, Вьетнам и Малайзия.
Использование натурального и синтетического каучука позволило значительно расширить производство изделий во многих отраслях промышленности. Однако синтетический каучук, благодаря своему многообразию и улучшенным эксплуатационным свойствам, используется намного чаще, чем его натуральный аналог. Так, изопреновые каучуки представляют собой один из типов синтетических каучуков, которые производятся путем полимеризации изопрена катализаторами. Этот тип каучуков отличается тем, что не сильно уступает в эластичности природному сырью. Бутадиен-метилстирольный каучук успешно применяется в шинной, кабельной, резинотехнической и других промышленных отраслях. Бутилкаучук широко используют в строительной области, при изготовлении клея, герметиков и других подобных материалов. Работа над совершенствованием технологических процессов обработки натурального и синтетического каучука, изготовлением из него тех или иных изделий не прекращается и по сей день, чтобы удовлетворить запросы самых различных категорий потребителей.
Билет № 11
При движении сверху вниз по группам увеличивается радиус атома и следовательно уменьшаются окислительные свойства.
Сравнительная характеристика окислительно-восстановительных свойств неметаллов на примере кислорода и серы.
Схемы электронных оболочек:
![]()
На внешнем электронном уровне атомов кислорода и серы находится по 6 электронов.
У кислорода окислительные свойства выражены сильнее, так как радиус атома меньше и валентные электроны сильнее притягиваются к ядру. Для кислорода наиболее характерна степень окисления —2, проявляющаяся при достройке внешнего энергетического уровня до 8 электронов.
Сера также может являться окислителем, проявляя степень окисления —2, но характерны также степени окисления +4 (при потере 4 р-электронов) и +6 (при потере всех шести валентных электронов).
В реакциях с металлами кислород и сера проявляют окислительные свойства, образуя оксиды и сульфиды соответственно:
![]()
В реакциях с неметаллами кислород проявляет свойства окислителя:
![]()
Сера может быть как окислителем
![]()
так и восстановителем:
![]()
Сера выступает в роли восстановителя в реакции с концентрированной азотной кислотой:
![]()
2.
Альдегиды (от лат. alcohol dehydrogenatum — спирт, лишённый водорода) — класс органических соединений, содержащих карбонильную группу (С=О) с одним алкильным или арильным заместителем. Альдегиды и кетоны весьма схожи, различие заключается в том, что последние имеют при карбонильной группе два заместителя. Поляризация двойной связи «углерод-кислород» по принципу мезомерного сопряжения позволяет записать следующие резонансные структуры: С=О ↔ С+—О−
3.

Билет №12
Аллотропия веществ, состав, строение, свойства аллотропных модификаций.
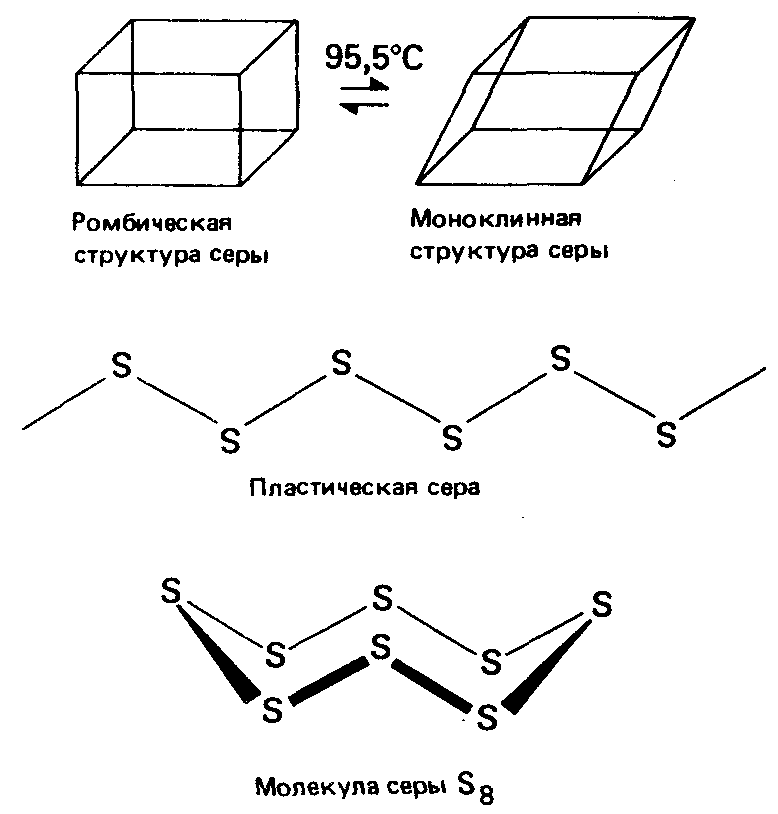
Если какой-либо элемент может существовать в двух или нескольких твердых формах (кристаллических либо аморфных), то считается, что он проявляет аллотропию. Различные формы одного элемента называются аллотропами. Аллотропы существуют приблизительно у половины всех элементов.
Например, углерод существует в виде алмаза либо графита. Сера существует в двух кристаллических формах - ромбической и моноклинной - в зависимости от температуры. Обе ее кристаллические формы являются примерами молекулярных кристаллов. Молекулы в них представляют собой гофрированные циклы, в каждом из которых содержится по восемь ковалентно связанных атомов серы. Твердая сера может существовать еще в третьей аллотропной форме как пластическая сера. Эта форма серы неустойчива. Она состоит из длинных цепочек атомов серы, которые при комнатной температуре разрушаются и снова образуют молекулы S8, кристаллизующиеся в ромбическую решетку.
Фосфор может существовать в трех аллотропных формах. Наиболее устойчивая из них-красный фосфор. Красный фосфор имеет каркасную кристаллическую структуру, в которой каждый атом ковалентно связан с тремя другими атомами фосфора. Белый фосфор представляет собой молекулярный кристалл. Каждая его молекула содержит четыре атома фосфора, ковалентно связанных в тетраэдричес-кую структуру. Третий аллотроп - черный фосфор - образуется только при высоких давлениях. Он существует в виде макромолекулярной слоистой структуры.
![]()
2. Кетоны — это органические вещества, в молекулах которых карбонильная группа связана с двумя углеводородными радикалами.
Общая формула кетонов: R1–CO–R2. Кетоны — летучие жидкости или легкоплавкие твёрдые вещества, низшие представители хорошо растворимы в воде и смешиваются с органическими растворителями, некоторые (ацетон) смешиваются с водой в любых отношениях. Невозможность образования межмолекулярных водородных связей обуславливает несколько бо́льшую их летучесть, чем успиртов и карбоновых кислот с той же молекулярной массой.
Существует три основных типа реакций кетонов.
Первый связан с нуклеофильной атакой по атому углерода карбонильной группы. Например, взаимодействие кетонов с цианид-анионом или металлорганическими соединениями. К этому же типу (нуклеофильного присоединения) относится взаимодействие карбонильной группы со спиртами, приводящее к ацеталям и полуацеталям.
Взаимодействие со спиртами:
CH3COCH3 + 2C2H5OH → C2H5—O—C(CH3)2—O—C2H5 + H2O
c реактивами Гриньяра:
C2H5—C(O)—C2H5 + C2H5MgI → (C2H5)3—COMgI → (C2H5)3—COH, третичный спирт. Реакции с альдегидами, и особенно с метаналем идут заметно активнее, при этом с альдегидами образуются вторичные спирты, а с метаналем — первичные.
Также кетоны реагируют с азотистыми основаниями, например, с аммиаком и первичными аминами с образованием иминов:
CH3—C(O)—CH3 + CH3NH2 → CH3—C(N—CH3)—CH3 + H2O
Второй тип реакций — депротонирование бета-углеродного атома, по отношению к карбонильной группе. Образующийся карбанион стабилизирован за счёт сопряжения с карбонильной группой, лёгкость удаления протона возрастает, поэтому карбонильные соединения являются сравнительно сильными С—Н кислотами.
Третий — координация электрофилов по неподелённой паре атома кислорода, например, таких кислот Льюиса, как AlCl3.
К отдельному типу реакций можно отнести восстановление кетонов — восстановление по Лейкарту с выходами близкими к количественным.
Название |
Формула |
Температура плавления |
Температура кипения |
Диметилкетон |
CH3COCH3 |
−95 °C |
56,1 °C |
Метилэтилкетон |
CH3CH2COCH3 |
−86 °C |
80 °C |
Диэтилкетон |
CH3CH2COCH2CH3 |
−40 °C |
102 °C |
Ацетофенон |
|
19 °C |
202 °C |
Бензофенон |
|
47.9 °C |
305.4 °C |
Циклогексанон |
|
−16.4 °C |
155.65 °C |
Диацетил |
CH3COCOCH3 |
−3 °C |
88 °C |
Ацетилацетон |
CH3COCH2COCH3 |
−23 °C |
140 °C |
Парабензохинон |
|
115 °C |
— |
