
- •Физическая химия
- •I Химическая термодинамика
- •1. Внутренняя энергия системы. Теплота и работа. Первое начало термодинамики. Закон Гесса. Тепловой эффект реакции.
- •Следствия из закона Гесса.
- •4. Второе начало термодинамики. Обратимые и необратимые процессы. Энтропия. Связь энтропии со статическим весом.
- •2 Начало термодинамики.
- •5. Зависимость энтропии, внутренней энергии и энтальпии от давления и объема. Зависимость энтропии от температуры. Третье начало термодинамики.
- •II. Поверхностные явления, адсорбция
- •III Электрохимия
- •1. Активность ионов. Ионная сила раствора. Зависимость коэффициента активности иона от ионной силы раствора. Теория Дебая-Хюккеля.
- •2. Равновесие в растворах электролитов. Протолитическая теория кислот. Константа основности оснований.
- •3. Ионное произведение воды. РН-растворов. Индиеаторы. Буфферные растворы.
- •4. Окислительно-восстановительное равновесие. Электродные потенциалы. Электроды первого рода. Нормальный потенциал.Водородный электрод. Ряд напряжений.
- •5. Электроды второго рода. Каломельный электрод. Окислительно-восстановительные электроды.
- •6. Диффузионные потенциалы. Потенциометрическое титрование. Поляризация электродов. Полярография. Перенапряжение.
- •IX Химическая кинетика и катализ
- •1. Скорость химической реакции. Закон действующих масс. Кинетическое уравнение для моно- и бимомолекулярных реакций.
- •2. Влияние температуры на скорость химической реакции. Уравнение Аррениуса. Энергия активации и определение ее по экспериментальным данным.
- •3. Сложные химические реакции. Обратимые, параллельные и последовательные реакции. Метод квазистационарных концентраций (метод Боденштайна).
Следствия из закона Гесса.
I следствие. Тепловой эффект реакции разложения какого-либо химического соединения равен по абсолютной величине, но противоположен по знаку тепловому эффекту реакции образования этого соединения.
II следствие. Если совершаются две реакции, приводящие из различных исходных состояний к одинаковым конечным, то разница между тепловыми эффектами реакций представляет собой тепловой эффект перехода из одного исходного состояния в другое.
III следствие. Если совершаются две реакции, приводящие из одинаковых исходных состояний к различным конечным, то разница их тепловых эффектов есть тепловой эффект реакции перехода из одного конечного состояния в другое.
IV следствие. Тепловой эффект химической реакции равен сумме теплот образования конечных и исходных продуктов реакции с учетом коэффициентов перед химическими формулами этих продуктов в уравнении химической реакции.
В аналитической форме записи:
![]() ,
(3.16)
,
(3.16)
где Q – тепловой эффект химической реакции;
![]() - теплоты образования конечных и исходных
продуктов реакции соответственно.
- теплоты образования конечных и исходных
продуктов реакции соответственно.
Теплота образования – тепловой эффект химической реакции образования данного вещества (продукта химической реакции) из простых, устойчивых в данных условиях. Стандартной теплотой образования называют теплоту образования, отнесенную к температуре 298 К и давлению 1,01 * 105 Па. Если известна эта величина, то термохимический расчет позволяет определить теплоту образования и при других значениях параметров состояния.
V следствие. Тепловой эффект химической реакции равен разности сумм теплот сгорания исходных и конечных продуктов химической реакции с учетом коэффициентов у химических формул этих веществ в уравнении химической реакции.
В аналитической форме записи:
![]() ,
(3.17)
,
(3.17)
где
![]() - теплоты сгорания конечных и исходных
продуктов реакции соответственно.
- теплоты сгорания конечных и исходных
продуктов реакции соответственно.
Теплота сгорания – тепловой эффект реакции сгорания 1 моля вещества в атмосфере чистого кислорода до образования высшего оксида.
Теплота сгорания существенно зависит от температуры, поэтому для термохимических расчетов вводится некоторая точка отсчета – стандартная теплота сгорания. Стандартной теплотой сгорания называется теплота сгорания, отнесенная к стандартным условиям, т. е. к 298 К и р = 1,01*105 Па.
VI следствие. Теплота растворения.
Теплотой растворения называется количество теплоты, выделяемое или поглощаемое при растворении 1 моля вещества в таком количестве растворителя, при котором его дальнейшее добавление к раствору уже не вызывает изменение температуры последнего.
В этой связи табличные значения теплот относятся к раствору 1 моля растворяемого вещества в 200 – 400 молях растворителя.
Теплота растворения (q) – сумма двух слагаемых:
q = q1 + q2, (3.18)
где q1 – теплота, затрачиваемая на перевод вещества из обычного состояния в то, в котором оно находится в растворе;
q2 – теплота взаимодействия частиц растворителя с частицами растворенного вещества (теплота сольватации или гидратации, если растворитель вода).
VII следствие. Теплота плавления и испарения.
Процессы плавления и испарения всегда эндотермические процессы, т. к. на их реализацию необходимо затратить значительную энергию на разрушение данного порядка в структуре вещества.
Между теплотой испарения (![]() )
и температурой кипения (ТЕ)
существует взаимосвязь:
)
и температурой кипения (ТЕ)
существует взаимосвязь:
![]() ,
(3.19)
,
(3.19)
определяемая как правило Трутона.
Существует такая же взаимосвязь для
теплоты плавления (![]() )
и температуры плавления (TS):
)
и температуры плавления (TS):
![]() ,
(3.20)
,
(3.20)
называемая правилом Ричардса.
VIII следствие. Теплота нейтрализации.
Реакция нейтрализации – реакция между щелочами и кислотами. В ее основе лежит процесс нейтрализации ионов водорода (Н+) ионами гидроксида (ОН-), приводящий к образованию молекул воды. Следовательно, тепловой эффект всех подобных реакций должен быть одинаков, что и показали точные опыты.
Теплота нейтрализации примерно равна 57,08 кДж/моль, если в реакции участвует одноосновная кислота
Тепловой эффект реакции.
Тепловой эффект - количество теплоты, выделившееся или поглощенное химической системой при протекании в ней химической реакции.
Тепловой эффект обозначается символами Q или ΔH (Q = –ΔH). Его величина соответствует разности между энергиями исходного и конечного состояний реакции:
ΔH = Hкон. – Hисх. = Eкон. – Eисх.
Реакции, протекающие с выделением теплоты, проявляют положительный тепловой эффект (Q > 0, ΔH < 0) и называются экзотермическими.
Реакции, которые идут с поглощением теплоты из окружающей среды (Q < 0, ΔH > 0), т.е. с отрицательным тепловым эффектом, являются эндотермическими.
В ходе реакции происходит разрыв связей в исходных веществах и образование новых связей в продуктах реакции. Поскольку образование связи идет с выделением, а ее разрыв - с поглощением энергии, то химические реакции сопровождаются энергетическими эффектами. Энергия выделяется, если рвущиеся связи в исходных веществах менее прочны, чем связи, образующиеся в продуктах реакции, в противном случае - энергия поглощается. Обычно энергия выделяется и поглощается в форме теплоты, т.е. химическая форма энергии преобразуется в тепловую. Таким образом, химические реакции сопровождаются тепловыми эффектами.
2. Тепловой эффект реакции при постоянном объеме и постоянном давлении. Теплоты образования веществ из элементов. Методы определения теплот образования. Расчет тепловых эффектов реакций с помощью средних энергий связей.
Тепловой эффект реакции при постоянном объеме и постоянном давлении.
При протекании хим. Реакций происходит перестройка электронных оболочек реагентов, в рез. Чего могут рваться старые хим. связи и образовываться новые. Т. к. для разрыва хим. связей в исходных в-вах потребуется затратить определенную энергию, а при образовании связей в продуктах реакции она будет выделяться, то протекание рекации сопровождается изменением энергии системы. Если при при протекании химической реакции отсутствуют другие виды работы, кроме работы расширения системы, то Q=ΔU+1∫2 PdV
Обычно хим. реакции проводятся при постоянном объеме или давлении. При постоянном объеме Q=ΔUV, а при постоянном давлении Qp=ΔH=ΔUp+PΔV/
Объем (давление) системы должен оставаться постоянным на всем пути от начала процесса до его завершения, только при этих условиях будут справедливы полученные уравнения. Для идеальных газовых смесей вн. энергия не зависит ни от объема, ни от давления (ΔUv= ΔUp), а для реальных газовых систем при высоких давлениях можно принять ΔUv≈ ΔUp.
Теплота Qp=ΔH=ΔUp+PΔV – тепловой эффект при постоянном давлении.
Под тепловым эффектом хим. р-ции понимают количество теплоты, которое выделяется или поглощается в условиях а) процесс протекает необратимо при постоянных объеме и давлении; б) в системе не совершается никаких работ, кроме расширения системы; в) продукты реакции имеют ту же температуру, что и исходные вещества. Тепловой эффект реакции не зависит от пути процесса (промежуточных стадий), а определяется только начальным и конечным состоянием системы.
Комбинируя ур-я получаем: Qp-Qv= PΔV. Отсюда вытекает, что разность тепловых эффектов при постоянном давлении и постоянном объеме равна работе, которая совершается системой (ΔV>0) или над системой (ΔV<0) за счет изменения ее объема при завершении изобарно-изотермических реакций. При изохорном процессе вся теплота, подводимая или отводимая от рабочего тела, расходуется на изменение внутренней энергии.
Теплоты образования веществ из элементов.
Теплота любой реакции (даже пока не осуществленной на практике) может быть вычислена как разность между суммой теплот образования всех продуктов и суммой теплот образования всех реагентов в данной реакции.
Принято использовать теплоты образования соединений из чистых элементов в стандартных условиях. Такие стандартные условия чаще называют стандартным состоянием веществ:
1. Для твердых, жидких и газообразных веществ стандартное состояние определяется как наиболее распространенная форма элемента при 25 оС (298 К) и давлении 1 атмосфера (1 атм).
2. Теплота образования чистых элементов по определению равна нулю.
Во многих случаях эти реакции
протекают при постоянном объеме или
постоянном давлении. Из первого закона
термодинамики следует, что при этих
условиях теплота является функцией
состояния. При постоянном объеме теплота
равна изменению внутренней энергии:
![]()
![]()
а при постоянном давлении
- изменению энтальпии:
![]()
![]() Эти равенства в применении к химическим
реакциям составляют суть закона Гесса:
Эти равенства в применении к химическим
реакциям составляют суть закона Гесса:
Из закона Гесса можно сформулировать два полезных следствия:
1. Тепловой эффект реакции равен алгебраической сумме теплот
образования продуктов реакции за вычетом суммы теплот образования
исходных веществ, т.е.
∆H = ∑ ∆H f − ∑ ∆H f . (3)
продукты исходн.
2. Тепловой эффект реакции равен алгебраической сумме теплот сгорания
исходных веществ за вычетом суммы теплот сгорания
продуктов реакции, т.е.
∆H = ∑ ∆H сгор. − ∑ ∆H сгор. . (4)
исходн. продукты
Закон Гесса дает возможность устанавливать тепловые эффекты реакций,
которые невозможно или трудно осуществить в экспериментальных условиях.
Методы определения теплот образования.
1 Очень часто по тем или иным причинам тепловой эффект реакции не может быть определен непосредственно. В таких случаях его вычисляют из тепловых эффектов, непосредственно определенных для нескольких реакций, подобранных таким образом, чтобы, если бы они были произведены последовательно, то в результате получилось бы то превращение веществ, тепловой эффект которого требуется определить.
2) Для вычислений тепловых эффектов всевозможных реакций с помощью имеющихся уже термохимических данных пользуются расчетом по теплотам образования сложных веществ из элементов. Расчет производится на основании правила: тепловой эффект реакции равен разности суммы теплот образования продуктов реакции и суммы теплот образования веществ до реакции.
3) Основным экспериментальным методом термохимии является калориметрия. Чрезвычайно большое количество различных типов калориметров может быть отнесено к двум видам: калориметры с переменной температурой и калориметры с постоянной температурой. Все калориметры состоят из двух основных частей - калориметрической системы и калориметрической оболочки.
Расчет тепловых эффектов реакций с помощью средних энергий связей.
3. Теплоемкость идеального газа. Поступательная, вращательная и колебательная теплоемкости. Теплоемкость твердого тела. Уравнение Эйнштейна. Зависимость теплового эффекта химической реакции от температуры.
Теплоемкость идеального газа.
Из молекулярно-кинетической теории следует, что кинетическая энергия (WК) 1 моля идеального газа равна:
![]() ,
(2.10)
,
(2.10)
где NA - число Авогадро, равное 6,02 1023 Дж/К.
Учитывая, что
![]() можно получить:
можно получить:
![]() .
(2.11)
.
(2.11)
Используя соотношение (2.8):
![]() .
(2.12)
.
(2.12)
Уравнения (2.11) и (2.12) представляют закон Дюлонга - Пти для идеальногогаза.
Если идеальный газ одноатомный, то i = 3 и тогда:
![]() .
(2.13)
.
(2.13)
Для двухатомного газа i = 5 и тогда:
![]() .
(2.14)
.
(2.14)
В случае трехатомного газа i = 6, поэтому:
СV = 3R; СР = 4R.
Идеальный газ — математическая модель газа, в которой предполагается, что потенциальной энергией молекул можно пренебречь по сравнению с их кинетической энергией. Между молекулами не действуют силы притяжения или отталкивания, соударения частиц между собой и со стенками сосуда абсолютно упруги, а время взаимодействия между молекулами пренебрежимо мало по сравнению со средним временем между столкновениями.
Теплоёмкость тела (обозначается C) — физическая величина, определяющая отношение бесконечно малого количества теплоты ΔQ, полученного телом, к соответствующему приращению его температуры ΔT.
Теплоемкость идеального газа - это
отношение тепла, сообщенного газу, к
изменению температуры δТ, которое при
этом произошло.
![]()
Молярная теплоемкость - теплоемкость 1 моля идеального газа.
δQ = νCΔT
![]()
Для идеальных газов вн. энергия не зависит от объема и давления и ур-е – Ср–Сv=Р [dV/dР]р
Ср–Сv=R.
Для реальных газов Ср–Сv>R, и чем выше давление газа, тем больше будет разность теплоемкостей отличаться от R/
Для
Теплоемкость идеального газа в процессах
Адиабатический
В адиабатическом процессе теплообмена с окружающей средой не происходит, т.е. δQ=0. Следовательно, теплоемкость идеального газа в адиабатическом процессе также равна нулю: Садиаб=0.
Изотермический
В изотермическом процессе постоянна
температура, т.е. dT = 0. Следовательно,
теплоемкость идеального газа стремится
к бесконечности:
![]()
Изохорический
В изохорическом процессе постоянен объем, т.е. δV = 0. Элементарная работа газа равна произведению изменения объема на давление, при котором происходит изменение (δA = δVP). Первое Начало Термодинамики для изохорического процесса имеет вид:
dU = δQ = CVΔT
А для идеального газа![]() Таким
образом,
Таким
образом,
![]() где
i - число степеней свободы частиц газа.
где
i - число степеней свободы частиц газа.
Изобарический
В изобарическом процессе (P = const):
δQ = dU + PdV = νCVΔT + νRΔT = ν(CV + R)ΔT = νCPΔT
Теплоемкость, так же как и количество переданной телу теплоты, зависит от того, каким образом, а точнее при осуществлении какого процесса, теплота передавалась этому телу.
Если в процессе изменения состояния идеального газа теплоёмкость его не изменяется, то такой процесс называется политропическим. Частными случаями политропического процесса являются рассмотренные ранее изопроцессы, протекающие при постоянных значениях температуры, давления или объема.
Поступательная, вращательная и колебательная теплоемкости.
Микрочастицы (молекулы, атомы), из которых состоит газ, могут совершать, в общем случае, три типа движений: поступательное , вращательное , колебательное .
Атом как материальная точка может совершать только поступательное движение в трех направлениях (три степени свободы - i=3).
Как показано в молекулярно-кинетической теории на каждую поступательную или вращательную степень свободы каждой микрочастицы приходится энергия равная (1/2)kT (закон равномерного распределения энергии по степеням свободы). Таким образом, для одного моля газа (число микрочастиц равно числу Авогадро N), внутренняя энергия газа:
U=i(1/2)kTNА=(i/2)RT
Вращательная
теплоемкость многоатомных газов.
Свободную энергию многоатомного газа,
как и двухатомного, можно представить
в виде суммы трех частей — поступательной
, вращательной и колебательной .
Поступательная часть характеризуется
теплоемкостью и химической постоянной,
равными:
![]() ,
,
![]()
Колебательная часть термодинамических величин газа становится существенной при значительно более высоких температурах, чем вращательная , потому что интервалы колебательной структуры термов велики по сравнению с интервалами вращательной структуры.
Вычисление теплоемкости сводится к вычислению средней энергии теплового движения отдельных молекул, которое складывается из поступательных и вращательных движений молекулы как целого и из колебаний атомов внутри молекулы. Молярная теплоемкость одноатомного газа равна 3R/2 (по R/2 на каждую степень поступательного движения молекулы). Теплоемкость многоатомного газа в общем случае может быть представлена суммой вкладов от отдельных видов движения - поступательного , вращательного , колебательного .
Поступательная теплоемкость рассчитывается так же, как для одноатомного газа. Вращательная и в особенности колебательная теплоемкости должны, как правило, вычисляться на основе квантовой статистики. Согласно классической статистике, вклады в молярную теплоемкость в расчете на одну степень свободы равны: для вращательного движения R/2, для колебательного движения R. Для большинства молекул при низких и средних температурах колебательные степени свободы вырождены и не дают вклада в теплоемкость Например, теплоемкость двухатомного газа при обычных температурах равна 5R/2. Лишь при достаточно высоких температурах возбуждаются колебания определенной частоты.
Теплоемкость твердого тела.
Твердое тело можно представить в виде огромной молекулы, состоящей из отдельных атомов. Число атомов в 1 моле равно NA, тогда общее число степеней свободы – 3 NA и выражение для расчета теплоемкости принимает следующий вид:
![]() ,
(2.16)
,
(2.16)
причем СV
![]() СР.
СР.
Соотношение (2.16) – закон Дюлонга – Пти для твердых тел.
Оказалось, что для углерода, кремния и бора соотношение (2.16) не выполняется. Кроме того закон Дюлонга – Пти не учитывает температурную зависимость теплоемкости.
Уравнение Эйнштейна.
Зависимость теплового эффекта химической реакции от температуры.
В общем случае тепловой эффект химической реакции зависит от температуры и давления, при которых проводится реакция. Влиянием давления на ΔН и ΔU реакции обычно пренебрегают. Влияние температуры на величины тепловых эффектов описывает закон Кирхгофа:
Большинство экспериментальных определений теплот реакций относится к комнатной температуре, хотя практически важно знать его значение при любой температуре. Первое начало термодинамики позволяет определить зависимость теплового эффекта от температуры и осуществлять соответствующие термохимические расчеты.
Для реакции вида:
![]() ,
(3.21)
,
(3.21)
где
![]() - коэффициенты;
- коэффициенты;
М1, М2, ..., N1,
N2, ... – продукты
химической реакции, тепловой эффект
![]() .
.
![]() .
(3.22)
.
(3.22)
Тогда:
![]() .
(3.23)
.
(3.23)
После дифференцирования по температуре:
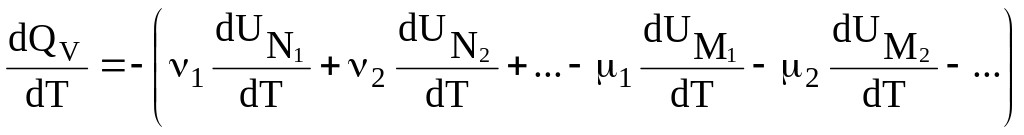 ,
(3.24)
,
(3.24)
где
![]() - температурный коэффициент теплового
эффекта химической реакции;
- температурный коэффициент теплового
эффекта химической реакции;
Учитывая, что = СV:
![]() (3.25)
(3.25)
или
![]() .
(3.26)
.
(3.26)
Уравнение (3.26) – уравнение Кирхгофа в дифференциальной форме записи, которое читается:
“Температурный коэффициент теплового эффекта химической реакции равен изменению теплоемкости системы за счет этой реакции.”
Если
![]() ,
то
,
то
![]() ,
т. е. с повышением температуры тепловой
эффект химической реакции уменьшается.
,
т. е. с повышением температуры тепловой
эффект химической реакции уменьшается.
Если
![]() ,
то
,
то
![]() и с повышением температуры тепловой
эффект химической реакции возрастает.
и с повышением температуры тепловой
эффект химической реакции возрастает.
При
![]() ,
то
,
то
![]() и температура не влияет на величину
теплового эффекта химической реакции.
и температура не влияет на величину
теплового эффекта химической реакции.
После разделения переменных и интегрирования:
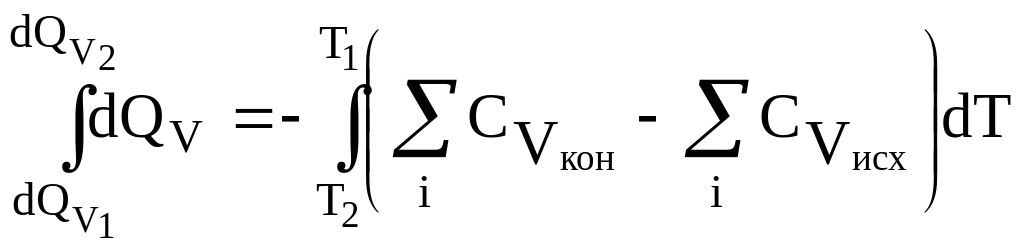 .
(3.27)
.
(3.27)
где
![]() .
.
Тогда
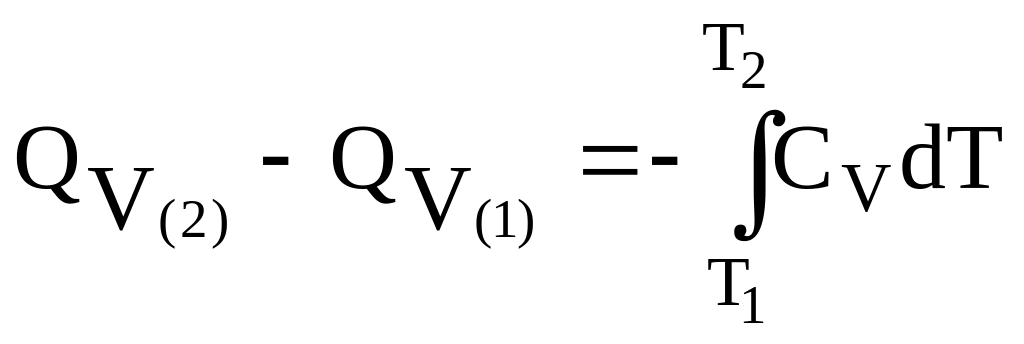 (3.28)
(3.28)
и по аналогии:
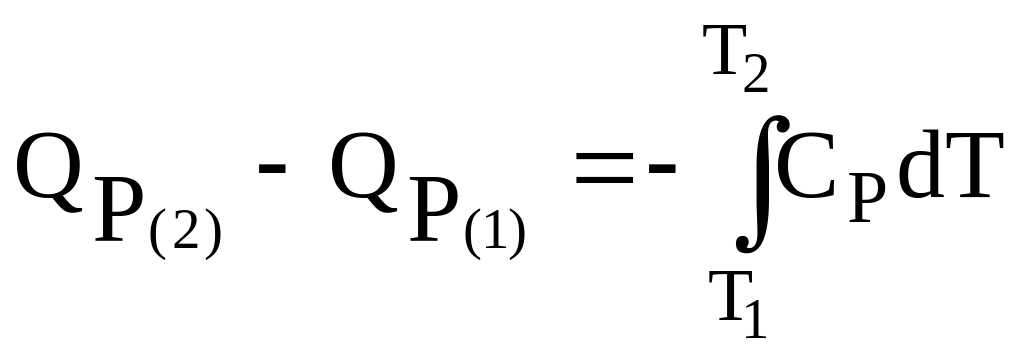 .
(3.29)
.
(3.29)
Уравнения (3.28) и (3.29) – уравнения Кирхгофа в интегральной форме записи.
В обобщенной форме записи:
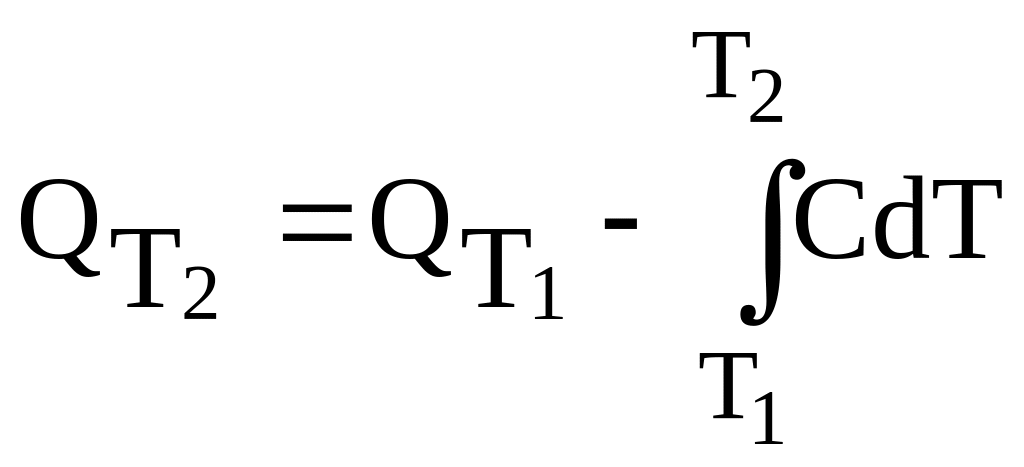 .
(3.30)
.
(3.30)
Кроме того:
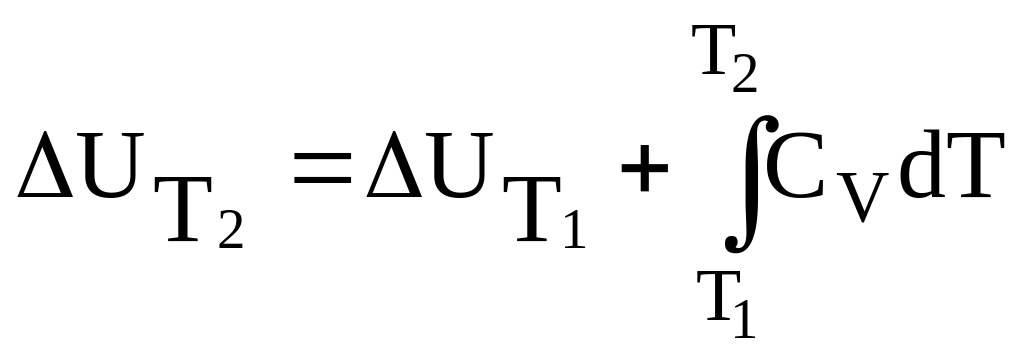 ,
(3.31)
,
(3.31)
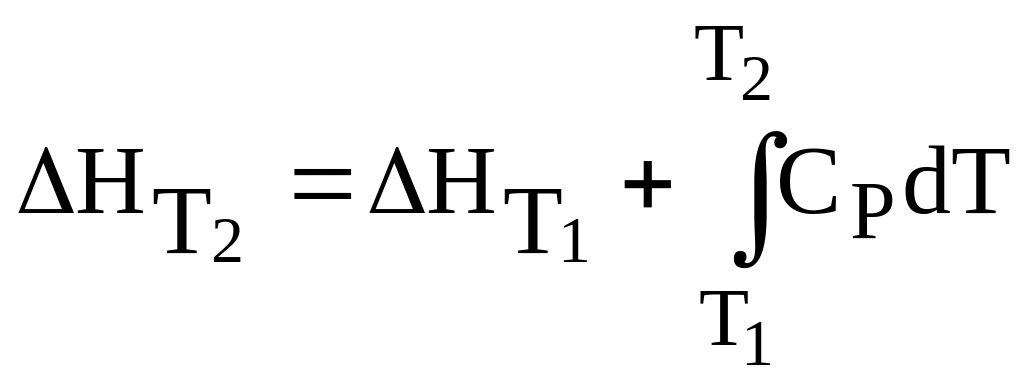 .
(3.32)
.
(3.32)
Таким образом, для нахождения величины теплового эффекта химической реакции при заданной температуре необходимо знать его величину при любой другой температуре и располагать уравнениями Сi = f (T).
