
- •Образ природы в неклассическом естествознании: тепловое излучение тел. Законы Вина и Стефана – Больцмана. Гипотеза Планка. Квантово – волновой дуализм света.
- •Образ природы в неклассическом естествознании: явление внешнего фотоэффекта.
- •Образ природы в неклассическом естествознании: гипотеза де Бройля. Соотношения неопределенностей.
- •Образ природы в неклассическом естествознании: квантовая механика. Уравнение Шредингера. Физический смысл волновой функции.
- •Образ природы в неклассическом естествознании: физика атома. Опыт э. Резерфорда. Квантовые числа, определяющие состояние электрона в атоме.
- •Образ природы в неклассическом естествознании: четыре фундаментальных взаимодействия в природе. Классификация элементарных частиц.
- •Квантовая физика в современных технологиях: ядерная энергетика. Дефект массы, энергия связи. Устойчивость ядер. Реакции деления (ядерный реактор, атомная бомба) и термоядерного синтеза.
- •Квантовая физика в современных технологиях: полупроводники.
- •Квантовая физика в современных технологиях: лазеры.
- •10 . Неклассические концепции в химии: Тепловой эффект и химическое равновесие реакции.
- •I. Тепловой эффект реакции.
- •II. Химическое равновесие реакции.
- •11. Неклассические концепции в химии: Скорость химической реакции.
- •12. Методы описания многочастичных систем, термодинамика, понятие о равновесном состоянии, уравнение состояния идеального газа. Статические распределения.
- •13. Основные положения классической термодинамики. Первое и второе начала термодинамики. Понятие об обратимых и необратимых процессах.
- •14. Второе начало термодинамики и энтропия. Энтропия, как мера беспорядка в системе. Формула Бельцмана.
- •15. Второе начало термодинамики и эволюционная парадигма. Открытые термодинамические системы. Понятия потока и градиента.
- •16. Основы неравновесной термодинамики. Градиент, поток, Флуктуация. Поведение различных систем при возникновении флуктуаций.
- •17. Понятие самоорганизации. Ячейки Бенара, диссипативные структуры, точка бифуркации. Бифуркционная диаграмма открытой сильнонеравновесной системы.
- •18. Самоорганизация и энтропия. Принцип Пригожина – Гленсдорфа.
- •19. Характерные признаки самоорганизации. Эволюционно – синергетическая парадигма.
- •20. Классическая наука о Вселенной. Возраст и размеры Вселенной. Закон Хаббла. Современная космологическая модель Вселенной.
- •21. Эволюция звёзд. Образование планетных систем. Гипотезы дальнейшего развития Вселенной. Эволюция Земли.
- •22. Эволюционные идеи в химии. Три основных направления исследований.
- •23. Эволюционные идеи в биологии. Концепции происхождения жизни на Земле.
- •24. Термодинамика и энергетика живых систем.
- •25. Концепция структурных уровней организации жизни: краткая характеристика каждого из уровней.
- •Молекулярно-генетический уровень.
- •27. Концепция структурных уровней организации жизни: клетка.
- •28. Воспроизводство жизни: днк, её состав и свойства.
- •29. Воспроизводство жизни: рнк, её состав и свойства.
- •30. Воспроизводство жизни: три стадии процесса воспроизводства. Ген. Основные направления развития генной инженерии.
- •31. Человек и природа: учение о биосфере.
- •32. Современный экологический кризис, его основные симптомы. Учение в.И. Вернадского о ноосфере.
Образ природы в неклассическом естествознании: физика атома. Опыт э. Резерфорда. Квантовые числа, определяющие состояние электрона в атоме.
Джозеф Томсон, английский физик 1897 г. - открытие электрона.
Опыты Резерфорда 1908 г. – облучение тонких металлических пластинок a - частицами: 1/10000 часть частиц отражалась на большой угол.
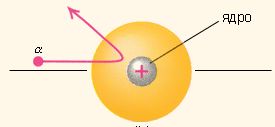 -
планетарная модель атома
-
планетарная модель атома
Противоречия планетарной модели атома
При движении по окружности электроны по теории Максвелла будут излучать волны.
Спектр излучения должен быть сплошным, а на опыте он линейчатый.
Излучая энергию, электроны потеряют энергию и упадут на ядро.
Современная модель атома
Из решения уравнения Шредингера следует, что состояние электрона в атоме определяется четырьмя квантовыми числами:
n = 1, 2, 3, … - главное квантовое число.
Определяет энергию электрона и размеры электронного облака.
l = 0, 1, 2, …, (n –1) - орбитальное квантовое число.
m = 0, ±1, ±2, … ± l - магнитное квантовое число.
Числа l и m определяют орбитальный момент импульса электрона, конфигурацию и ориентацию электронного облака.
ms = ± ½ - спиновое квантовое число.
Определяет собственный момент импульса электрона.
(Электронные облака (орбитали) - совокупность точек, в которых велика вероятность нахождения электрона.)
Образ природы в неклассическом естествознании: четыре фундаментальных взаимодействия в природе. Классификация элементарных частиц.
Сильное – взаимодействие протонов и нейтронов в ядрах атомов (радиус взаимодействия ~ 10–15 м);
Электромагнитное – взаимодействие электрических зарядов, токов, электрических и магнитных полей (радиус взаимодействия до ∞);
Слабое – взаимодействие элементарных частиц при радиоактивном распаде (радиус взаимодействия ~10–15 м);
Гравитационное – взаимодействие всех тел (радиус взаимодействия до ∞).
Взаимодействия осуществляются посредством обмена элементарными частицами, их известно более 400.
Основные характеристики частиц
Масса.
В середине прошлого столетия была создана классификация элементарных частиц по массе

Фотоны –частицы с массой покоя, равной нулю. Участвуют в электромагнитных взаимодействиях.
Лептоны – легкие частицы (электрон, позитрон, нейтрино…) Участвуют во всех взаимодействиях, кроме сильного.
Адроны – крупные частицы, участвуют во всех видах взаимодействий:
Мезоны – обмен этими частицами обеспечивает сильное взаимодействие частиц ядра
Барионы - протон, нейтрон и гипероны.
Сверхэлементарные частицы - шесть кварков, М. Гелл-Ман и Д. Цвейг, американские физики, 1963 г.
Мезоны – 2 кварка, барионы – 3 кварка.
Электрический заряд: 0, +|е|, −|е|.
Среднее время жизни:
Стабильные частицы:
фотон
две разновидности нейтрино
электрон
протон.
Нестабильные частицы – все остальные, время жизни ~ 10-8 – 10-24 с.
Спин (собственный момент импульса частицы) и квантовые числа.
Квантовая физика в современных технологиях: ядерная энергетика. Дефект массы, энергия связи. Устойчивость ядер. Реакции деления (ядерный реактор, атомная бомба) и термоядерного синтеза.
![]()
Z – порядковый номер элемента, число протонов в ядре;
А – массовое число, общее число протонов и нейтронов (нуклонов).
Изотопы – ядра с одинаковым Z, но разным А.
Дефект
массы ядра:
![]()
Энергия связи ядра - энергия, необходимая для расщепления ядра на составляющие его нуклоны:
![]()
Устойчивость ядер
Удельная энергия связи - энергия связи, приходящаяся на один нуклон ядра:
![]()

Чем больше удельная энергия связи, тем более устойчиво ядро.
Реакция деления.
а) Ядерные реакторы.
Первые реакторы – 1942 г., Э. Ферми, США и 1949 г., И.В. Курчатов, Россия.
Делящееся вещество – смесь изотопов урана U238 и U235 (или плутоний Рu239).
При попадании в ядро нейтрона оно делится, испуская два или три вторичных нейтрона. Может возникнуть цепная реакция.
В зависимости от скорости нейтроны делятся на быстрые и медленные.
Медленными нейтронами делится только изотоп урана U235. Природный уран U238 «обогащают» и используют их смесь.
Схема активного блока ядерного реактора
1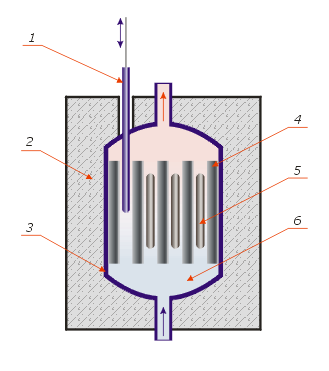 – Управляющий стержень
– Управляющий стержень
(поглотитель нейтронов
из бора или кадмия).
2 – Биологическая защита.
3 – Тепловая защита.
4 – Замедлитель (сам уран
и графит).
5 – Ядерное топливо.
6 – Теплоноситель.
б) Атомная бомба.
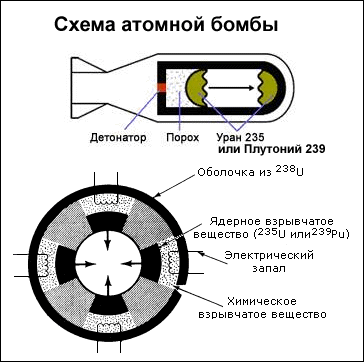
После взрыва пороха масса активного вещества становится больше критической и происходит неуправляемая цепная реакция.
